编者按:
帕金森症是一种常见的中老年人神经系统变性疾病。近年来,随着人口老龄化的加剧,帕金森症的发病率激增。我国 65 岁以上人群的患病率大约为 1.7%,总患病人数在 200 万以上。然而,目前针对帕金森症尚无立竿见影的治愈方法。
而研究发现帕金森症患者往往会先出现一些非运动症状,如胃肠道症状、抑郁症和睡眠不足。那么,肠道菌群和帕金森症之间的是否存在关联呢?是否可以利用肠道菌群预防和治疗帕金森症呢?
今天,我们特别关注肠道菌群与帕金森症,希望本文能够为相关的产业人士和各位读者带来一些启发与帮助。
帕金森症
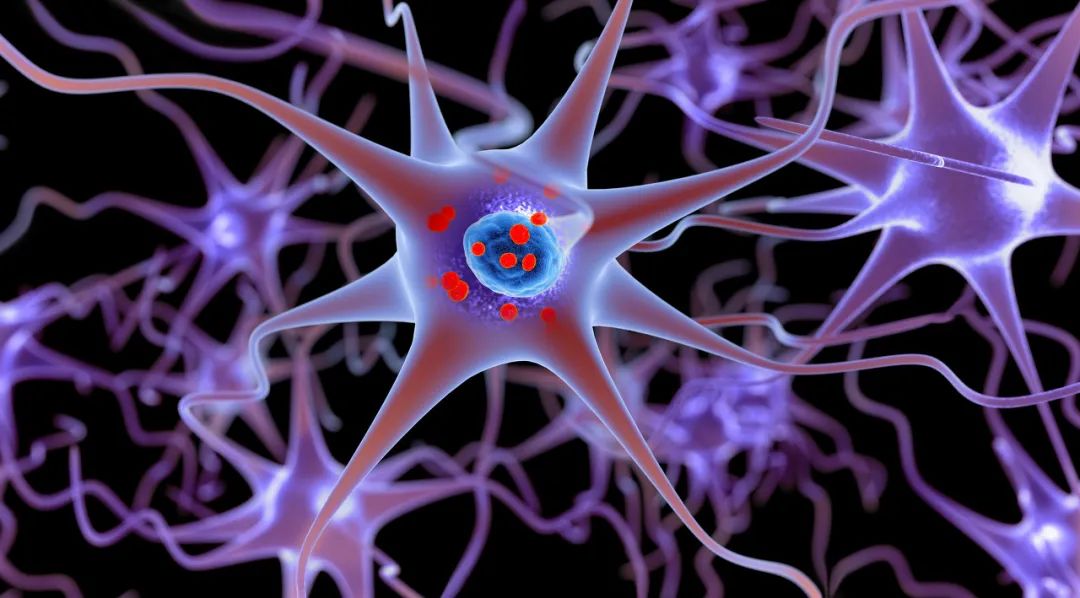
帕金森症(PD)是一种常见的神经系统变性疾病,其特征是肌肉静息时出现震颤(静止性震颤)、肌张力增高(僵直或强直)、自主运动缓慢、维持平衡困难(姿势不稳)。还有许多患者会出现思考障碍或痴呆等1。
目前,关于帕金森病的病因仍不明确。有一种理论认为,帕金森病是由 α-突触核蛋白(脑内一种帮助神经细胞间信息传递的蛋白质)异常沉积引起的,这种沉积物称为 Lewy 体,主要聚集在脑内几个区域,尤其是在黑质处(大脑深部)。Lewy 体的出现会导致多巴胺能神经元死亡,从而影响大脑功能,并进一步造成运动障碍以及行为和认知问题1。
现在,我们通常认为遗传因素、环境因素、衰老、氧化应激等均可能参与到多巴胺能神经元的变性死亡过程中。
然而,除了上面提及的显著震颤和运动症状外,帕金森症患者往往还会先出现一些非运动症状,如睡眠障碍、抑郁症和胃肠道症状(高达 75%的帕金森症患者表现出了胃肠道异常2)。而且帕金森症患者大脑中的 Lewy 体,也可以在肠道的神经细胞中找到,这不禁让人怀疑,帕金森症是否起源于肠道?或者说,肠道以及肠道菌群是否与帕金森症之间存在一定的联系呢?

进展1: 帕金森症源起肠道?
2017 年,一项发表于 npj Parkinson’s Disease 杂志的研究讨论了肠道菌群与帕金森症之间的联系,该研究提出了一种帕金森症发病机理的模型,认为该疾病起源于肠道,并以炎症为基础机制不断发展3。
芬兰赫尔辛基大学医院(Helsinki University Hospital)的神经学家 Filip Scheperjans 相信帕金森症与肠道之间存在某种关系,他的主要研究方向是肠道菌群与帕金森症。
2014 年,Scheperjans 团队的研究发现,与健康对照组相比,帕金森症患者肠道菌群中普氏菌(Prevotellaceae)的平均丰度减少了 77.6%4。该研究还发现帕金森症患者肠道菌群的变化与他们的运动症状有关: Enterobacteriaceae 细菌的相对丰度与姿势不稳定和步态困难的严重程度呈正相关。
除了这项研究以外,其他研究也发现了与帕金森症相关的肠道菌群的变化,但是在这些研究中关于帕金森症的生物标记物并不一致。
Hill Burns 等人的一项研究揭示了帕金森症患者肠道菌群的失调特征,该研究发现帕金森患者肠道内的双歧杆菌科、Christensenellaceae、Tissierellaceae、毛螺旋菌、乳杆菌科、巴斯德菌科和疣微菌科的丰度显著变化5。这项研究纳入了 197 位帕金森病人和 130 位健康人,是迄今为止关于帕金森症患者肠道菌群样本量最大的研究。
而今年 5 月发表的一项最新研究发现,无论胃肠道功能如何,帕金森症患者的粪便菌群均与健康人存在显著差异。此外,该研究还发现患者的粪便菌群代谢功能发生显著变化:碳水化合物发酵及丁酸盐合成减少,而蛋白水解及有害氨基酸代谢产物生成增加。这些变化与患者的粪便硬度及便秘密切相关。
关于该研究《热心肠日报》做过简要报道:
肠道菌群的组成及代谢与帕金森病患者的肠道健康相关
Movement Disorders——[8.061]
① 纳入197名帕金森病患者及103名健康人,对粪便菌群进行测序分析,并对血清进行非靶向代谢组学分析;② 无论胃肠道功能如何,帕金森病患者的粪便菌群组成显著不同于健康人;③ 患者的粪便菌群代谢功能发生显著改变,表现为碳水化合物发酵及丁酸盐合成的减少,蛋白水解及有害氨基酸代谢产物(包括对甲酚及苯乙酰谷氨酰胺)生成的增加;④ 粪便菌群组成的变化及血清蛋白水解产物的增加与患者的粪便硬度及便秘密切相关。
Microbiota Composition and Metabolism Are Associated With Gut Function in Parkinson's Disease
05-01, doi: 10.1002/mds.28052
【主编评语】Movement Disorders上发表的一项横断面队列研究,对比分析了帕金森病患者与健康人的肠道菌群差异,发现患者的菌群组成及代谢功能均发生了显著变化,其中,血清中有害菌群蛋白水解产物的增加与患者的便秘症状密切相关。(@szx)
除此之外,还有研究表明肠道中噬菌体也与帕金森症存在一定的联系。人类的胃肠道不仅是细菌、古细菌的家园,也是真菌和病毒的家园。近年来的研究发现,肠道中存在的噬菌体(一种是感染和破坏细菌的病毒)对宿主的健康具有重要意义。
而一项关于帕金森症的研究表明,药物依赖的帕金森症患者肠道中的乳球菌仅有健康对照组的 1/10。值得注意的是,乳球菌的减少的同时,溶解性噬菌体会增加,这暗示帕金森症患者肠道中乳球菌的减少可能是由溶解性噬菌体引起的6。
另外,还有研究团队探索了肠道菌群与帕金森症引发的运动障碍之间的联系2。该团队利用 α-突触核蛋白过表达小鼠,一种帕金森症小鼠模型,发现如果这种小鼠缺乏肠道菌群,那么它们大脑中 α-突触核蛋白沉积会减少,行动也会更灵活。
进一步该团队研究了肠道中产生的短链脂肪酸失衡是否与大脑中激活的免疫反应有关。研究人员用帕金森症患者肠道微生物产生的短链脂肪酸处理无菌小鼠后发现,这种小鼠的脑中有更高水平的神经炎症,而这种炎症与小胶质细胞激活导致的神经元功能紊乱有关。
他们还对小鼠进行了粪便移植,结果显示接受帕金森症患者粪便的小鼠会出现运动功能缺陷。
另外,肠道菌群还可能通过另一种途径——肠神经系统,影响帕金森症。一项研究证明迷走神经干切断术(把迷走神经干从食道至胃的一段切除)与帕金森症风险的降低有关7。
这些研究提示我们肠道菌群可能在帕金森症的发展过程中起着关键作用。然而,肠道菌群还可能会通过影响抗帕金森药物的治疗效果来影响帕金森症。
一项发表于 Nature Communications 的研究表明,肠道中某些细菌产生的酪氨酸脱羧酶,能够将左旋多巴转化为多巴胺,影响小肠近端对药物的吸收,从而影响左旋多巴联合卡比多巴治疗帕金森症的疗效。
关于该研究《热心肠日报》做过简要报道:
Nature子刊:肠道细菌脱羧酶影响帕金森病治疗
Nature Communications——[11.878]
① 含有酪氨酸脱羧酶(TDC)的肠道细菌能将左旋多巴转化为多巴胺,影响左旋多巴联合卡比多巴治疗帕金森(PD)的疗效;② TDC的竞争性抑制剂酪氨酸以及人TDC抑制剂,均不能抑制细菌TDC的左旋多巴脱羧作用;③ PD病人粪便菌群中编码TDC的基因丰度越高, 左旋多巴联合卡比多巴的用药剂量越大、治疗时间越长;④ 小肠近端是吸收左旋多巴的主要区段,大鼠中该区域TDC丰度与血液中左旋多巴含量呈负相关;⑤ 小肠近端细菌TDC丰度可解释PD病人的用药情况。
Gut bacterial tyrosine decarboxylases restrict levels of levodopa in the treatment of Parkinson’s disease
2019-01-18, doi: 10.1038/s41467-019-08294-y
【主编评语】肠道菌群不仅影响宿主健康状态,更会影响药物治疗效果。本文通过研究PD病人粪便菌群和实验动物模型,发现肠道细菌产生的酪氨酸脱羧酶能够左旋多巴转化为多巴胺,影响小肠近端的左旋多巴吸收,从而影响巴联合卡比多巴治疗帕金森的疗效。该结果对研究药物-菌群互作、提高帕金森药物治疗效果具有参考价值。(@周旸)
反之,某些药物如抗生素等的使用也可能会通过改变肠道菌群的组成影响帕金森症。
进展2: 抗生素对帕金森症的影响
过去的研究已经发现过度接触抗生素会改变肠道菌群组成,而特定的肠道菌群组成可能会增加罹患精神疾病、克罗恩病和结直肠癌的风险。现在,研究人员们也开始研究抗生素使用与帕金森症之间的潜在联系。
Scheperjans 在一份新闻稿中说:“众所周知,帕金森症患者的肠道菌群组成异常,但病因尚不清楚。帕金森症的病理可能起源于肠道,并且可能与微生物的变化有关,所以抗生素暴露与帕金森症之间的联系符合目前的潮流观点。我们的研究结果表明,一些常用的抗生素,会剧烈地影响肠道菌群,这很可能是帕金森症的诱发因素。”
为了进一步探讨抗生素高暴露与帕金森症发病之间的可能联系,芬兰赫尔辛基大学医院的研究人员进行了一项全国性的病例对照研究,以比较帕金森症患者和正常人的抗生素暴露情况。该研究于 2019 年 11 月发表于 Movement Disorders 杂志8。
这项研究的大数据样本来自国家登记处,包含了 1998 年至 2014 年间在芬兰被诊断为帕金森症的 13976 人,以及 40697 名年龄、性别、居住地点相同的非帕金森症患者(对照组)。研究人员根据购买口服抗生素的数据确定抗生素暴露情况,然后对三个不同的时间段进行了分析:帕金森症发作前 1~5 年、5~10 年和 10~15 年。
“84.9%的帕金森症患者和对照组中 83.6%的人至少购买了一个抗菌药物。青霉素的购买频率最高,占全部购买量的 22.8%,”研究人员如是说。平均而言,帕金森症患者比对照组购买的抗生素更多,但对照组因细菌感染住院的频率更高。
与帕金森症联系最密切的是口服大环内酯类和林可酰胺类抗生素,这两类抗生素针对不同类型的细菌,通过阻止细菌产生生存所需的蛋白质而起杀菌作用。
进一步的分析表明,暴露于广谱抗生素如四环素,以及那些专门针对厌氧菌的抗生素,与 10~15 年内帕金森症风险增加有关。此外,其他类型的抗生素,如磺胺类和甲氧苄啶,以及抗真菌药物,被发现与 1~5 年内帕金森症风险增加有关。
研究人员说:“虽然还不能得出因果关系的结论,但口服抗生素似乎是使胃肠道更易受(帕金森症)病理影响的一个因素,增加了患病的风险。我们的发现需要在不同的研究中得到证实。如果真的得到证实,那么普通口服抗生素和神经变性之间的联系可能会对处方实践和公共卫生产生重大影响。”
如果肠道菌群的改变确实与帕金森症的发生有关,那么我们是否可以利用肠道菌群预防或者治疗这类疾病呢?
进展3: 益生菌可改善帕金森?
爱丁堡大学和邓迪大学的研究人员们正在研究益生菌是否能够改善帕金森症。
研究人员首先构建了一种能表达人 α-突触核蛋白的线虫模型,再给线虫饲喂各种非处方益生菌,结果他们发现一种特定的益生菌——枯草芽孢杆菌(Bacillus subtilis)能够清除线虫的一些 α-突触核蛋白团块,并改善运动障碍文章。他们的研究结果于 2020 年 1 月发表在 Cell Reports 杂志上9。
这项研究的通讯作者爱丁堡大学发现脑科学中心(Centre for Discovery Brain Sciences)的 Maria Doitsidou 博士在一份声明中说:“这些研究结果提供了一个机会,可以研究改变构成肠道菌群的细菌对帕金森症的影响。”
Doitsidou 和他的同事发现,枯草芽孢杆菌是通过改变对鞘脂(一种特定的脂肪)的酶促反应而起作用的,这种益生菌产生的化学物质可以调节线虫的代谢途径(如鞘脂代谢),进而阻止 α-突触核蛋白形成团块。
但这一结果并不意味着每个帕金森患者都应该立马去药店买益生菌,研究人员警告说,这一发现仍需要在小鼠身上以及在大规模临床试验中得到证实。但他们相信,这确实支持了先前的发现,即肠道微生物与帕金森症有关,同时为利用肠道菌群改善帕金森症提供了可能。
这项益生菌研究由英国帕金森症基金会资助,该基金会希望相关的临床试验能够尽快进行。该组织的研究经理 Beckie Port 博士在声明中说:“研究发现了一种对帕金森症有益的细菌,不仅有可能改善症状,甚至可以在一开始就保护人们不患上这种疾病。”
进展4: 微生物疗法或成帕金森治疗新希望
除了利用益生菌治疗帕金森症的手段之外,还有研究报道监测肠道健康状况能够帮助我们防患帕金森症3。
研究人员指出:“荟萃分析表明,帕金森症患者出现便秘的几率是正常人的两倍多,而便秘患者在评估后 10 年内发生帕金森症的可能性也高出正常人两倍。根据这些结果,我们也许能更好地理解消化和中枢神经系统之间的联系,并且有助于我们在帕金森症的早期阶段开发治疗方法。”
而 2018 年,密歇根州范安德研究所的研究发现,切除阑尾的人患帕金森症的几率降低了 25%——他们怀疑这一现象与他们在阑尾组织中发现 α-突触核蛋白团有关10。所以如果能清除肠道中的 α-突触核蛋白,就极有可能预防帕金森症。
此外,一篇发表于 Science 杂志的研究确定了两种共同作用代谢人类肠道中左旋多巴的酶,这两种酶由不同的细菌产生。因此,只要阻断其中一种细菌酶,或可显著提高药物对帕金森症患者的疗效11。
粪菌移植是常见的微生物疗法之一。一项由江南大学发表的关于粪菌移植的相关研究发现12,把帕金森症小鼠的粪便菌群移植给正常小鼠,后者产生运动障碍,且纹状体神经递质减少。相反,如果将正常小鼠的粪便菌群移植给帕金森症小鼠,可缓解肠道菌群失调和肢体障碍,从而改善帕金森症小鼠的症状。
除此之外,一个医学案例报道称,一位患帕金森症 7 年、顽固性便秘 3 年的老人在粪菌移植后可以在 5 分钟内顺利排便,并保持每日排便通畅,直至随访结束。患者下肢震颤在粪菌移植后 1 周内几乎消失13。虽然在粪菌移植两个月后,老人右下肢的震颤又复发了,但这说明肠道菌群的重建可能对帕金森病患者有治疗作用,特别是那些具有胃肠道症状的患者。
目前,生物制药领域也有许多企业开始以帕金森症患者的肠道-大脑连接为中心研发能有效抗击帕金森症的药物。
2016 年,加州理工学院的研究人员在小鼠模型中发现一些肠道细菌会促进帕金森症的发展。基于该研究,他们创办了一家名为 Axial Biotherapeutics 的公司,以寻求针对该疾病和其他中枢神经系统疾病的微生物治疗法。2019 年 2 月,该公司在 B 轮融资中筹集了 2500 万美元。
肠道菌群会带来春天吗?
虽然肠道菌群与帕金森症的关系才刚刚起步,但是近年来的研究已经表明肠道菌群与帕金森症之间存在一定的关联。这些研究有助于解释帕金森症的发病机制,并为我们提供预防与治疗帕金森症的新疗法。
此外,帕金森症很可能是一种多发性疾病,也许微生物组无法完全解释该病的发病机理,但是相信随着我们不断深入研究肠道菌群与帕金森症之间的关系,我们会在可期的未来拥有更多治愈帕金森症的新疗法。
参考文献:
(滑动下方文字查看)
1.https://www.msdmanuals.cn/home/brain,-spinal-cord,-and-nerve-disorders/movement-disorders/parkinson-disease-pd
2.T. Sampson, J. Debelius, T. Thron, S. Janssen, S.M.J. Cell, GutMicrobiota Regulate Motor Deficits and Neuroinflammation in a Model ofParkinson’s Disease, 167(6) (2016) 1469-1480.e12.
3.M.C. Houser, M.G. Tansey, The gut-brain axis: is intestinal inflammationa silent driver of Parkinson's disease pathogenesis?, Npj Parkinson Dis 3(2017).
4.F. Scheperjans, V. Aho, P.A.B. Pereira, K. Koskinen, L. Paulin, E.Pekkonen, E. Haapaniemi, S. Kaakkola, J. Eerola-Rautio, M. Pohja, E. Kinnunen,K. Murros, P. Auvinen, Gut Microbiota Are Related to Parkinson's Disease andClinical Phenotype, Movement Disord 30(3) (2015) 350-358.
5.E.M. Hill-Burns, J.W. Debelius, J.T. Morton, W.T. Wissemann, M.R. Lewis,Z.D. Wallen, S.D. Peddada, S.A. Factor, E. Molho, C.P. Zabetian, R. Knight, H.Payami, Parkinson's Disease and Parkinson's Disease Medications Have DistinctSignatures of the Gut Microbiome, Movement Disord 32(5) (2017) 739-749.
6.G. Tetz, S.M. Brown, Y.H. Hao, V. Tetz, Parkinson's disease andbacteriophages as its overlooked contributors, Sci Rep-Uk 8 (2018).
7.B. Liu, F. Fang, N.L. Pedersen, A. Tillander, J.F. Ludvigsson, A. Ekbom,P. Svenningsson, H. Chen, K. Wirdefeldt, Vagotomy and Parkinson disease: ASwedish register-based matched-cohort study, Neurology 88(21) (2017) 1996-2002.
8.T.H. Mertsalmi, E. Pekkonen, F. Scheperjans, Antibiotic exposure and riskof Parkinson's disease in Finland: A nationwide case-control study, Mov Disord35(3) (2020) 431-442.
9.Goya M E, Xue F, Sampedro-Torres-Quevedo C, et al. Probiotic Bacillussubtilis Protects against α-Synuclein Aggregation in C. elegans[J]. CellReports, 2020, 30(2): 367-380. e7.
10.B.A. Killinger, Z. Madaj, J.W. Sikora, N. Rey, A.J. Haas, Y. Vepa, D.Lindqvist, H.L. Chen, P.M. Thomas, P. Brundin, L. Brundin, V. Labrie, Thevermiform appendix impacts the risk of developing Parkinson's disease, SciTransl Med 10(465) (2018).
11.V. Maini Rekdal, E.N. Bess, J.E. Bisanz, P.J. Turnbaugh, E.P. Balskus,Discovery and inhibition of an interspecies gut bacterial pathway for Levodopametabolism, Science 364(6445) (2019).
12.Sun M F, Zhu Y L, Zhou Z L, et al. Neuroprotective effects of fecalmicrobiota transplantation on MPTP-induced Parkinson’s disease mice: Gutmicrobiota, glial reaction and TLR4/TNF-α signaling pathway[J]. Brain,behavior, and immunity, 2018, 70: 48-60.
13.H. Huang, H. Xu, Q. Luo, J. He, M. Li, H. Chen, W. Tang, Y. Nie, Y.Zhou, Fecal microbiota transplantation to treat Parkinson's disease withconstipation: A case report, Medicine (Baltimore) 98(26) (2019) e16163.
作者|赵婧
审校|617


