编者按:
微生物与人体之间存在着复杂的关联,一些微生物入侵人体可能会导致严重的疾病,而另一些微生物则可能在默默守护着人体健康。
艰难梭菌是一种革兰氏阳性菌,其引发的感染已经在全球范围内造成重大的健康和经济负担。今天,我们特别关注艰难梭菌,介绍其致病机制及正在研发的最新治疗手段。希望本文能够为相关的产业人士和诸位读者带来一些启发和帮助。
艰难梭菌(Clostridioides difficile)又称难辨棱状芽孢杆菌,是一种可形成孢子的厌氧性梭菌属细菌。该细菌是一种肠道病原体,会引发严重腹泻,甚至可导致死亡。
艰难梭菌感染(CDI)是美国最常见的医疗相关感染。2011 年,艰难梭菌大约感染了 50 万人,导致约 2.9 万人死亡,医疗支出增加 48 亿美元。
这种病原体可形成具有高度传染性和耐受力的孢子,并通过粪口途径传播。当接触到肠道中的初级胆汁酸后,艰难梭菌会滋生。在没有正常微生物群定植抵抗的情况下,该病原体会定植于结肠并产生毒素。这些毒素会抑制宿主细胞的肌动蛋白聚合,导致细胞死亡。随后,艰难梭菌细胞可以在肠道内孢子化,并通过腹泻排出体外。
通过培养发现,营养贫瘠会诱发艰难梭菌在分裂静止期生成孢子,但孢子生成的肠道诱因仍不清楚。
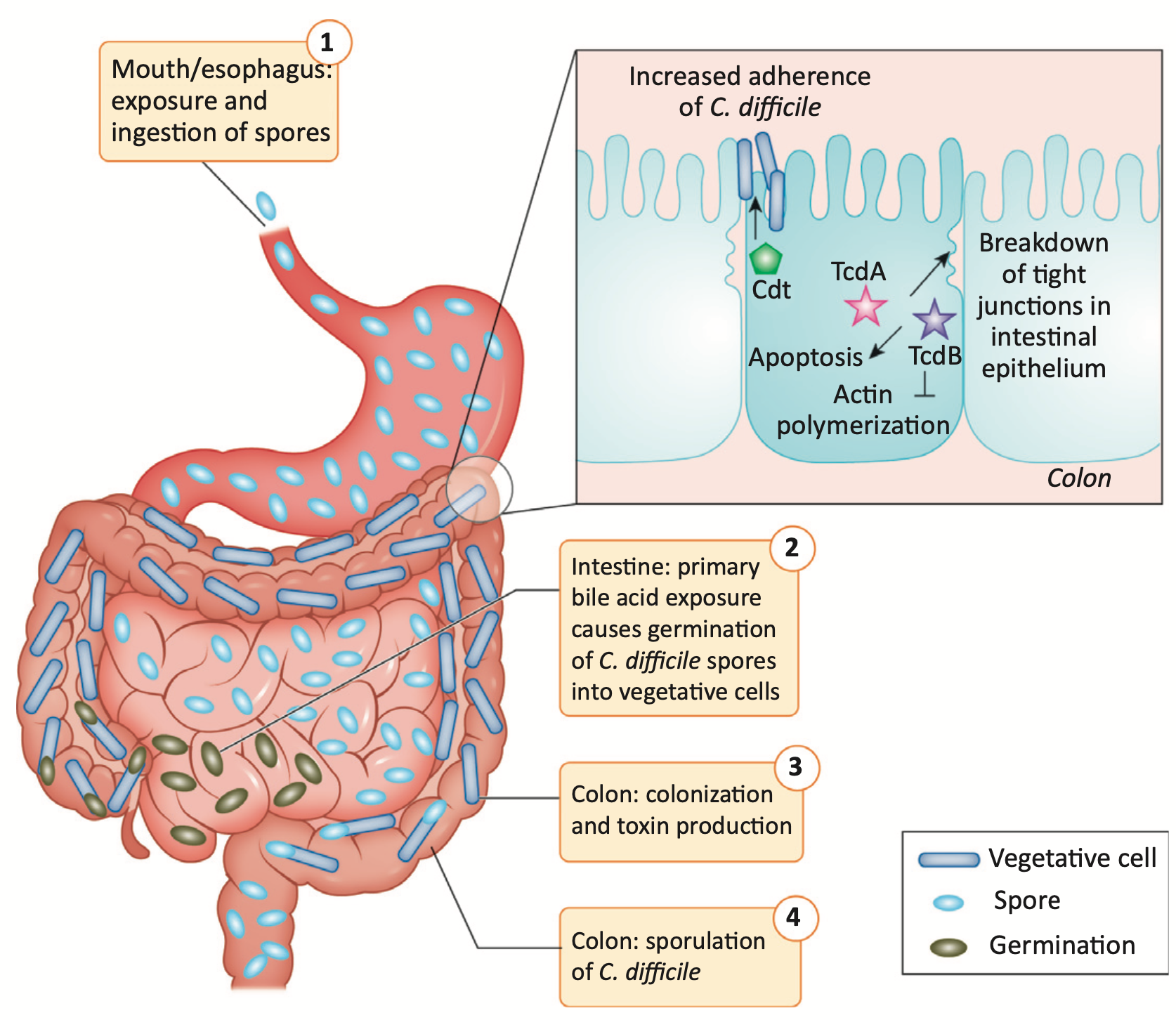
1. 艰难梭菌于 1935 年首次被报道,但直到 1978 年才发现其与抗生素相关腹泻和假膜性结肠炎有关。
2. 艰难梭菌有一个大约 4.3Mb 的环状染色体。
3. 艰难梭菌的孢子对热、氧和乙醇类消毒剂具有抗性,但可被 1:10 稀释的次氯酸钠(漂白剂)杀死。
4. CDI 可用的动物模型包括仓鼠、小鼠、幼兔、小猪、草原土拨鼠、小马驹、鹌鹑,以及大鼠。
5. 艰难梭菌毒素的作用已在大鼠、小鼠、仓鼠、兔、豚鼠、小恒河猴和斑马鱼胚胎中被表征。
6. 艰难梭菌产生的两种主要毒素是 TcdA 和 Tcd,它们是可抑制 Rho、Rac 和 Cdc42 的葡糖基转移酶。在核糖核酸分型编号为 027 的菌株中发现了第三种毒素 Cdt。
1. 老年人、医疗机构人员以及接受过抗生素治疗的人最容易患 CDI。
2. 最可能导致 CDI 的抗生素包括克林霉素、氟喹诺酮、头孢菌素,以及单环内酰胺类和碳青霉烯类药物。抗生素数量越多、累积剂量越高、暴露时间越长,CDI 风险越大。
3. 据估计,在初次感染的前 30 天内,CDI 的复发率为 13.5%,死亡率为 1.3%。

CDI 通常采用抗生素治疗,然而多达 20% 的 CDI 患者会再次患病。近年来,CDI 已经成为活菌制剂的一个重要治疗目标,目前已有多家企业进入了 2/3 期阶段。
1. 2022 年,辉凌制药(Ferring Pharmaceuticals)在 2022 年美国消化疾病周上公布了治疗复发性 CDI(rCDI)的候选药物RBX2660的3期临床阳性结果,目前该公司已经提交了 RBX2660 的生物制品许可申请(BLA);
2. 2021 年,Seres Therapeutics 公司预防 rCDI 的候选药物 SER-109 的 3 期临床试验获得阳性结果,并于2022年6月7日公布了 SER-109 补充试验ECOSPOR IV的阳性结果。目前,该公司已经开始向FDA滚动提交BLA 申请,预计于2022年年中完成提交;
3. 2021 年,Finch Therapeutics 公司预防 rCDI 的候选药物 CP101 的 2 期临床试验获得阳性结果,并正在开展该药物的 3 期临床试验;
4. 2021年,Vedanta Bioscience 预防 rCDI 的候选药物 VE303 的 2 期临床试验获得阳性结果,预计将于 2022 年进行 3 期试验;
5. 2022 年,Destiny Pharma 预防 rCDI 的候选药物 NTCD-M3 的 2 期临床试验获得阳性结果,正在准备3期临床试验。
参考文献:
(滑动查看全部)
1. Lessa, F.C. et al. (2015) Burden of Clostridium difficile infection in the United States. N. Engl. J. Med. 372, 825–834
2. Dubberke, E.R. and Olsen, M.A. (2012) Burden of Clostridium difficile on the healthcare system. Clin. Infect. Dis. 55, S88–S92
3. Raibaud, P. et al. (1974) Sodium taurocholate, a germination factor for anaerobic bacterial-spores in vitro and in vivo. Ann. Microbiol. B125, 381–391
4. Voth, D.E. and Ballard, J.D. (2005) Clostridium difficile toxins: mechanism of action and role in disease. Clin. Microbiol. Rev. 18, 247–263
5. Hall, I.C. and O’Toole, E. (1935) Intestinal flora in new-born infants – with a description of a new pathogenic anaerobe, Bacillus difficilis. Am. J. Dis. Children 49, 390–402
6. Bartlett, J.G. et al. (1978) Role of Clostridium difficile in antibiotic-associated pseudomembranous colitis. Gastroenterology 75, 778–782
7. Best, E.L. et al. (2012) Models for the study of Clostridium difficile infection. Gut Microbes 3, 145–167
8. Oka, K. et al. (2018) Establishment of an endogenous Clostridium difficile rat infection model and evaluation of the effects of Clostridium butyricum MIYAIRI 588 probiotic strain. Front. Microbiol. 9, 1264
9. Hutton, M.L. et al. (2014) Small animal models for the study of Clostridium difficile disease pathogenesis. FEMS Microbiol. Lett. 352, 140–149
10. Abt, M.C. et al. (2016) Clostridium difficile colitis: pathogenesis and host defence. Nat. Rev. Microbiol. 14, 609–620
11. https://www.cell.com/trends/microbiology/fulltext/S0966-842X(18)30200-2
原文链接:
https://doi.org/10.1016/j.tim.2018.09.004
作者 | Brindar K. Sandhu和Shonna M. McBride
编译 | wx
审校 | 617
编辑 | 豫小鱼


