
图片来源:AntoineDoré
1 月 29 日,Nature 发表的新一期 Nature Outlook 聚焦肠道微生物,该期报道由达能公司赞助,共含 12 篇文章。内容主要涉及健康微生物组、疾病、药物研发、微生物组工程改造、饮食等方面,并选取了一些肠道微生物领域的重要研究进行了报道。
前几天,我们的公众号《热心肠研究院》对这期 Nature Outlook 各篇文章做了简短的报道:Nature Outlook 专题:肠道菌群研究的现在和未来 | 热心肠日报。
《肠道产业》将对本期 Nature Outlook 的全部内容进行编译,并于今起 3 天陆续发布。其中,达能公司百年历史之前已经在《肠道产业》进行过报道:巨头大手笔:创立 100 年后,达能 all in 肠道和菌群!
今天,我们发布以下 3 部分内容的编译:人肠道微生物组研究概况、肠道微生物组的重点研究以及寻找健康微生物组。
人肠道微生物组研究概况
我们并不孤单,每个人体内生活着数万亿的微生物,包括细菌、真菌、病毒和其它属于微生物的生命形式。各种器官都有不同的微生物,但是在生物医学研究中最受关注的是肠道微生物。
为了更好地掌握肠道微生物在健康和疾病中扮演的角色,来自全球的研究人员正在研究什么微生物构成了“健康良好”的肠道微生物组。毕竟,肠道中有数百种不同的细菌,有些是致病的,有些是有益的。
计算生物学家 Eran Segal 认为,收集丰富的微生物组数据能够对志愿者进行深入的表型分析从而改变药物的发现方法。而关于某些能促进健康的益生菌的研究提供了一些新的生物学见解,这些见解或能够帮助药物开发。
现在认为一些疾病会受到肠道微生物组的影响,这些疾病包括癌症、自身免疫疾病(例如多发性硬化症)和自闭症谱系障碍。
另外,肠道微生物组还与某些药物(包括某些心理健康疗法)具有强烈的相互作用,并能够影响其效果。
越来越多的证据表明肠道微生物组对健康具有重要意义,合成生物学家正在寻找对微生物组进行工程改造的方法(包括个体物种层面和生态系统层面)以阻止疾病的发展。
公众对肠道微生物组会被如何影响的兴趣日益浓厚,主要体现在个人的饮食选择。微生物学家 Peter Turnbaugh 对这一问题的理解是,不是简单地探索哪种食物对我们的健康有益,而是可以从肠道微生物与饮食之间的相互作用中获得哪些医学结论。
关于肠道微生物组的更多研究正在进行,远远超过了本期 Outlook 所涵盖的范围,但也正是因为如此才能让人更加充分感受到这个领域的广度。
肠道微生物组重点研究
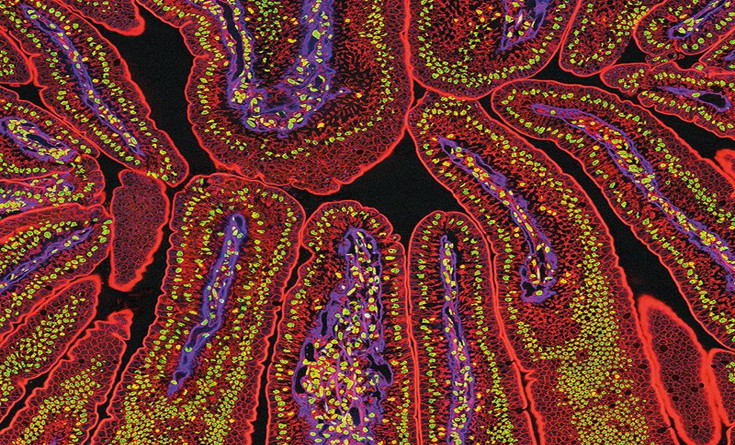
小肠的绒毛是肠道微生物的家,图片提供:NCMIR / SPL,Thomas Deerinck
一项对 1000 多名志愿者的研究为肠道微生物组与心理健康之间的关联提供了有力证据。
比利时鲁汶天主教大学的 Jeroen Raes 及其团队试图基于比利时佛兰德肠道菌群项目的参与者数据,寻找微生物组与抑郁和生活质量之间的关联。在这个队列中,研究小组发现两种细菌与参与者自己报告的高生活质量相关,而另一种细菌在低生活质量的人群中居多。
随后的一项分析将人群分为 4 类微生物群类型中的一种,结果发现抑郁症患者通常属于一种总体细菌丰度较低的类型。
基于已发表的肠道细菌代谢途径的遗传特征,研究小组还发现了约 50 种肠道微生物产生神经活性代谢物的途径。在这些途径中,研究人员发现了生活质量的提高与能产生神经递质多巴胺代谢产物的细菌之间存在联系。
这项工作为未来的研究建立了基础。未来,可以探究微生物组是否会影响心理健康,如果可以,那么可以进一步探究是否是通过改变多巴胺信号传导进行的。
本节参考文献:Nature Microbiol. 4, 623–632 (2019)
一项关于粪菌移植(FMT)治疗溃疡性结肠炎的临床试验的后续分析可能已经确定了有助于治疗这种炎症性肠病的细菌。
在 2017 年的一项试验中,27%的溃疡性结肠炎患者在接受 FMT 治疗之后病情完全缓解——这是成功的,但是遗憾的是只有部分患者有这样的效果。
最近,澳大利亚悉尼新南威尔士大学的 Nadeem Kaakoush 和他的同事进行了详细的分析,这些分析将症状缓解与接受者治疗前后的肠道菌群特征,以及供体粪便的细菌组成联系起来。
处于缓解期的患者在 FMT 前后均具有更高的微生物组多样性。但治疗后,症状缓解与两种细菌的富集有关:霍氏真杆菌(Eubacterium hallii)和食葡糖罗斯拜瑞氏菌(Roseburia inulinivorans)。
这些微生物被认为可以促进短链脂肪酸(SFCAs)的产生和淀粉的分解,事实上,研究发现处于缓解期的人的内脏 SCFA 产量增加。
成功治疗的可能性还与供给者粪便的细菌含量有关。如果粪便中含有大量的拟杆菌属,那么缓解的可能性更大,而链球菌属则在未发生缓解的样本中更常见。
研究结果为溃疡性结肠炎治疗选择合适的 FMT 供给者和接受者提供了依据,也为内科医生使用特定的菌株增强溃疡性结肠炎的治疗效果或反馈提供了依据。
本节参考文献:Gastroenterology 156, 1440–1454 (2019)
一项临床试验的结果显示,每天服用一剂 Akk 菌或可治疗代谢综合征。代谢综合征是一种容易导致 2 型糖尿病和严重心血管疾病的疾病,其特征是肥胖、高血压,以及血糖、脂肪和胆固醇的水平升高。瘦的人肠道中富含 Akk 菌,而 Akk 菌的丰度会随着肥胖而下降。
在一项验证性研究中,比利时的研究人员给抵抗胰岛素和超重或肥胖的人提供了活的 Akk 菌、巴氏灭活的 Akk 菌或安慰剂,每天服用,为期 3 个月。
结果显示,活菌和巴氏灭活后的 Akk 菌都具有益处。巴氏灭菌的 Akk 菌尤其降低了循环中的胰岛素和总胆固醇的水平,并缓解了胰岛素抵抗。这些微生物还降低了白血球计数,这表明整体炎症减弱了。
目前尚不清楚为何死亡的细菌更有效,但是研究结果表明,细菌的代谢产物或细胞壁碎片可能具有治疗活性。
但是,比利时鲁汶天主教大学的 Patrice Cani 和他的团队指出,这项研究的规模很小,每组大约只有 10 个人,而且腹部脂肪和体重指数均未降低。
他们现在正在研究单个分子在小鼠中的作用,并计划在人体中进行巴氏灭活后的 Akk 菌的更大规模试验。
本节参考文献:Nature Med. 25, 1096–1103 (2019)
研究肠道微生物组与特定疾病之间的关系往往存在因果关系的问题:目前尚不清楚改变的微生物组是否会导致疾病,或者疾病是否会改变微生物组的组成。
但是荷兰格罗宁根大学的 Serena Sanna 和 Cisca Wijmenga 以及英国牛津大学的 Mark McCarthy 领导的研究团队使用一种称为孟德尔随机化的分析方法解决了这个问题,该研究表明微生物组可引起代谢功能障碍。
在该分析方法中,遗传变异被视作定义实验组的标准。研究人员还提出了一种引发代谢功能障碍的机制:微生物产生短链脂肪酸(SCFAs)的变化。
荷兰近 1000 人的代谢健康数据发现健康状况与某些细菌和细菌代谢途径的存在有关。最值得关注的是,肠道微生物产生的一种 SCFA——丁酸盐,在粪便中的含量越高,胰岛素反应越好。
这项研究还表明,参与者的基因一定程度能够预测人们肠道内丁酸盐的产生水平以及微生物群落结构。这一发现在另一个 4000 多人的数据集上得到了证实。
接下来是因果关系的检验。如果胰岛素敏感性的变化改变了微生物(而不是微生物组扰乱了胰岛素生理学),那么所有已知能够影响胰岛素敏感性的遗传因素应该也能预测出丁酸盐产量,但是事实上并不能。
这表明,与微生物组结构和胰岛素反应相关的基因会影响肠道微生物组,进而再破坏胰岛素信号。
该研究小组还发现,遗传变异会增加另一种细菌来源的 SCFA——丙酸盐在粪便中的含量,从而增加 2 型糖尿病的风险。这些发现为代谢疾病个性化治疗程度的增加铺平了道路。
本节参考文献:Nature Genet. 51, 600–605 (2019)

一个人的肠道菌群是在生命早期确定的,主要由他们所接触到的细菌以及这些细菌在肠道内繁殖情况决定。
英国 Wellcome Sanger 中心的 Trevor Lawley 和伦敦大学学院的 Nigel Field 主导的研究表明,剖腹产从根本上影响了新生儿的微生物组,以这种方式出生的婴儿往往是医院中机会主义细菌的宿主。
研究人员观察了 596 名刚出生不久的健康婴儿和 8~10 个月大的婴儿,发现在婴儿出生 4 天后,剖腹产婴儿的微生物组与顺产婴儿明显不同。尽管剖腹产婴儿的微生物组在出生后 3 周内与顺产婴儿越来越接近,但是在婴儿期仍然存在显著差异。
剖腹产婴儿的微生物组最显著的差异之一是拟杆菌属的丰度较低。在医院通过剖腹产出生的新生儿的微生物组中发现的细菌,在出生后的几个月里急剧下降,但是这些细菌的数量仍然比 8 个月左右的顺产婴儿略多。
作者将这种差异归因于剖腹产出生的婴儿在出生过程中接触母体微生物较少。
该研究还发现,当顺产的母亲在产前服用预防性抗生素,一种几乎所有剖腹产的妇女都会服用的抗生素,那么这些顺产婴儿的拟杆菌属丰度也会变得很低。
剖腹产和接触抗生素都与儿童过敏的发生有关。虽然这项研究并没有提供直接的证据证明改变的微生物组是这些事件和疾病之间的连接媒介,但它确实提出了一个问题:截然不同的初始肠道微生物组是否会产生长期的影响。
本节参考文献:Nature 574, 117–121 (2019)
法国科学家研究了严重肥胖患者的微生物组,以及减肥手术后微生物群落的变化。
巴黎索邦大学的 Karine Clément 和她的同事进行的这项研究表明,大多数严重肥胖患者的肠道微生物都很贫乏,而且手术后的体重减轻和代谢健康的改善并没有伴随着微生物多样性的完全恢复。
研究人员通过量化整体基因组多样性以及测量术前和术后血清中微生物组相关代谢物的水平来分析微生物群落。该试验 3/4 的参与者都属于低微生物基因丰富度组,相比之下,这一比例在中度肥胖人群中为 20~40%。
当研究人员寻找代谢物和微生物组结构之间的相关性时,他们发现 9 种代谢物受到微生物组变化的影响。
减肥手术,也就是胃束带或者旁路手术,使微生物的多样性增加了 25~40%,但平均水平仍然低于正常体重的人。在手术后的 1 年,也就是减肥效果最明显的时候,该结论仍然成立。有些人在术后 5 年依然多样性较低。
这项研究表明,在外科手术的同时,采取策略来改善与严重肥胖相关的肠道失调,或可进一步改善代谢功能。
本节参考文献:Gut 68, 70–82 (2019)

图片来源:AntoineDoré
寻找健康微生物组
健康的森林长什么样?一片看似兴旺、翠绿的野地,可能隐藏着污染、疾病或入侵性物种,但只有生态学家才能发现可能危及整个生态系统长期福祉的问题。
微生物研究人员正在努力研究同样的问题。破坏生活在人类肠道中的微生物群落,会提高许多疾病的患病风险并导致其恶化。因此,许多科学家已成为颇有建树的细菌博物学家,致力于厘清这些具有惊人多样性的共生群落。
在每个人的肠道中大约居住着有 500~1000 种细菌,同时还有无法估计确切数量的病毒、真菌和其他微生物等。
DNA 测序技术的飞速发展大大推动了对这些细菌的鉴定工作,使研究者们能够编写出针对人类肠道中物种的“野外指南”。
来自比利时根特生命科学研究所的生物信息学家 Jeroen Raes 说:“我们开始了解这些参与者是谁了,但仍有相当多的‘暗物质’。”
目前,这个“野外指南”在区分健康和非健康微生物组方面的用途有限。这其中的部分原因是健康人群的微生物组之间存在着潜在的巨大个体差异,这些差异的产生受到包括环境、遗传和生活方式在内的多种复杂因素的影响。
这意味着,在决定一个个体是相对健康还是具有较高的患病风险(如罹患糖尿病)时,相对细微的差异可能会发挥出不成比例的作用。理解这些差异在临床中的意义仍然是一个挑战,因为这些细菌之间,细菌和宿主之间,以及和周围的生存环境之间都在发生着广泛的相互作用。
一位来自德国图宾根的马普所发育生物学研究所的微生物生态学家 Ruth Ley 表示,“一个人的健康微生物组在另一种背景下可能就是不健康的—这是令人感到棘手的概念。”
像 Ley 这样的研究人员们正在致力于从现代化进程和进化历史中更好地理解与发挥人类肠道微生物群的力量。日渐浮现出来的结果提示我们,即使不存在一个健康的人类微生物组,我们的生活方式仍然有充足的机会干扰这些复杂的共生群落的正常功能。
为了理解这些生态系统的崩溃是如何导致疾病,研究人员们需要突破微生物领域的束缚,剖析这些物种是如何与他们的宿主互作的以及它们相互之间又是如何发生作用的。
母亲送给她孩子的第一份礼物是少量的健康微生物。它们有些是通过母乳喂养和皮肤接触传播的,还有不少微生物是在分娩过程中通过母婴传递的。这意味着,如果婴儿是通过剖腹产出生,那么它将错过一套非常珍贵的“微生物启动包”。
因为一般在童年早期会建立形成肠道菌群,并且在整个成年时期基本维持不变,由此产生的干扰可能会对健康造成严重的长期后果。
一名来自新泽西州新布朗斯维克的罗格斯大学微生物学家 Maria Gloria Dominguez-Bello 认为,“这些婴儿出生后,会有较高的肥胖风险,以及糖尿病、过敏和哮喘等现代疾病的患病风险。”
在一项小型的临床实验中,她的团队发现,用来自母亲产道内的液体擦拭剖腹产出生的婴儿,可以有效地降低婴儿微生物多样性的丧失1。一些大型的临床试验正在进行中,以评估长期的益处。
早期的环境暴露也会对儿童的微生物组产生强烈的影响。加州大学旧金山分校的微生物组研究员 Susan Lynch 一直在研究儿童时期的环境因素和后续出现的过敏和哮喘风险之间的关联。她的发现表明,新生儿的父母们不应该过于害怕灰尘或皮毛。
在完成对近 1200 名婴儿的跟踪调查后,Lynch 和她的同事们发现狗狗或许是婴儿们最好的朋友,因为和狗狗在一起可以有效避免呼吸系统方面的疾病2。Lynch 认为“区别呼吸系统方面疾病患病高风险和低风险的唯一因素就是是否养狗”。
Lynch 还说,“饲养狗狗(还有猫咪)在一定程度上可以提高抚养婴儿的房间内的细菌的多样性,并且降低房间内的真菌的多样性”。
这一发现与其他研究一致,共同表明相对于在都市环境中长大的儿童,在农村或在农场中长大的儿童体内可能会产生更加丰富的肠道微生物组,从而降低患有炎症性呼吸系统疾病的风险。
(本部分内容之前《肠道产业》进行过相关报道:要想宝宝身体好,家里不如养条狗?似乎比猫好点?)

家里养狗会增加孩子接触细菌的多样性 图片来源:RachaelPorter/Getty
在童年的某个时期,肠道微生物组的组成会停止改变,然而确切时间点在何时尚不知晓。2012 年开展的一项研究,调查了来自马拉维、委内瑞拉和美国的人群的肠道微生物,并发现一种异乎寻常的模式3。
这篇论文的作者之一 Dominguez-Bello 说:“在三岁的时候,婴儿和成年人的肠道菌群之间便没有差别了。” 但是,她解释道,也有证据表明跨越这个时间点后,微生物组仍然会发生变化。很明显在进入成年期以前,肠道菌群的生态系统就已经进入平衡状态。
来自以色列魏茨曼科学研究所的计算生物学家 Eran Segal 声称:“这个平衡状态非常稳定,我们看到它们会变化,但是即使过了很多年的时间,不同时间点的肠道菌群仍然表现出显出极高的相似度。”
微生物组在成年时期的一些变化是由环境和生活方式驱动的。在 2018 年,Segal 对生活在以色列的 1046 名不同种族的成年人进行调查,他发现了与种族无关的微生物组的差异4。“环境因素导致的变化占到微生物组差异性的 20~25%,” Segal 说。
药物是一个明显的干扰源,应对感染时服用的和饮食中无意吃下的抗生素可以深刻地影响微生物组,甚至在控制细菌方面没有明确作用的药物也会引起混乱。Raes 指出,一项欧洲微生物组研究发现糖尿病药物二甲双胍(metformin)会产生意想不到的干扰作用5。
饮食也是一个强大的外在影响因素,尽管产生这种影响的具体机制还不清楚。
一项 2018 年的研究发现:从泰国移居到美国的移民其肠道菌群经历了显著“西方化”过程,这个改变可能,至少一部分是由转变为美国饮食导致的6。

从泰国移居到美国的移民身上所观察到的肠道菌群改变还伴随着肥胖风险的增加。虽然这项研究并没有建立肠道菌群和肥胖之间的因果联系,但是该研究结果与一个逐渐流行的假说一致,即“城市化”,或者说是整个现代生活:现代化生活可能会对人类和其体内的微生物之间的亲密关系造成巨大破坏。
加州斯坦福大学的微生物学家 Justin Sonnenburg 表示:“我们本来假设一个健康的西方人的菌群是一个健康菌群。”但是,事实上他和其他研究者认为饮食、抗菌预防措施和个人卫生习惯三者综合导致肠道菌群丢失部分微生物,而这种损害可能会导致现代社会中的慢性疾病的患病风险的上升。
“西方饮食和丢失的肠道菌群二者可能导致了长潜在的炎症状态。”Sonnenburg 说道。
若干项研究已证实,城市人群与以传统农业和狩猎生活方式为主的人群的肠道菌群存在明显差异,而后者与我们早期祖先的微生物组更为相似。这种差异主要是细菌多样性的丧失,而细菌多样性的丧失似乎与西方饮食中纤维的缺少有关。
Sonnenburg 说:“生活在塔桑尼亚的哈扎人(Hadza)以狩猎采集为生,他们每天摄入 100~150g 膳食纤维,这个摄入量是一个普通美国人的 10 倍。”
因此,在非西方人群中,消化纤维的细菌,例如普氏菌属,其比例能占到肠道菌群的 60%,而这个占比在美国人群中却小得多。
Sonnenburg 的团队已经证明了这些变化是怎样在短短几代时间里在一个人群中变得根深蒂固的7。
小鼠在接受人类肠道菌群后分别喂食低纤维素食物和高纤维素食物,结果显示喂食低纤维食物的组会丢失掉部分种类的肠道细菌,而吃高纤维食物的小鼠的微生物种类并不改变。
而当低纤维素饮食的小鼠后代再次喂食高纤维素饮食时,丢失掉的这部分种类的肠道细菌会发生恢复。但是低纤维素饮食的小鼠传至四代之后,丢失的细菌就会永远丢失,无法恢复。
(本部分内容之前《肠道产业》进行过相关报道:12000字强文:工业化毁菌促慢病,菌群重建路在何方?)

一位来自位于伊利诺伊州埃文斯顿的西北大学的人类学家 Katherine Amato 一直在研究非人——灵长类动物,追踪人类生活方式与生理的改变,试图寻找到人类健康微生物组的进化源头。
Amato 说,一般情况下,灵长类物种之间微生物组组成的相似度和它们之间的进化关系密切相关。
但是,在 2019 年的一项对比分析中,Amato 发现人类微生物组的组成(尤其是来自非工业化社会的人们的微生物组)并没有如预期的那样,与我们的近亲,如类人猿、黑猩猩和倭黑猩猩保持高度的相似性8,反而和狒狒表现出惊人的相似度。
虽然狒狒与人类有较远亲缘关系,但是它们的生活方式和早期人类非常相似。Amato 说:“大部分的类人猿生活在热带雨林,以果实为食,但是我们倾向于认为我们的祖先是生活在开阔林地或者大草原上,并且像狒狒一样,为杂食性饮食。” 这说明饮食习惯和环境因素都在塑造人类微生物组方面发挥着重要作用。
Ley 认为微生物组为快速适应生活方式的变化提供了一种强大的应对机制——至少相对于正常的缓慢进化来说是这样的。事实上,她的团队找到了微生物组适应乳糖耐受性9和进化获得高淀粉饮食消化能力的证据——这种基因适应只在过去大约 1 万年的某些特定人群中出现过。
但是,如果变化发生得太快,正如过去几个世纪的快速工业化所展示得那样,宿主和微生物组之间的健康的相互关系就会遭到破坏,因为那些在进化中留下的,宿主所依赖的微生物物种会消失。
Dominguez-Bello 说:“抗生素和卫生设施体系在控制感染性疾病中发挥着重要作用,但是,它们也会带来意想不到的副作用,损害我们我们体内有益的微生物。”
虽然研究者们已经对人类肠道微生物组有了更好的了解,但是他们仍然还在努力确定哪些成分是对于我们的健康是至关重要的。一个问题是,目前的数据不足,以至于研究人员无法得出微生物组和健康或疾病之间可靠的联系。
Segal 将其与人类基因组类比,认为只有出现足够可用的高质量序列时,数据才能开始提供临床意义。“到目前为止,大约有 3 千万人完成了全基因组测序,而对于微生物组,在公共平台上仅有一万例公开样本。”他说。
这一问题因地理差异对微生物组的影响而变得更加复杂。除了少数针对选定人群的研究,比如非洲的哈扎人,大部分的数据来自于美国、欧洲和中国。
Raes 说:“我们对非洲、东南亚和南美洲的人类微生物组的变化了解太少,这一信息缺口对理解前面提到在工业化世界里的‘微生物丢失’问题的严重程度尤为重要。”
一个更大的、更全球化的数据集将为整体了解一个健康个体的正常微生物组可能是怎样的提供更好的起点,并将更容易识别与疾病相关的扰动。
但是,研究人员还需要突破仅仅根据健康个体或某一特定时间点上患有某种疾病的人体内是否存在某种特定微生物的局限性,应该要更全面地进行相关性的研究。
目前涌现出很多长期的纵向研究,该类研究在长时间内跟踪监测多个个体的微生物组。
比如,加拿大健康婴儿纵向发展研究项目(Canadian Healthy Infant Longitudinal Development Study)在 5 年内对 3400 多名儿童进行了跟踪调查,试图找到影响哮喘和过敏等疾病的因素。
“如果我们能发现某个微生物组的变化先于临床上变化,那么我们也许能够确定它们之间的因果关系,”Segal 说。
这样的模式将使得临床医师对诊断结果或者医疗干预的潜在价值更有信心,并且对于了解微生物组如何影响慢性疾病(比如糖尿病)的发生具有无法估量的价值。

同时,研究人员们也在努力把细菌的普查工作做得更加精细。早期的微生物组研究仅仅局限在实验室可以培养的肠道微生物物种。但是,测序成本的快速下降,使得我们能够从粪便微生物中提取到更为详细的 DNA 信息。
现在研究人员们可以将微生物的鉴定超越物种水平细化到菌株水平,甚至是菌株水平不同的基因组变体。比如,Sonnenburg 正在利用该技术寻找可能影响不同肠道微生物的代谢活性或饮食偏好性的突变。
但是,有些微生物依然是“漏网之鱼”。微生物组分析的标准方法有助于细菌的鉴定,但是在识别其他常见的肠道微生物的效果并不好。
Lynch 说:“在我们的数据中很少能看到真菌的信息,但是我知道它肯定是存在的,并且我们知道它们有助于微生物和宿主之间整体的相互作用中。”
新的微生物分析技术为我们提供了解决方法。比如说,收集和分析 RNA,而非 DNA,可以让研究人员们能够获取基因表达的变化,从而揭示出看似正常的肠道物种的功能障碍。“一个表面看似正常的微生物组可能正在做着不健康的事情,”Ley 说。
其他的研究人员开始转向代谢相学技术,对微生物样本中各种各样的生物分子进行综合性的化学分析。这有助于研究人员了解微生物之间和微生物与宿主细胞之间是如何进行交流的。
“这些分子是终产物。”Lynch 说,“我们要寻找的健康微生物组的生物标记物就在它们中间。” 利用该技术,她的团队已经取得了一些重要的进展,其中包括找到一种名为 12,13-diHOME 的微生物脂类分子,该类脂分子似乎是哮喘高危婴儿炎症的一个驱动因素10。
这样的数据可能为我们提供了至今为止最好的关于我们内部生态系统繁荣程度的解读——从根本上讲,就是要同时关注土壤、水源和森林中树木的叶子,而非仅仅数一下树木的数量。
“不存在‘绝对健康’的微生物组,就像不存在完美的基因组一样。”Segal 说,“健康的标准应该是多重的。”这些关于微生物活动的研究可能是验证微生物组功能和功能障碍假说的最快途径,并将加速向临床试验的转化。
“虽然通过观察手段研究微生物的时代还没结束,但是接下来我们真的应该尝试一下干预方法。”Raes 说,“你只有好好踢一脚,看看会发生什么,才能理解一个系统。”
参考文献
(滑动下方文字查看)
1. Dominguez-Bello, M. G. et al. Nature Med. 22, 250–253 (2016).
2. Havstad, S. et al. J. Allergy Clin. Immunol. 128, 880–885(2011).
3. Yatsunenko, T. et al. Nature 486, 222–227 (2012).
4. Rothschild, D. et al. Nature 555, 210–215 (2018).
5. Forslund, K. et al. Nature 528, 262–266 (2015).
6. Vangay, P. et al. Cell 175, 962–972 (2018).
7. Sonnenburg, E. D. et al. Nature 529, 212–215 (2016).
8. Amato, K. R. et al. Genome Biol. 20, 201 (2019).
9. Goodrich, J. K. et al. Cell Host Microbe 19, 731–743(2016).
10. Levan, S. R. et al. Nature Microbiol. 4, 1851–1861(2019).
第一部分:人肠道微生物组研究概况
原文链接:https://www.nature.com/articles/d41586-020-00194-2
作者|Herb Brody
编译|617
第二部分:肠道微生物组的重点研究
原文链接:https://www.nature.com/articles/d41586-020-00203-4
作者|Liam Drew
编译|617
第三部分:寻找健康微生物组
原文链接:https://www.nature.com/articles/d41586-020-00193-3
作者|Michael Eisenstein
编译|朱国利
审校 | 617


