体外诊断(IVD)是指在人体之外,通过对人体样本(血液、体液、组织等)进行检测而获取临床诊断信息,进而判断疾病或机体功能的产品和服务。IVD产业是随着现代检验医学的发展而产生的,而产业的发展反过来又极大地推动了检验医学的发展。IVD作为无创、高灵敏、低成本、操作便捷的临床检测手段,在胃肠道领域应用繁多,主要可以分为胃肠癌早筛、消化系统肿瘤伴随诊断、病原菌检测。
今天,我们特别关注IVD在胃肠道领域的应用。希望本文能够为相关的产业人士和诸位读者带来一些启发和帮助。
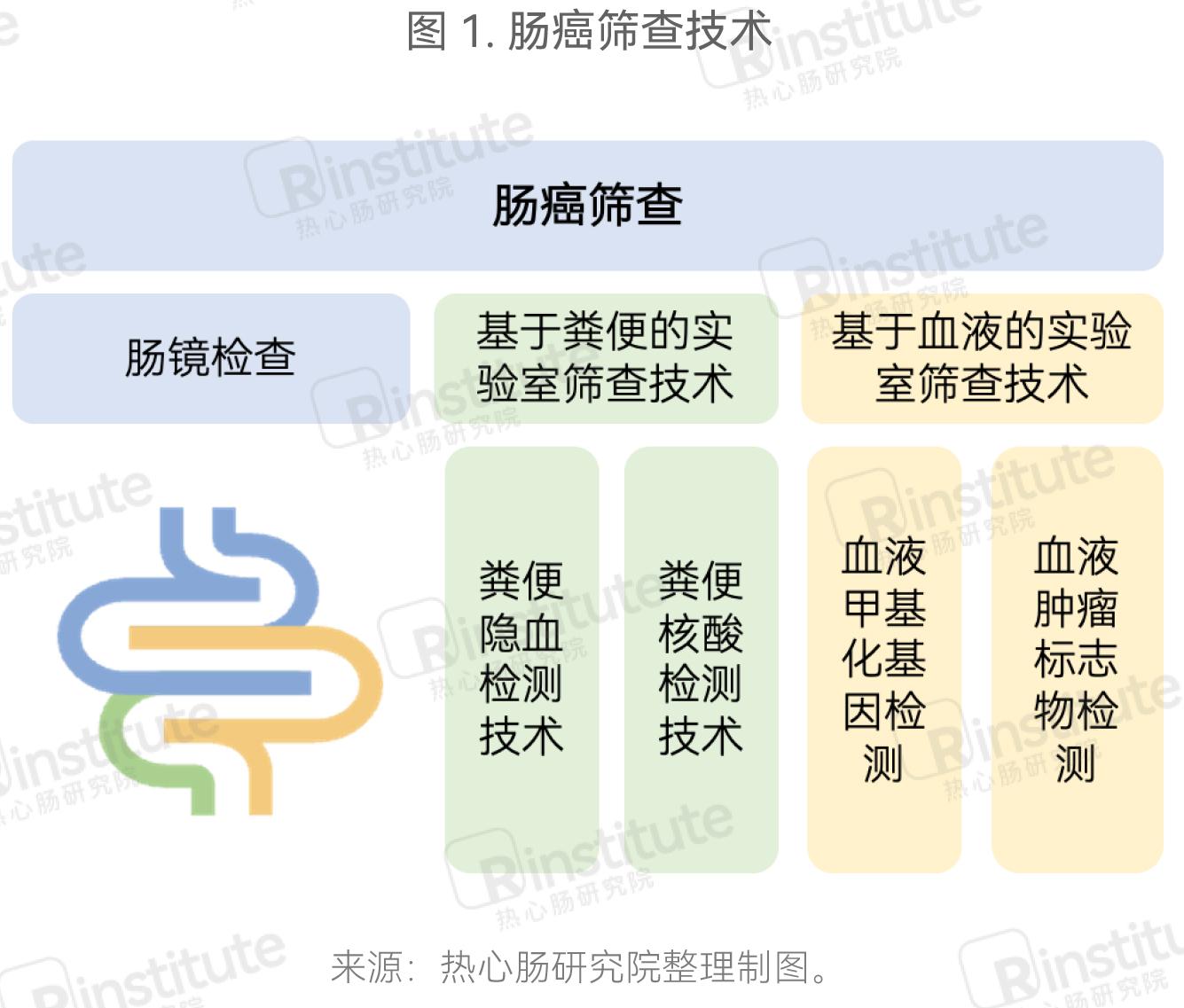
肠癌早筛指在无癌症病史或癌前病变历史的无症状人群中检测早期结直肠癌和癌前病变的过程。根据2019年发布的《中国早期结直肠癌筛查流程专家共识意见》和2021年发布的《早期结直肠癌和癌前病变实验诊断技术中国专家共识》,我们可以将肠癌筛查技术分为三大类(图1):肠镜检查、基于粪便的实验室筛查技术、基于血液的实验室筛查技术。
其中基于粪便的实验室筛查技术可以进一步分为粪便隐血检测技术和粪便核酸检测技术。基于血液的实验室筛查技术主要为血液甲基化基因检测和血液肿瘤标志物检测,另有一些初创公司正在探究通过检测血液中的痕量微生物DNA来筛查癌症。
1. 粪便隐血检测技术
粪便中出现潜血是结直肠癌(colorectal cancer, CRC)的征兆之一,在消化道恶性肿瘤患者中,早期约20%患者可出现潜血试验阳性,晚期患者的潜血阳性率可达到90%以上。粪便隐血试验(fecal occult blood tests,FOBT)通过检查粪便中隐匿的红细胞、血红蛋白或转铁蛋白而确定有无消化道出血,是目前应用最为广泛、评价最多的CRC筛查方法,具有无创、价廉、检测便捷等优点。临床常用的粪便隐血试验按照方法主要有化学法和免疫法。
• 化学法粪便隐血试验
原理:通过检测粪便中的亚铁血红素来确定消化系统有无出血。亚铁血红素是含铁血红蛋白的主要成分,具有过氧化物酶活性,可催化过氧化氢生成新生态氧,使试剂的色原底物产生有色化合物,显色者即为粪潜血试验阳性,根据显色颜色深浅与显色时间可大致判断粪便中血红蛋白含量。
细分类型:据试剂底物色原的不同,化学法粪便隐血试验分为还原酚酞法、联苯胺法、邻甲苯胺法、无色孔雀绿法、愈创木酯法、匹拉米洞法等。其中愈创木酯法(guaiac fecal-occult blood test,gFOBT)为比较常用的检测方法,被很多肠癌筛查指南所推荐。
特点:该检测方法会受日常饮食中许多因素的影响(如红肉、维生素C等),容易出现假阴性和假阳性结果;依从性低;送检时间需在2小时内。
• 免疫法粪便隐血试验(FIT)
原理:FIT利用单克隆或多克隆抗体针对粪便中人血红蛋白抗原等血液成分检测肠道的出血情况。
细分类型:可以分为定性FIT和定量FIT。前者多采用免疫层析技术为基础的胶体金试纸法,后者使用以免疫乳胶凝集反应和免疫比浊法检测为基础的自动定量检测仪进行检测。
特点:该技术可检测出粪便中较低浓度的球蛋白,不受饮食、药物和粪便中其他成分的干扰;对CRC的检测敏感度和特异度均高于gFOBT。
2. 粪便核酸检测
粪便核酸检测是目前诊断结直肠肿瘤的最前沿技术,其生物学基础是细胞脱落现象的持续存在。正常成人每天都会有上皮细胞脱落至肠腔,并随粪便排出体外,而CRC肿瘤细胞由于快速分裂和对基底膜黏附性降低等因素,会持续不断地脱落到肠腔中,从而可以从粪便中提纯和分析肠道肿瘤脱落细胞的基因成分并以此判断肠道肿瘤的发生情况。
• 粪便DNA检测
原理:粪便DNA检测主要测定肠道脱落细胞中某些特定DNA位点突变和表观遗传生物标志物(如KRAS突变、NDRG4、BMP3和SDC2基因甲基化)的异常改变。
细分类型:根据检测靶点数量,可以分为单靶点和多靶点。
特点:具有无创、便捷、精准等优点,可以与FIT联合检测,且无需特殊设备、无需限制饮食等。但是由于肿瘤细胞DNA极其痕量,且需要实现定量检测,因此对粪便处理方法、核酸提取方法、靶基因捕获技术以及实验室条件和操作人员有较高的要求。
• 粪便微小RNA检测
原理:miRNA 是一种非编码调控小RNA,通过结合3′-非翻译区或招募RNA诱导沉默复合物来调节mRNA的表达。miRNA在细胞增殖、分化、凋亡等过程中起到重要的调控作用,与人类癌症发生发展也密切相关,多种癌症类型肿瘤的生长和转移均发现miRNA的参与。CRC具有独特的miRNA谱。检测粪便中具有CRC独特性的miRNA(如miRNA-92a),可用于筛查CRC。
特点:具有无创、便捷等特点,但具有与粪便DNA检测同样的问题,同时miRNA在检测过程还存在一定的降解风险。
3. 血液甲基化基因检测
原理:Septin9基因属于抑癌基因,编码GTP-结合蛋白,与染色体分离、DNA修复、迁移、凋亡等细胞功能有关。结肠癌组织Septin9启动子存在不同程度甲基化。因此,对外周血甲基化Septin9进行检测可对CRC的筛查和诊断提供一定的参考。
特点:具有取样方便,患者接受度高等优势,但其对早期CRC和晚期腺瘤的诊断灵敏性较低,单独使用在筛查癌前病变时价值有限。
4. 血液肿瘤标志物检测
原理:肿瘤标志物是肿瘤细胞自身产生或者宿主对肿瘤的刺激反应而产生的物质,是能够反映肿瘤发生、发展,或监测肿瘤对治疗反应的一类物质,它包括了蛋白质、酶和激素等。通过检测血液中CRC肿瘤标志物或可用于诊断CRC。
特点:具有取样方便,患者接受度高等优势,肿瘤标志物在诊断和监测预后上具有重要临床价值,但因为有限的特异度和敏感度,不建议将肿瘤标志物作为筛选工具。可以考虑将该方法与其他方法结合,以提高灵敏性和特异性。
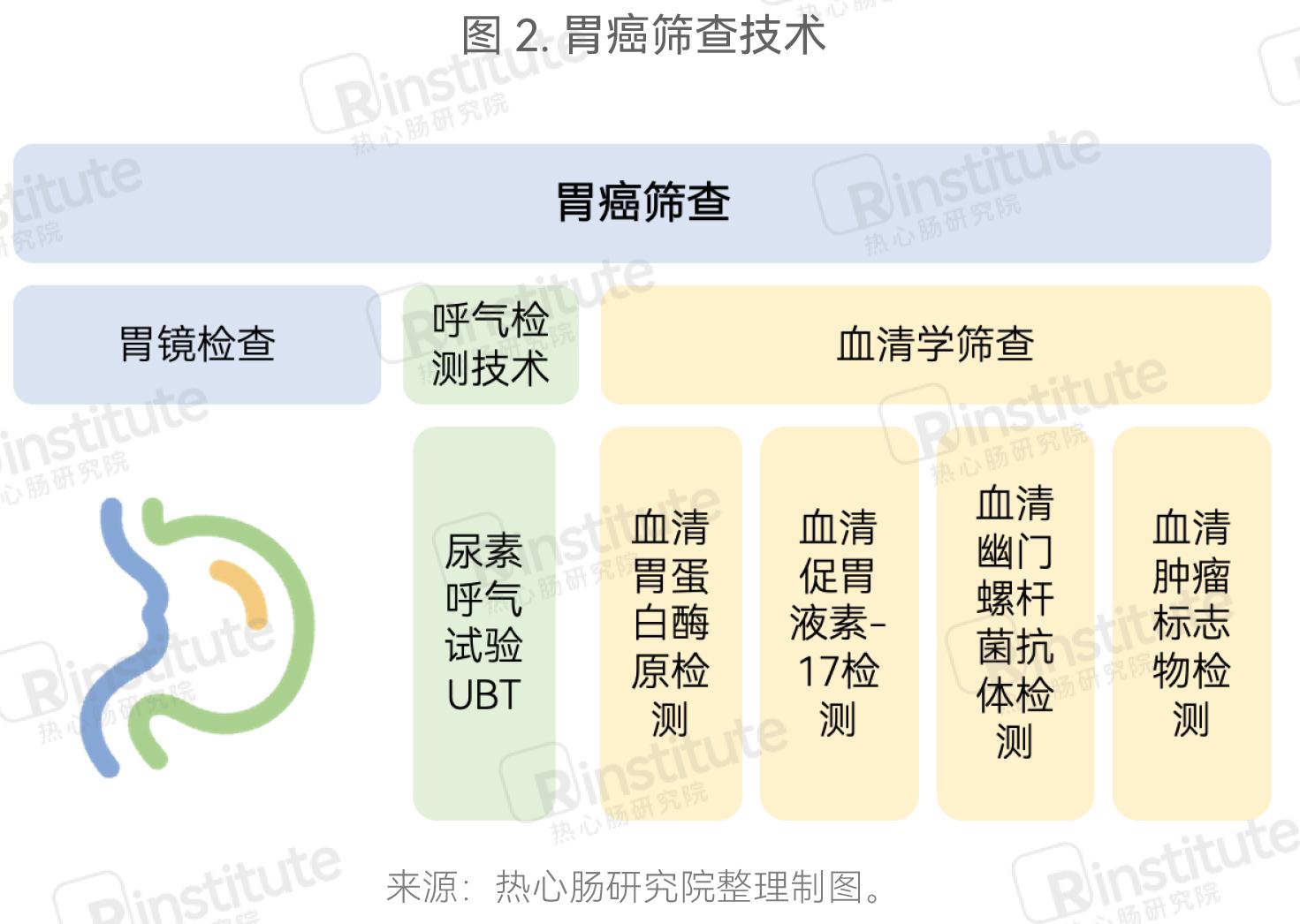
开展胃癌筛查可显著提高胃癌早期病变检出率,改善患者预后,大幅提高患者生存率。根据《中国早期胃癌筛查检验技术专家共识》(2023年)和《中国早期胃癌筛查流程专家共识意见》(草案,2017年,上海),胃癌筛查可分为胃镜检查、呼气检测技术、血清学筛查。其中,呼气检测技术主要是用于检测幽门螺杆菌的尿素呼气实验(UBT),血清学筛查则可进一步分为血清胃蛋白酶原(PG)检测、血清促胃液素-17(G-17)检测、血清幽门螺杆菌(Hp)抗体检测和血清肿瘤标志物检测(图2)。
尽管胃镜检查是一种筛查胃癌的精确手段,但是由于其侵入性大、依从性低,难以用于大规模胃癌筛查。而体外诊断技术可以帮助医生筛选患有胃部疾病的人群,并通过与胃镜筛查相结合,实现精准预防。
肿瘤是一种基因疾病,其发生源于一系列基因变异的积累,进而导致细胞异常增殖。不同肿瘤患者的基因突变类型不同,并可能随病程进展发生变化,呈现出不稳定性。由于当前不同肿瘤药物针对的靶点不同,且某些基因突变会造成耐药性,因此确定患者关键基因的变异情况对肿瘤治疗具有重要意义。肿瘤伴随诊断正是诞生于这一背景下,并已成为肿瘤领域的重要诊断手段之一。
肿瘤伴随诊断是指对肿瘤患者的样本进行基因测序等分析确定药物受体作用位点,从而实现精准用药、降低成本的目标。换言之,肿瘤伴随诊断可以为精准医学提供必要的生物学信息,支持医生对患者进行个体化的诊断和治疗方案的制定,并提高治疗效果和生存率。
目前针对肿瘤伴随诊断的技术主要分为PCR、荧光原位杂交技术(FISH)、免疫组织化学技术(IHC)、测序技术(NGS)等类别,不同技术的优缺点不同(表1)。

目前肿瘤伴随诊断技术已经在胃肠道癌症上取得了较大的进展。胃癌的伴随诊断技术手段主要是以PCR或FISH为主的分子诊断和IHC的免疫诊断。对于胃癌标志物来说,HER2的检测金标准是IHC和FISH,微卫星高度不稳定(MSI-H)/错配修复缺陷(dMMR)检测基于PCR、NGS等手段,PD-L1检测基于IHC(图3)。
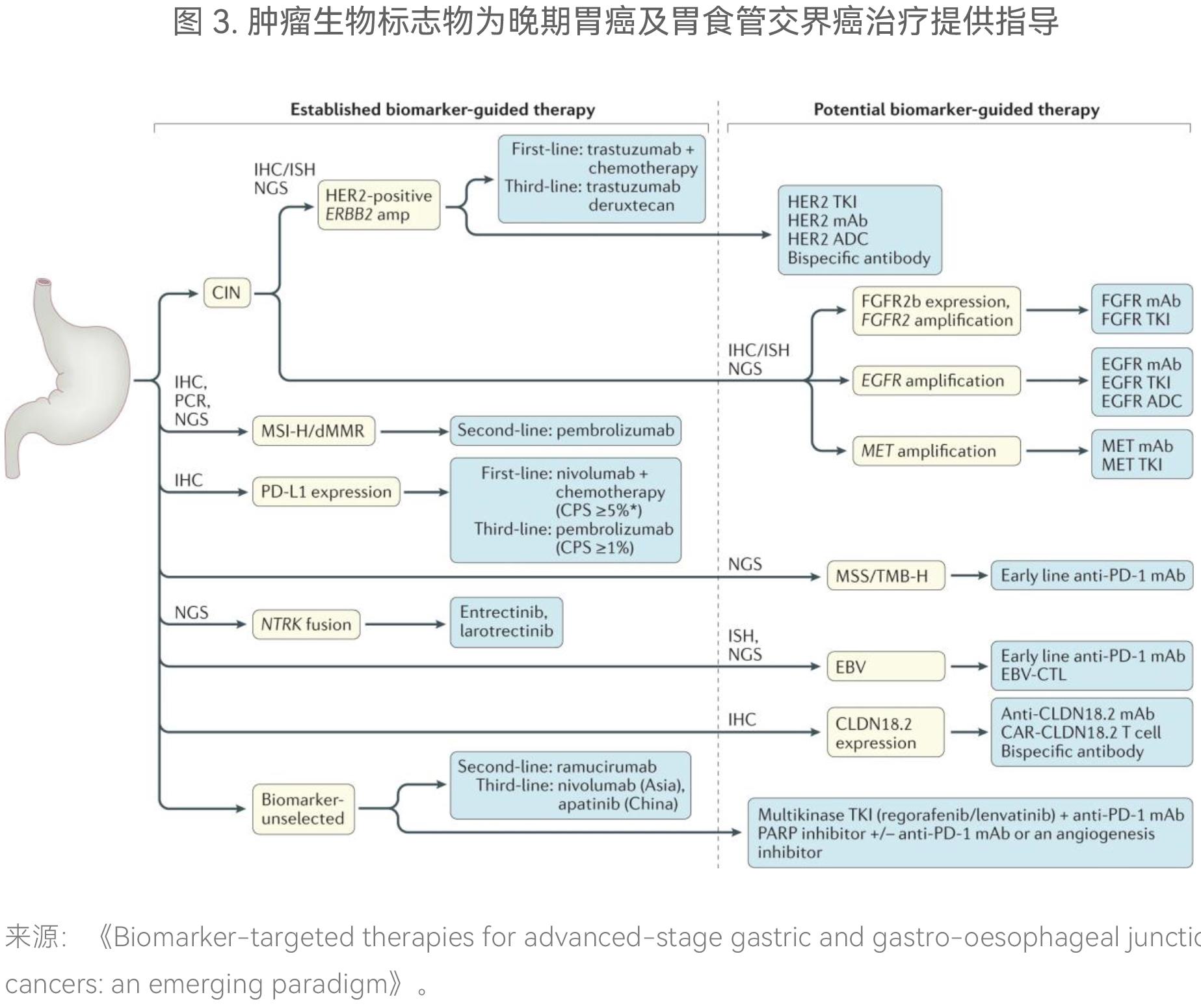
CRC是最常见的恶性肿瘤之一。CRC的发生发展是多基因、多步骤的复杂过程,个体差异较大(图4)。CRC患者通常过量表达表皮生长因子受体(EGFR)。EGFR信号转导下游有两条重要通路 RAS-RAF-MAPK和PI3K-AKT-mTOR,两条通路中的相关基因的突变会导致EGFR信号转导通路的持续激活,造成CRC患者不能从抗EGFR单克隆抗体治疗中获益。因此在靶向治疗前对KRAS、NRAS、BRAF、PIK3CA等基因状态进行联合检测非常有必要,可以避免患者因不合理用药而产生不良反应并减轻由此对患者家庭所造成的经济损失。
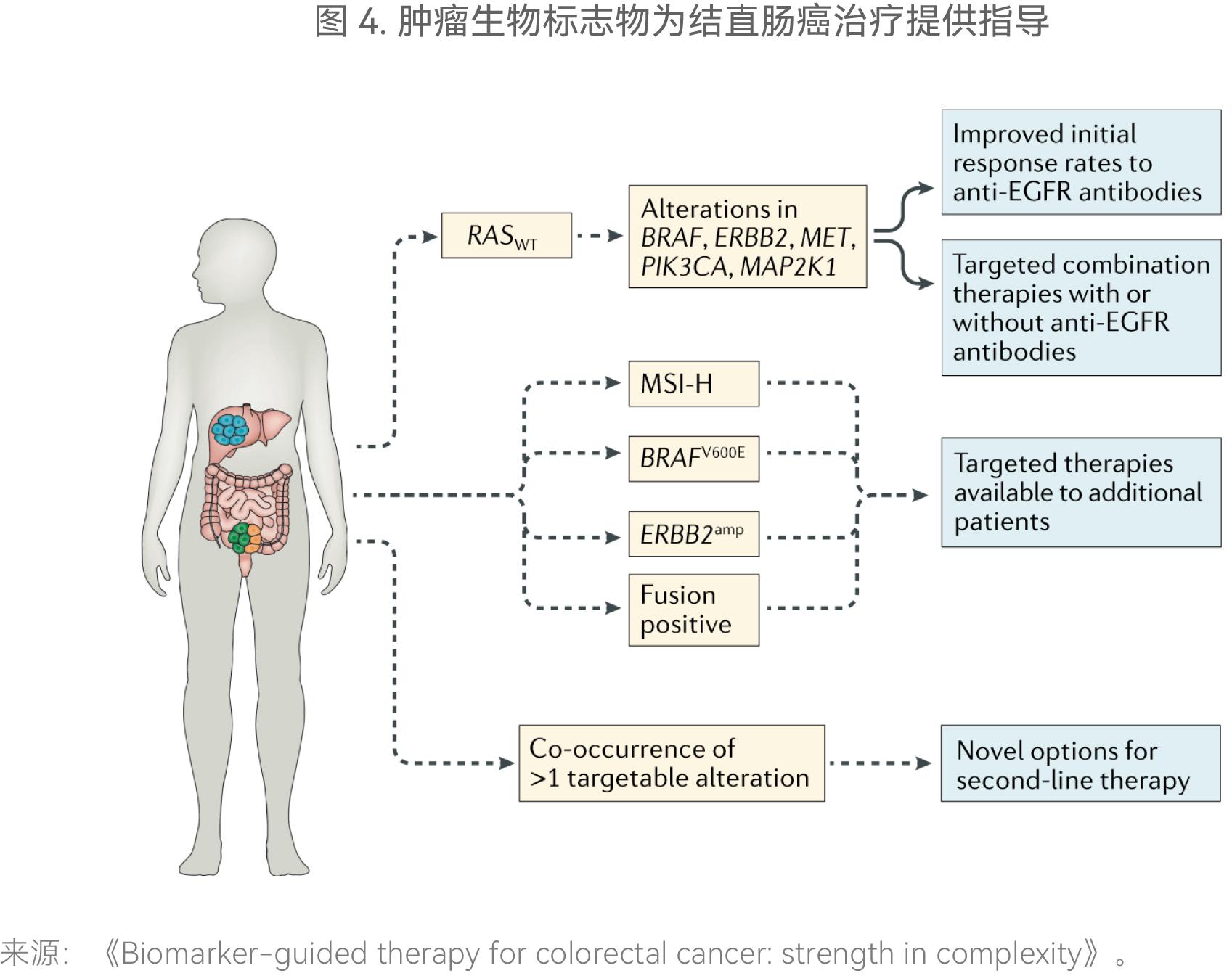
病菌感染主要是指的患者受到各种各样病原体感染引起的一系列病变。在机体免疫功能明显下降时,容易被各种病原体侵袭,并产生相关的症状,常见病原体包括细菌、病毒、真菌、寄生虫。
病原菌感染是大部分流行病的形成原因,其中消化道因其特殊功能,会遭受多种病原菌的感染。白色假丝酵母、单纯疱疹病毒(HSV)和巨细胞病毒(CMV)感染会造成食管炎症,而幽门螺旋杆菌感染参与到胃部炎症甚至胃癌的发生发展,胃肠炎以及腹泻则会由多种多样的食源性致病菌造成的,包括沙门菌、志贺菌、弯曲菌、致病性大肠杆菌、耶尔森菌属、弧菌属(如造成霍乱的霍乱弧菌)、气单胞菌、邻单胞菌属、迟钝爱德华菌、金黄色葡萄球菌、蜡样芽孢杆菌、产气荚膜梭菌,以及臭名昭著的艰难梭菌。
传统的病原微生物的检测方法查以染色、培养、生化鉴定等为主,但随着体外诊断技术的发展,快速高效准确的病原菌检测技术不断被开发出来,目前用于检测消化道病原菌感染的体外诊断技术包括质谱技术、宏基因组测序技术、16S rRNA检测技术等。


