近年来,肠菌移植(FMT)成为了一种备受关注的医学技术。肠菌移植通过将健康人粪便中的微生物群移植到患者的肠道中来恢复患者肠道菌群的平衡,以治疗一系列疾病。那么肠菌移植的流程究竟有哪些步骤呢?又需要注意什么?目前发展情况如何?
今天,我们共同关注肠菌移植。希望本文能够为相关的产业人士带来一些启发和帮助。
肠菌移植(Fecal Microbiota Transplantation,FMT)是一种将特定健康人粪便中的功能肠道菌群移植到患者肠道内,重塑失衡的肠道菌群,以实现肠道及肠道外疾病治疗的医疗技术。
在早期,FMT被直译成“粪菌移植”,但从美学、伦理学以及肠道菌群发挥最主要作用的角度考虑,越来越多人开始将FMT翻译为“肠道菌群移植”,简称“肠菌移植”。如《肠道菌群移植临床应用管理中国专家共识(2022版)》就将FMT译作“肠菌移植”。因此,在本文中我们也统一使用“肠菌移植”这一名词。
那么肠菌移植究竟是怎样的一个流程呢?实际上,肠菌移植目前尚无全球统一的操作规范,但一般将其操作流程分为如下几个环节:
1. 供体筛选:按照体检结果、粪便检测、血清学检测、精神健康检查、用药史检查以及家族遗传病调查结果等指标进行肠菌的供体筛查,以避免潜在的移植风险。
2. 肠菌制备:筛查后合格的志愿者/健康人提供新鲜粪便,交由专业实验室通过全自动设施进行注水、搅拌、过滤、离心、沉淀等步骤以获得纯净肠菌。该步骤暂时无公认的操作标准,且随着肠菌移植技术的发展,被不断调整与优化。
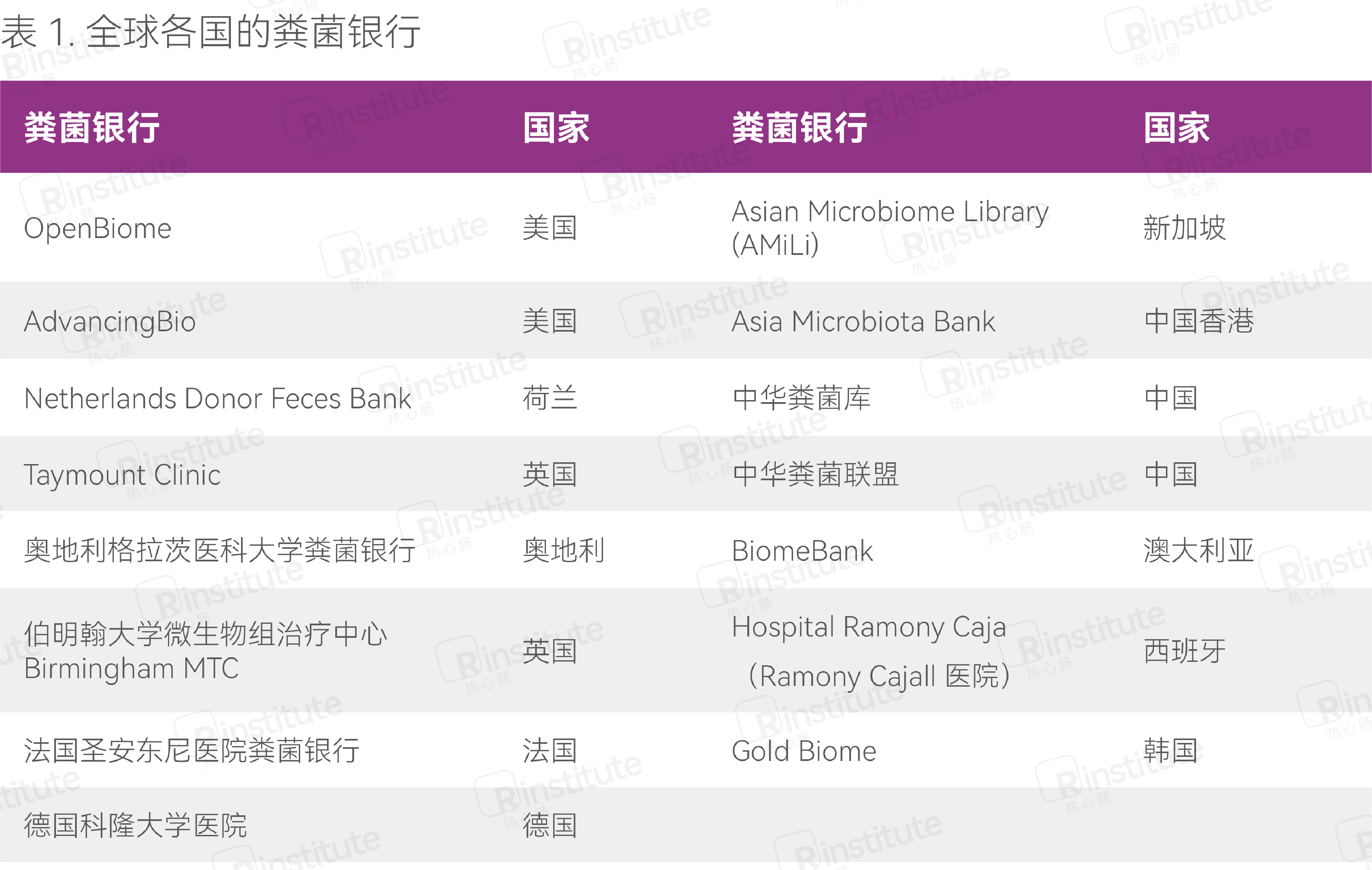
3. 供受体配型:制备好的纯净肠菌一般会保存在粪菌银行(表1),待有需要时被配对后提供给受体。
4. 移植:配对后的肠菌会以菌液或菌丸的形式低温运输到移植地点,医师将根据患者身体状况及其他因素来选择合适的移植方式。目前移植方式大体可分为侵入式和非侵入式两种。其中侵入式主要是以经内镜(包括胃镜、肠镜、经内镜肠道植管)和鼻肠管等方式进行移植,有创因此存在一定医疗风险。非侵入式包括经消化道和灌肠两种方式,经消化道一般使用的是粪菌胶囊即菌丸。
5. 随访:在经单次或多次肠菌移植后,如患者达到临床治愈或缓解的标准,那么在结束肠菌移植治疗后还要进行一段时间的随访工作。随访方式包括门诊复查、电话和网络问卷等模式。目前认为因为肠菌移植的系统较为复杂,不良反应和长期疗效等都很难准确预测,因此不低于8周的随访工作是必不可少的。
从肠菌移植的发展历程来看,我们可以根据肠菌移植的方式将其分为4个阶段,分别为“1.0时代:1700年前葛洪《肘后备急药方》”“2.0时代:标准化肠菌移植(传统手工)”“3.0时代:洗涤菌群移植”和“4.0时代:精准肠菌移植”。目前,洗涤菌群移植已经是一种较为成熟的肠菌移植技术,而精准肠菌移植仍处于起步阶段。
早在春秋战国时期,《素问》就记载:浊阴出下窍,宜其足以制阳亢,而心则火之主也,故独入之。造法于冬月取竹箩置缸上,棕皮铺满,加草纸数层,屎浇于上,汁淋在缸。新瓮盛贮,磁钵盖之,盐泥封固,埋地年深,自如清泉,闻无秽气。又法,腊月取淡竹刮去青皮,浸厕中取汁亦佳。
这是中药金汁的制备工艺,将健康人粪便使用竹箩、棕皮、草纸过滤,将汁水密封在缸内,埋于地下数年,其气味无臭时可用。又或者使用腊月的淡竹刮去竹皮,放于粪坑,浸取汁水。也有另外一种制备流程,在健康人粪便中加入井水、泉水、红土等发酵后取汁待用。
《本经逢原》则记载了另一味中药人中黄的制备工艺:甘咸寒无毒。造法,用大竹截段,两头留节,削去外皮,傍钻一孔,用甘草细末入满于中,以蕉扇柄削圆塞孔,冬至浸大粪池内,立春后取出,悬风处晾干,取用。又法如前制竹,不入甘草,但用蕉扇柄或杉木塞孔,浸粪池中,以取其汁与金汁无异,仅供一时取用,不能久藏。粪清亦解瘟热诸毒。又误食毒菌、枫树上菌、及过食银杏,胀闭欲死者,悉能解之。并解砒石、野葛、野芋等毒。即家芋三年不收,花开如莲者亦能杀人,急取灌吐,方可得生。
简而言之就是将甘草末放置于竹简内密封后在冬天浸在粪便中,到第二年春天取出,洗干净后于通风处阴干,之后从竹筒中取出的甘草末就是药物人中黄。
上面两味中药对粪便均进行了一定的处理,比如过滤或者加入甘草等进行萃取。
而魏晋时期葛洪所著的《肘后备急药方》记载了治疗腹痛和食物中毒的治疗方法——绞粪汁,饮数合至一二升,谓之黄龙汤,陈久者佳。这种就是直接使用未处理的粪便进行肠菌移植的先例,同时在李时珍的《本草纲目》中也记载了23个以人粪为组分的药方,包括直接使用和添加其他成分使用的。
同时在17世纪,意大利解剖学家和外科医生Acquapendente根据贝都因人治疗细菌性痢疾的秘方——食用骆驼粪便,提出了“转宿”的概念,即将健康动物咀嚼过的食物转移到生病的动物身上来治疗胃肠疾病。这种方法在兽医界风靡一时。
在近现代医学中,成功将肠菌移植应用于疾病治疗的有美国科罗拉多大学医学院的外科医生Eiseman等,他们用人粪清灌肠的方法治愈了3例对万古霉素和甲硝唑治疗无效的伪膜性肠炎患者。

1929年,人们首次发现了抗生素。随后抗生素大的量使用导致艰难梭菌感染,并引起相关疾病。在这一时代背景下,医生们又重新将目光转向肠菌移植。1981年美国Bowden团队通过经小肠置管输入粪液的方法,成功治愈16例伪膜性肠炎患者。1983年,肠菌移植也因成功复发性艰难梭菌感染被首次发表在《柳叶刀》杂志上。
随后,关于使用肠菌移植治疗艰难梭菌感染的临床病例开始大量出现。到了2013年,首个采用肠菌移植治疗复发性艰难梭菌相关性腹泻的临床对照研究宣称肠菌移植的疗效明显优于万古霉素。美国食品药物监督管理局(FDA)于2013年正式宣布可将人类粪便作为药物使用。同年肠菌移植被纳入治疗复发性艰难梭菌感染的临床指南,并入选了《时代》杂志当年的“十大医学突破”。这一里程碑事件也被认为是肠菌移植发展的重要转折点。

先前国际上的大多数临床研究,都是手工制备菌液,再给肠治疗,这种手工制备的过程对操作者是一种挑战。此外,受美学、对粪便中所含病原体的担忧以及尊严等因素影响,很多患者、医生、医学生和候选供体对肠菌移植持消极态度,不愿意去接受或开展肠菌移植。
我国自2014年起就开始研发基于智能粪菌分离设备和相关的新移植途径,这种途径被称为“洗涤菌群移植(WMT)”。因其基于自动化设备且存在多次洗涤过程,可去除未消化的食物残渣、真菌、寄生虫卵和部分促炎代谢产物,制备的菌液质量可控且具备良好安全性。
据相关数据显示,使用洗涤菌群移植的预后总不良反应事件发生率(包括发热、腹泻、腹痛、腹胀、恶心、呕吐等)在溃疡性结肠炎患者中从38.7%降低至12.3%;在克罗恩病患者中从21.7%降低至4.26%。
2022年10月,国家市场监督管理总局和国家标准化管理委员会联合发布公告,由张发明教授牵头,李潘等参与制定的国家标准GB/T41910-2022《洗涤粪菌质量控制和粪菌样本分级》即日获批执行。这是肠群移植领域发布的第一项国家技术标准,也是洗涤菌群移植的第一项国家技术标准。这对于粪菌移植的技术发展和规范实践具有重要意义。该标准明确规定了洗涤粪菌需要的实验室条件和技术要求,确立了洗涤菌群移植的剂量单位。更重要的是,该标准还根据实验室制备方法和安全性等级,明确了规定粪菌样本的安全性等级。

尽管肠菌移植在治疗艰难梭菌感染等疾病上展现出了良好的疗效。然而现有的肠菌移植方式存在一定的盲区,即无法知晓健康肠菌供体中是否含有可以对患者病症起效的关键细菌。众所周知,不同个体的肠道菌群存在较大的异质性,即便是健康人的肠道菌群也有肠型之分,因此实现精准化肠菌移植对于肠菌移植而言意义重大。
近年来有一些研究人员探索了精准化肠菌移植。如2022年,承葛生物联合全国16家三甲医院和双一流高校在Microbiology Spectrum杂志上发表了精准菌群移植供-受体配型算法文章,这也是全球首个精准菌群移植供-受体配型算法。
该研究以溃疡性结肠炎为例,结合荟萃分析与层次分析,从肠道微生物丰富度、菌群结构、有益菌、有害菌、有益通路和有害通路六大维度,构建精准供-受体配型模型。该模型在其他国家的测试数据集中整体准确率>70%;接受该模型所推荐供体的患者,其菌群移植后有效率高达100%。
除了采用肠菌移植的方式,也有许多企业从另一个角度实现“精准化”,即研发活菌药物(也被称为活体生物药,live biotherapeutic product,LBP),挖掘具有治疗作用的肠菌或肠菌组合。如近期获得FDA批准的首款口服活菌胶囊VOWST(候选药物名:SER-109)正是由厚壁菌门的芽孢组成的,用于预防艰难梭菌感染复发。
相信随着肠道菌群研究的日益深入,我们将会更深入地了解肠道菌群与不同疾病之间的因果关系,从而为推动精准化肠菌移植提供科学依据。同时也相信在研究人员的持续努力下,肠菌移植技术将会变得更加安全与有效,帮助我们治疗更多疾病。


