
各位老师,各位同学,各位专家,大家晚上好。今天,我非常荣幸参加本期的“肠·道”演讲。
我是来自清华大学医学院的研究员,名叫程功,也是清华大学医学院病毒传染病学实验室的负责人。
大家可能看到过我们的报道,我们发现肠道微生物可以调控蚊虫携带并且传播病毒的能力。今天就借这个机会,给大家来介绍一下关于虫媒病毒与肠道微生物之间的关系。
说起虫媒病毒,实际上的话,它有一个英文词叫Arbovirus,这个词实际上是由三个词组合而成的。
Arthropoda叫作节肢动物,Borne叫传播,Virus就是病毒,合在一块儿呢,就是节肢动物传播的病毒。
实际上WHO(世界卫生组织)对Arbovirus进行了比较准确的定义,它们是指一类由节肢动物携带,并且通过叮咬或者接触传播给易感的脊椎动物宿主。
或者是经由宿主的生殖系统,由母代传播给子代的病毒,使得这个病毒能够在自然界中,长期的生存、存在、传播、循环下去。
为什么我们要研究虫媒病毒,为什么我们要研究虫媒传染病,为什么说研究虫媒传染病非常重要?
我给大家先引入一个概念,什么是国际检疫传染病,这是在1851年在巴黎国际卫生大会上提出的一个概念。
那为了在最大程度上来避免烈性病毒,在不同国家之间的传播和流行,就规定有六种传染病为国际检疫传染病。
这六种传染病是在人类历史上,导致死亡人数最多、爆发流行最为广泛、最为烈性的六种传染病。
哪六种呢?我们可以看一下,分别是霍乱、鼠疫、黄热病、天花、斑疹伤寒和回归热。在这六大国际检疫传染病中,有四种都是由虫媒媒介携带并且传播给人的。
大家可以看到呢,实际上虫媒传染病曾经给人类的历史造成非常严重的公共卫生的灾难。但是随着医疗技术的不断发展,使得一些烈性传染病被人们有效控制了。
因此呢,现在的话,我们将国际检疫传染病由六种变成了三种,分别是霍乱、鼠疫和黄热病。
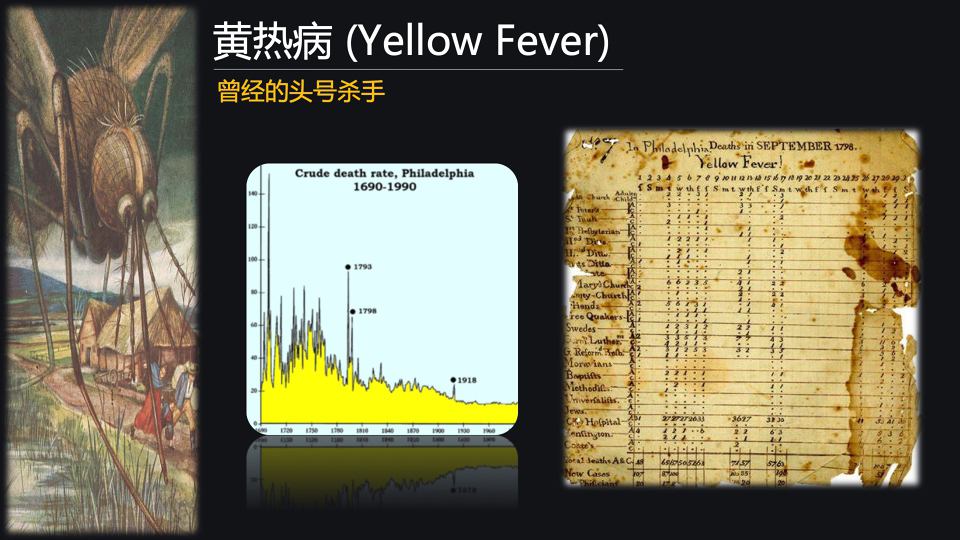
黄热病作为一个典型的蚊媒传播的病毒性传染病,仍然受到人们密切的关注。
黄热病病毒感染人以后,可以破坏人的肝脏,引起黄疸。病人通体发黄,因此它又被叫做Yellow Jackets(黄马甲),这是黄热病名字的来源。
实际上,黄热病毒感染人以后,最主要临床症状是重度的出血热,这导致非常高的死亡率。
大家可能不知道,在17到19世纪的时候,美国曾经是黄热病的一个主要疫区。大家说,美国也不是热带地区,怎么黄热病如此之严重?
实际上,一方面美国和非洲存在着黑奴贸易,随着奴隶船到达美国的,除了黑奴以外,还有带着黄热病的蚊子。
此外,美国南部的一些州和中美洲、南美洲都存在着相关的一些贸易联系。中美洲、南美洲是黄热病的主要疫区,它们的蚊子带着病毒就进入了美国。
黄热病毒从东向西,从南向北,在美国不同地区传播流行,就成了美国一个地方病。
大家可以看中间这张图,是美国当时的首都费城当时黄热病的疫情图。在1793年,据报道出现了非常严重的黄热病的疫情。
那这次疫情有多严重呢?有数万人都逃出了费城来躲避瘟疫,包括当时的总统乔治·华盛顿、汤姆斯·杰弗逊,这些美国的国父,都逃出了费城来躲避瘟疫。整个疫情下来以后,有十分之一的人口都死于黄热病的感染。
五年以后呢,再次爆发了黄热病的疫情,导致有数万人逃出了费城,7000多人死于黄热病的感染。
那后来,美国首都是从费城搬到了华盛顿,其实很大程度上也因为费城的疫情得不到有效的控制。
这是一个烈性传染病对人类政治、经济、生活产生重要影响的非常有代表性的案例。
黄热病毒感染宿主以后的话,感染人以后的话,死亡率在40%。大家可以想象,死亡率40%的这样的一个传染病,由蚊子携带,通过随机叮咬传播给人,必然会引起非常严重的公共卫生的灾难以及社会的恐慌。
那实际上的话,当一个烈性传染病突然出现的时候,我们需要做什么?
那我们是需要研发药物,我们是需要研发疫苗,但是呢,药物和疫苗的研发周期,实际上还是比较长的。
我们要在短时间之内控制传染病,首先我们还是希望有效的去发现它的传播途径,切断它的传播途径。

在黄热病的传播途径发现过程中,做出杰出贡献的有这两个人,一个叫做Carlos Finlay,一个叫做Walter Reed。
Carlos Finlay是古巴的一个内科医生,他通过长期观察就认为,黄热病是由蚊子传播的。在1881年,他提出了著名的黄热病由蚊虫传播的假说,我们叫做Mosquito Hypothesis(蚊虫假说)。
但是他只是一个内科医生,他没有足够的人力物力去验证他这样的一个假说。那这个假说,被另外一个叫Walter Reed的人验证。
他是美军驻古巴的医疗官,他当时主要的研究兴趣,就是发现黄热病的传播途径。当时美军在古巴,因为黄热病死亡的人数实在太多了,这是他的一个主要军事任务。
实际上,他通过长期观察认为,Mosquito Hypothesis(蚊虫假说),蚊虫传播的理论可能是正确的。
于是他就组织了志愿者进行相关的人体实验,就是将志愿者置入一个隔离的棚子里面,让他们与外界环境隔离,再放入疑似黄热病感染的蚊子,让蚊子咬这些人。
到最后,发现很多志愿者都出现了黄热病的症状,从而直接证明了黄热病实际上是由蚊子携带并且传播的。
因此,人们终于意识到,原来在自然界中的话,蚊虫是可以携带并且传播病毒的。这也是人类对于传染病认识的巨大的进步。

人们真正有效地去控制黄热病,还是要到了上个世纪30年代。有一个科学家,大家应该记住他的名字,叫Max Theiler。
这个人非常伟大,南非人,他是当时在美国洛克菲勒大学成立的实验室,是一个年轻的助理教授。他当时的主要研究兴趣,就是发现黄热病的疫苗,以及相关的治疗策略。
他首先先从在非洲拿来一个非常烈性的黄热病的毒株,叫Asibi Strain(Asibi株)。这个毒株非常烈性,感染老鼠,老鼠马上就死掉了。
他于是呢,先使用了当时世界上最为流行的减毒活疫苗的制备方法。利用这样的一个毒株,在鼠脑、在鸡胚中连续传代,传了50到100代,这个病毒仍然保持了非常强的感染活性。
那方法失败了,他于是就改变了自己的实验策略。
实际上,他接下来就使用了当时最先进的一个平台技术,继续传代病毒。什么呢?就是大家现在常用的体外的细胞培养技术。
又传了50到100代,病毒终于发生了突变,变成了一个减毒活疫苗株,叫做17-D。
17-D这个疫苗株是一个非常安全有效的减毒活疫苗株,它免疫或者感染人以后,可以诱导非常牢固的体液免疫和细胞免疫,但是完全不会出现任何的临床症状。
因此这个毒株马上得到推广,使人们终于掌握了一个有效控制黄热病的武器,使得黄热病的疫情得到非常有效的控制。
由于他做出的杰出贡献,于1951年获得诺贝尔生理医学奖。

那除了像是黄热病等一些老的烈性的传染病以外,一些新的蚊媒传染病也是不断的出现,来危害人们的健康。那最为典型的呢,实际上就是登革热。
到本世纪初,登革热已经成为世界上最为严重的虫媒传播的病毒性传染病了。
据统计,全世界有100多个国家存在登革病毒的感染流行,有25亿人生活在受登革病毒感染威胁的区域。据估计,每年有3.9亿人被登革病毒感染和重复感染,50到100万人入院治疗。
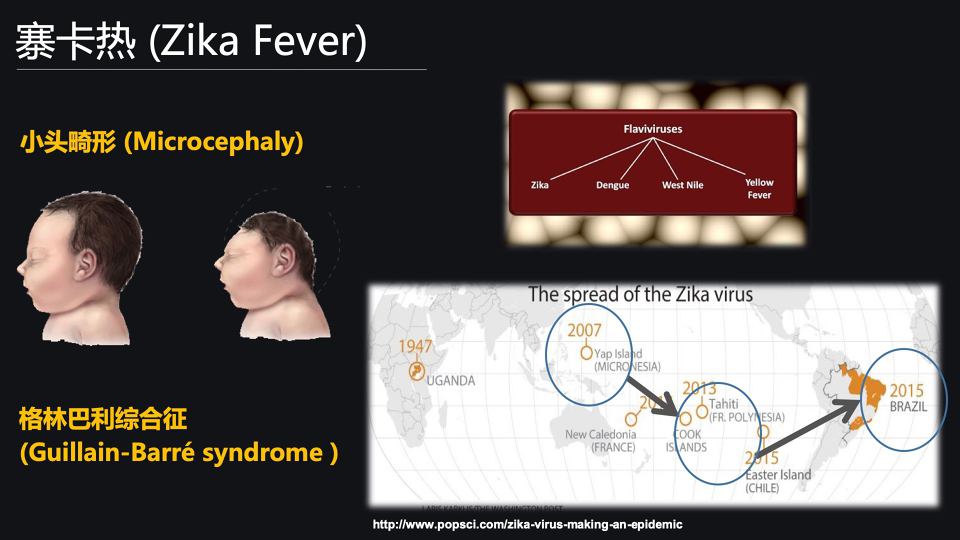
那除了登革热以外呢,由寨卡病毒感染引起的寨卡热,也是一个现代人们最为关注的烈性传染病。
寨卡病毒感染人以后,引起的临床症状与登革热非常类似,包括发热、头痛、关节痛或者皮疹等。
最近的一些临床研究结果显示,一些严重的神经系统症状,像是成年人的格林巴利综合症,或者新生儿的小头畸形,均属于寨卡病毒感染高度相关。
也因此,寨卡病毒在自然界中大规模的感染、散布、流行,也引起了非常严重的公共健康问题。

实际上,根据盖茨基金会的研究报道显示,蚊子已经成为了导致人类死亡的头号杀手了。根据2015年的数据,全世界有83万人之多,被蚊子携带并且传播的疾病感染而导致死亡。
像西尼罗脑炎,自2000年以来在美洲和欧洲多个地方爆发流行,导致至少有250万人感染;那基孔肯雅热呢,在2010年以来爆发流行,导致有200万人感染;寨卡热呢,至少有200万人感染;而登革热的话,每年有3.9亿人被病毒感染或重复感染。
那因此呢,我们深入去研究蚊媒病毒性传染病,去研究蚊媒病毒将具有非常重要的公共卫生意义以及科学意义。
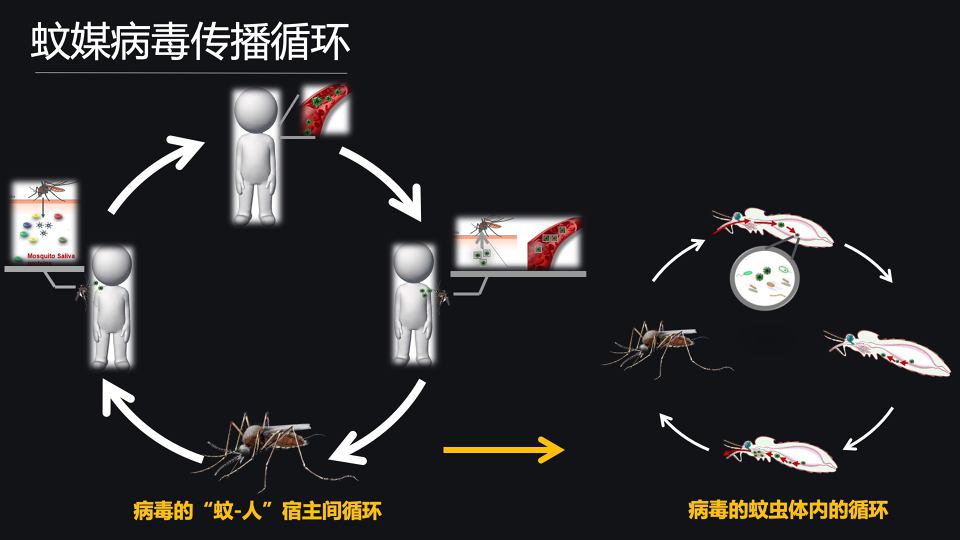
实际上,蚊媒病毒是在宿主和蚊子之间传播循环的。
蚊子先获得了感染,感染的蚊子之后通过叮咬将病毒传播给人,或其他一些脊椎动物宿主。之后病毒呢,在人和宿主体内非常快速的繁殖和扩增,产生非常高量的病毒血症。
那在病毒血症期呢,一个未感染的蚊子可以通过叮咬吸血从而获取病毒;之后病毒回到蚊子体内,感染蚊子的组织,使蚊子具备携带和传播病毒的能力。
再通过叮咬呢,将病毒传播给另外的宿主,就完成这样一个传播循环过程。
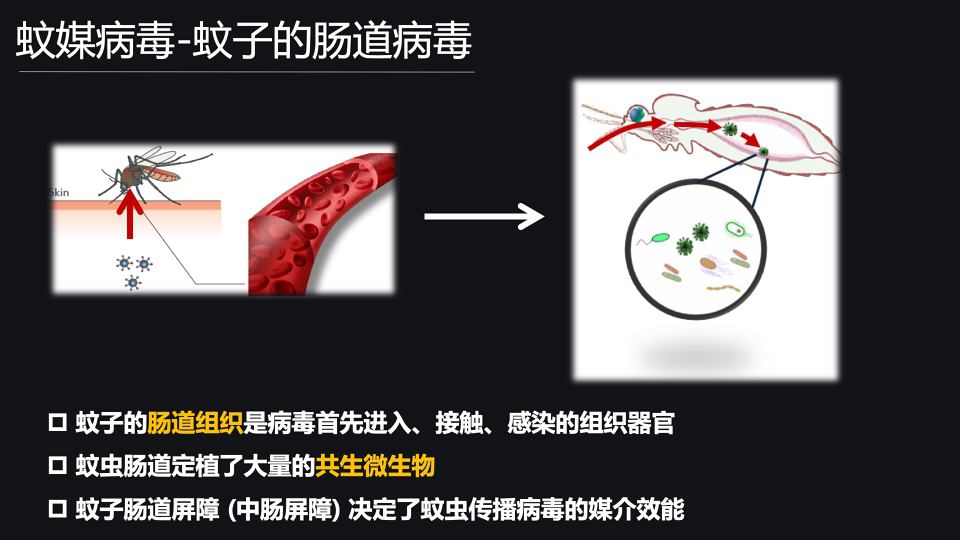
那因此呢,蚊子的肠道组织是病毒首先进入、接触、感染的组织器官。
我帮大家建立一个概念,实际上蚊媒病毒感染人以后,它可以引起脑炎、脑膜炎、出血热等一系列症状。
但是我们知道,蚊子是通过去叮咬吸血感染的宿主去获取病毒,将血液和病毒获取到肠道中来获得感染的。因此蚊媒病毒,对于蚊子来说,是蚊子的肠道病毒。
那实际上,相对于蚊子的唾液腺和血淋巴等对于病毒比较易感的器官来说呢,蚊子的肠道组织可以有效去抵御病毒的感染,是病毒感染蚊虫最主要的生理屏障。
我们有个词叫中肠屏障,实际上蚊子的中肠屏障可以有效的去抵御病毒的感染,去决定蚊虫对于病毒的易感性,从而决定蚊虫携带并且传播病毒的媒介效能。
那我们知道,在肠道中有多种因素,像肠道中的共生微生物、免疫反应、生理屏障等,均可以去调节中肠屏障对于病毒的阻抑能力。
在肠道中,定植着大量的共生微生物,这些共生微生物可以去和获取进入肠道的病毒颗粒相互作用,从而调控病毒在肠道中感染和扩增的整个过程。
于是在这个工作中,我们就希望去研究蚊虫的肠道微生物在病毒感染过程中,到底起到怎样的重要的角色和功能。
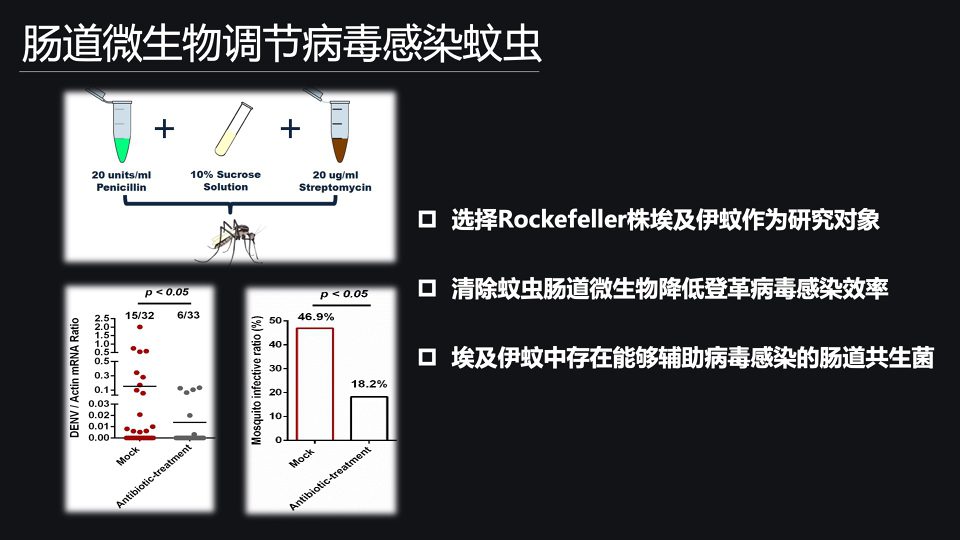
那要回答这个问题呢,我们首先选取了洛克菲勒株埃及伊蚊作为我们研究对象。
洛克菲勒株埃及伊蚊是一个在实验室条件下,长期饲养并且传代的实验室标准蚊株,它是对病毒是普遍的易感。
那接下来,我们就利用含有抗生素的蔗糖溶液去饲喂洛克菲勒株埃及伊蚊,利用人工的方法,在肠道中去清除它的微生物。
接下来,我们再利用含有病毒的血液去饲喂蚊虫、感染蚊虫,在感染后的第八天处死埃及伊蚊,检测病毒载量。
那我们就发现,在肠道微生物被清除以后,蚊虫对登革病毒的感染能力就出现了非常明显的下降。
那这个数据就进一步说明,在洛克菲勒株埃及伊蚊的肠道中,存在某种特异性的肠道共生菌,去辅助病毒在埃及伊蚊体内感染和扩增的整个过程。
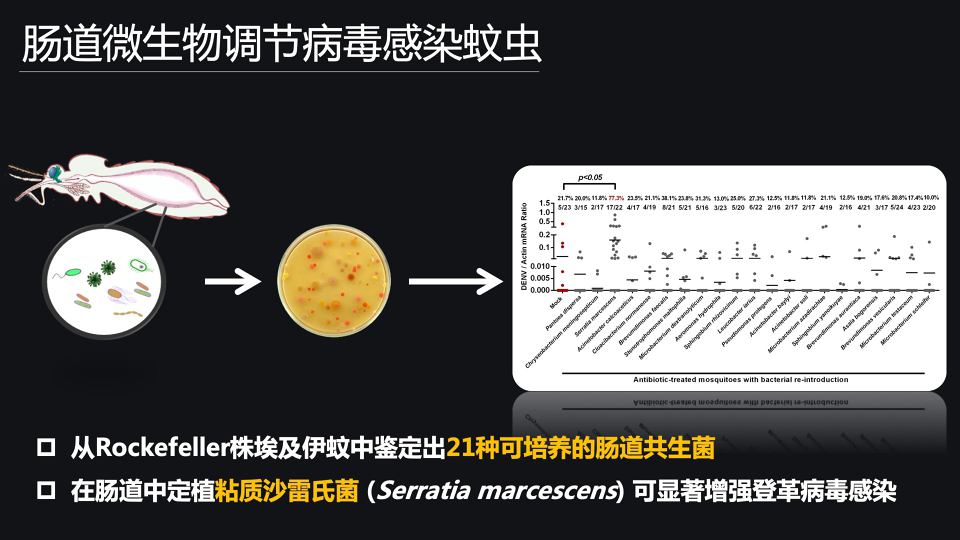
那随后呢,我们就希望鉴定出能够辅助病毒感染蚊虫媒介的肠道共生菌。
我们首先先收集洛克菲勒株埃及伊蚊的肠道组织,把它匀浆以后,利用四种不同的培养基来分离肠道共生菌,最终有21种可以培养的肠道菌,被我们成功鉴定和分离了出来。
随后,我们体外培养这些肠道菌,利用菌悬液和新鲜人的血液,和人的含有病毒颗粒的细胞上清液,混合去饲喂埃及伊蚊。
那最终呢,我们发现饲喂一种粘质沙雷氏菌,可以显著去提高登革病毒在埃及伊蚊体内的感染效率。
那就说明呢,在肠道中定植粘质沙雷氏菌,可以显著增强病毒在埃及伊蚊体内的感染和扩增。也说明粘质沙雷氏菌在肠道中定植,是导致洛克非勒株埃及伊蚊对登格病毒易感的关键性的因素之一。
那随后我们就希望去研究,到底粘质沙雷氏菌是如何辅助病毒感染蚊虫媒介的。
细菌它非常复杂,它利用多种的组分,像是细菌的细胞组分,细菌的分泌蛋白或者细菌的代谢化学产物等,与宿主细胞相互作用,从而辅助细菌在复杂的环境下有效的生存和定植下来。
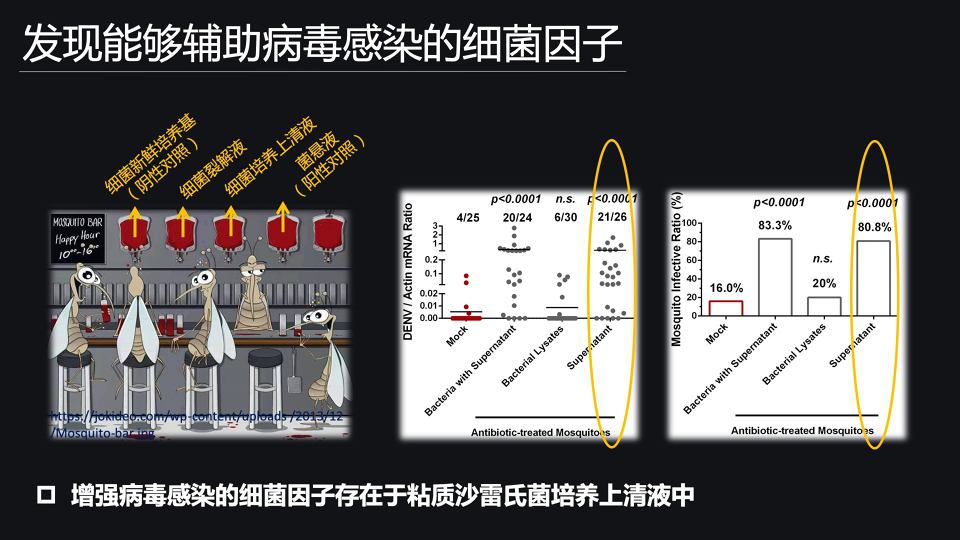
那接下来的话,我们将继续利用功能实验和分离实验,来鉴定出能够辅助病毒感染蚊虫媒介的细菌功能因子。
我们先将粘质沙雷氏菌在37度下培养两个小时,然后利用离心和过滤的方法,来收集细菌培养上清液;那获得的菌体呢,利用超声的方法来破碎,来获得细菌裂解液。
接下来,我们就利用细菌培养上清液和细菌裂解液,分别混合病毒,混合人的血液去饲喂埃及伊蚊。
那我们就发现,原来是饲喂细菌培养上清液而不是细菌裂解液,可以显著提高登革病毒在埃及伊蚊体内的感染效率。
那就说明,能够辅助病毒感染蚊虫媒介的细菌功能因子,它是存在于细菌培养上清液中。但是大家知道,对于细菌培养上清液,也是一个非常复杂的组分。
那接下来,我们将继续利用功能实验和分离实验呢,希望鉴定出能够辅助病毒感染蚊虫媒介的细菌功能因子。
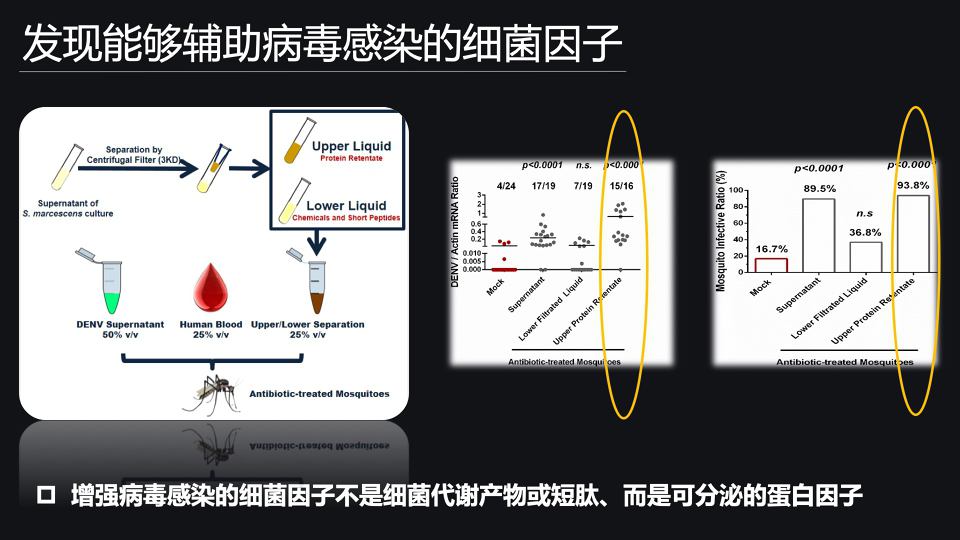
首先,我们先利用3KD的过滤系统来分离细菌培养上清液。在这样的一个分离体系中,上层主要是分子量比较大的蛋白质;而下层是分子量比较小的短肽以及细菌代谢的化学产物等。
那接下来,我们将利用上层蛋白质溶液以及下层的过滤液,分别混合病毒,混合人的血液饲喂埃及伊蚊。
我们发现,饲喂上层蛋白质溶液而不是下层的过滤液,可以显著提高病毒在埃及伊蚊体内的感染效率。
那就说明,能够增强病毒感染的细菌功能因子,它并不是分子量比较小的细菌代谢产物或者短肽等,而是分子量比较大的蛋白质因子。
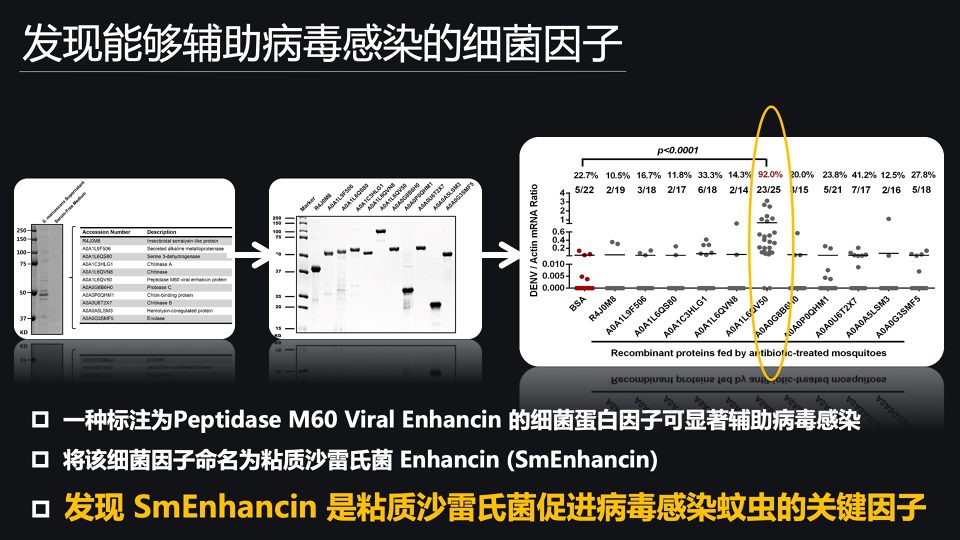
那随后的话,我们就将上层蛋白质溶液在SDS胶中把它给分离,然后再利用质谱的方法来鉴定出溶液中的蛋白组分。
我们选择在质谱鉴定中丰度最高的这些蛋白组分,做为我们的研究对象。我们克隆了这些基因,并在E coli(大肠杆菌)中表达并且纯化这些蛋白。
那我们就发现,饲喂一种标注为Peptidase M60 viral Enhancin的蛋白,可以显著提高登革病毒在埃及伊蚊体内的感染效率。
那就说明,这个蛋白就是我们需要寻找的,能够辅助病毒感染蚊虫媒介的细菌功能因子。我们将这个蛋白命名为粘质沙雷氏菌的Enhancin-SmEnhancin,进行后续的研究工作。

实际上,Enhancin(增强蛋白)这个蛋白并不是被我们第一个发现的,而是在二三十年之前,已经在杆状病毒研究中被人们成功鉴定出来了。
杆状病毒可以去感染昆虫的肠道上皮细胞,再感染和进入昆虫的体内,这是它的整个感染机制。
对于昆虫来说,它的肠道上皮细胞表面一层Mucin粘蛋白层,粘蛋白的主要特点是被高度糖基化,作为物理屏障去分隔肠道上皮细胞和肠道内容物,对肠道上皮细胞起到保护作用。
之前研究结果显示,杆状病毒的Enhancin(增强)蛋白可以非常有效地,去降解在肠道细胞表面的Mucin(粘)蛋白层。从而打破它的物理屏障,辅助病毒在肠道细胞中感染、复制和扩增的过程。
那除了杆状病毒以外,有多种细菌被发现也可以去编码和分泌Enhancin(增强)蛋白。细菌的Enhancin(增强)蛋白,与杆状病毒的Enhancin(增强)蛋白有非常高的同源性,同时功能也非常相似。
于是我们就推测,SmEnhancin(Sm增强蛋白)同样是一个细菌的Enhancin(增强)蛋白。那是否SmEnhancin(Sm增强蛋白)也可以通过去降解蚊虫肠道细胞表面的Mucin(粘)蛋白层,从而去辅助病毒在埃及伊蚊体内的感染和扩增呢?
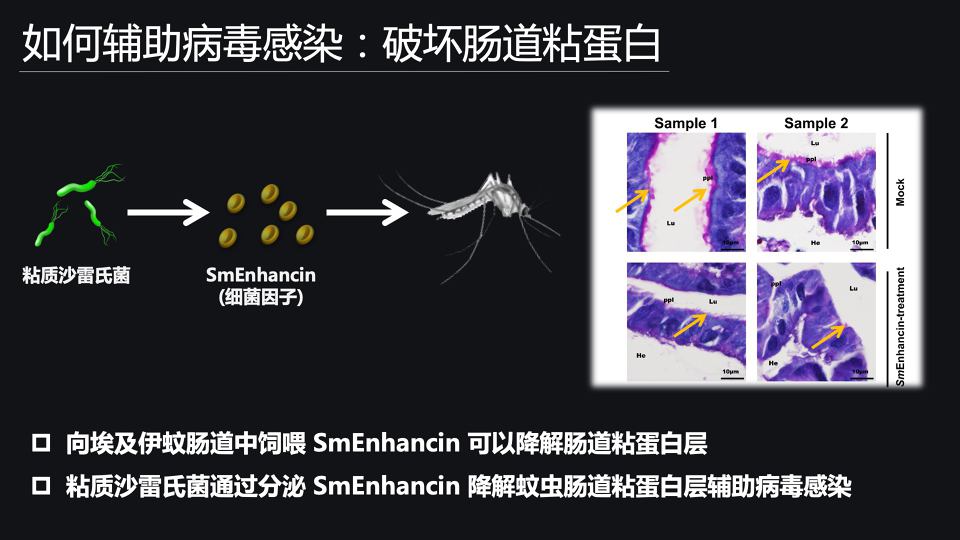
那要回答这个问题,首先我们先将纯化后的SmEnhancin(Sm增强蛋白),直接饲喂到埃及伊蚊的肠道中。我们利用了等量的BSA蛋白(牛血清白蛋白),饲喂埃及伊蚊作为一个阴性对照。
在饲喂之后的12小时,我们收集埃及伊蚊的肠道,进行PAS糖基化染色分析。我们就发现,饲喂了SmEnhancin(Sm增强蛋白)以后,它可以直接去切割在肠道细胞表面的粘蛋白层。
那就说明,粘质沙雷氏菌是通过分泌SmEnhancin(Sm增强蛋白)这样一个细菌功能因子,去降解肠道表面的粘蛋白层,打破它的物理屏障,最终辅助病毒在埃及伊蚊体内感染和扩增的。
实际上,我们之前所有的研究,都是利用洛克菲勒株埃及伊蚊来进行的,它是一个在实验室条件下,长期饲养并且传代的实验室标准蚊株。
那我们还是希望去了解,如果在野生蚊虫肠道中也定植粘质沙雷氏菌,那是否同样可以大幅去提升蚊虫携带并且传播病毒的媒介效能呢?
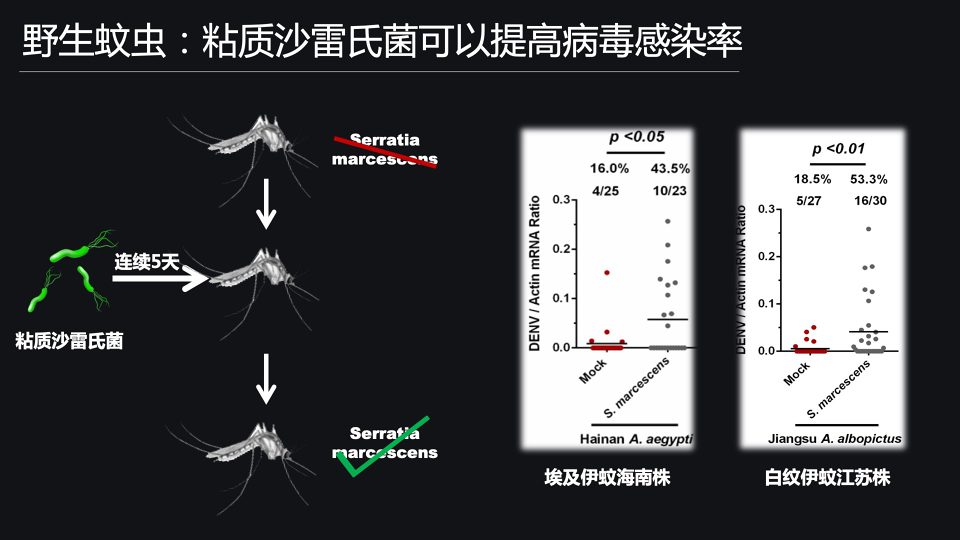
那要回答这个问题呢,首先我们先选取了两株野生的蚊虫,分别是埃及伊蚊海南株以及白纹伊蚊江苏株,做为我们的研究对象。
我们发现,在这两株野生蚊虫肠道中,几乎都没有粘质沙雷氏菌的定植。
接下来我们就利用含有粘质沙雷氏菌的蔗糖溶液,饲喂这两株蚊虫,利用人工的方法在肠道中定植粘质沙雷氏菌。那随后呢,我们再利用含有登革病毒的新鲜人的血液去饲喂蚊虫,感染蚊虫。
那我们就发现,如果你在肠道中定植粘质沙雷氏菌,确实可以大幅去提升登革病毒在野生蚊虫体内的感染能力。
那也说明,在野生蚊虫肠道中,如果你定植了粘质沙雷氏菌,同样可以大幅去提升蚊虫携带并且传播病毒的媒介效能。从而可能会辅助病毒在自然界中大规模的感染、散布和流行。

实际上,粘质沙雷氏菌是一个在自然界下广泛存在、广泛分布的一个环境共生菌。
之前有流行病学公共卫生调查就发现,粘质沙雷氏菌在巴西、在巴拿马、在泰国以及我国广州地区的蚊虫肠道中,被多次反复的鉴定出来。而这些地区均是登革病毒在自然界中爆发流行的关键区域。
于是我们就推测,粘质沙雷氏菌在自然界中的分布和定植,与登革病毒的爆发流行具有非常密切的关系。
那当然了,这种相关性还需要进一步的流行病学公共卫生调查,然后来进行验证。因此,我们未来的研究兴趣之一,就是希望在自然界中,继续验证登革病毒流行与粘质沙雷氏菌分布之间的相关性。
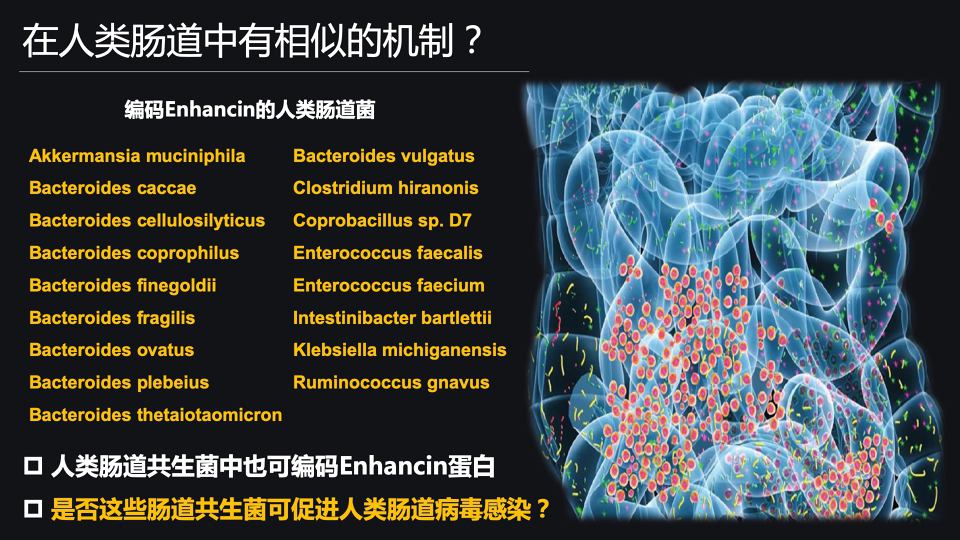
我们另外一个研究兴趣,是关于人类的肠道菌。
那我们知道,很多的肠道菌都可以分泌和编码Enhancin(增强)蛋白。从人类的肠道共生菌中,发现了有17个不同的肠道菌可以去编码Enhancin(增强)蛋白。
理论上说,这些人类肠道菌所编码的Enhancin(增强蛋白),有可能能够降解人类肠道的粘蛋白层,从而去调控人类肠道的免疫平衡。
那是否这些人类肠道共生菌,也可以去促进人类肠道病毒的感染呢?那是否的话,这些人类肠道共生菌在肠道中的定植,与人类对于肠道病毒的易感性之间,存在非常密切的联系呢?还需要我们进一步的调查和研究。

那最后呢,我想总结一下我们的研究。
我们创造性地利用埃及伊蚊和蚊媒病毒,作为研究对象和研究平台。我们就发现,粘质沙雷氏菌作为一个肠道共生菌,它可以去辅助病毒在埃及伊蚊体内的感染和扩增。
那进一步研究结果发现,实际上粘质沙雷氏菌是通过分泌SmEnhancin(Sm增强蛋白)这样的一个细菌功能因子,去降解在肠道细胞表面的Mucin(粘)蛋白层,打破它的物理屏障,最终辅助病毒感染和扩增的过程。
同时,我们进一步研究结果发现,如果在野生蚊虫肠道中定植粘质沙雷氏菌,同样可以大幅去提升蚊虫携带并且传播病毒的媒介效能。
那就说明,粘质沙雷氏菌在自然界中的定植和分布,与登革病毒的爆发流行可能存在非常密切的关系。
同时也进一步说明,肠道微生物在病毒感染过程中,确实起到非常关键的调控功能。
最后呢,感谢各位老师、各位同学、各位专家的聆听,谢谢大家!

谢谢大家!


