
各位老师,各位同道,大家好!
我是美国夏威夷大学癌症研究中心的贾伟,从事基于代谢组学的癌症代谢和生物学研究。那么今天呢,我跟大家分享的主题是肠道菌与肝脏疾病。
说到肝脏,大家都不陌生。它是我们人体最大的一个代谢器官,承担了我们人体非常重要的生物分子的生化合成和代谢。
这些生物分子包括糖、蛋白质、脂质、胆固醇等等,那么还有一类物质——胆汁酸也是我们肝脏合成出来的。
那么在几十年以前,胆汁酸一直被认为是一类非常简单的肠道消化液,没有什么大的作用,就是帮我们人体吸收和消化来自于食物的脂肪。
那么最近10年的研究结果让我们非常震惊,我们发现胆汁酸是一类非常非常重要的生化分子。
它不仅仅能够帮助我们消化和吸收来自于食物的脂肪,还可以调控脂肪代谢,还可以调控我们的糖代谢,调控药物代谢,还可以调控很多很多生物分子的肠肝循环和体内平衡。
肝脏也可以被认为是一个解毒器官,它可以分解和代谢我们体内的毒性物质,所有摄入我们人体的毒性物质。
包括药物、药物的代谢物,以及我们食物当中分解出来的带有毒性的代谢产物,都会在我们肝脏代谢酶的作用下面,分多种渠道进行解毒。
我们讨论肝脏的代谢功能,我们不得不说一下肠道细菌,因为我们知道肠道菌群也同样具有很重要的代谢功能。
事实上,我们可以说,肠道菌群是我们人类后天获得的一个非常非常重要、不可或缺的代谢器官。
所有摄入我们体内的食物、营养都会在肠道接触到肠道细菌,被我们的肠道细菌所代谢。
那么反过来,肠道细菌如果失衡、如果紊乱,也可能会产生毒素,这些毒素会通过肠屏障和门静脉进入肠肝循环,加重肝病的发展。

肝脏疾病有很多种,包括脂肪肝、肝炎、肝硬化、肝性脑病、肝癌等等。
那么肝脏的病因又比较复杂,它包括了病毒性的感染,叫病毒性肝炎;那么还有因寄生虫感染而得的肝炎,还有由于饮食不当、过度饮酒、过度的高脂饮食引起的脂肪性的肝炎。
那么病毒肝炎包括了甲型病毒性肝炎,我们称之为甲肝,还有乙肝、丙肝等等;而黄曲霉菌感染过的食物则会使我们的肝脏产生黄曲霉素中毒;大量的长期的饮酒可以诱导出酒精性的脂肪肝;那么高脂饮食可以导致脂肪性的肝炎。
那么在肝病当中,最为危重的疾病就是肝癌了。
最新统计呢,全世界每年约有85万例左右的新发肝癌病人,其中有47万例,就是超过一半的人在中国。中国是个肝病大国,也是肝癌大国。
讨论肝癌呢,我们有一些这个领域里面最新的一些发现可以跟大家分享。
那么随着我们人类对于癌症的防控手段的不断的提升,那么在世界范围之内,很多大的癌种的发病率和死亡率都在缓慢的下行。
但是呢,肝癌作为一个非常恶性的肿瘤,一个5年生存期不到18%的恶性肿瘤,它的发病率其实并没有得到有效的控制。
我们不说别的国家,在美国,肝癌的发病率不降反升,这是很重要的一个现象。
那么第二个现象呢,临床上有一个很重要的、也是很令人费解的观察,就是不少患者即便是去除了病因,比如说停止饮酒,不再吃高脂饮食,肝炎病毒已经被控制住了,但是这些病人的肝脏疾病仍然可能会进展为肝纤维化、肝硬化、甚至肝癌。
也就是说,在传统意义上几个重要的肝癌病因之外,似乎还有一些不为我们所知的因素,它们作为推手,在推动着整个肝病的发展病程。
那么第三个现象呢,是脂肪性肝病最终导致肝癌的比例,是远远低于病毒感染性肝炎。但是脂肪性肝病的人群基数是非常大的。
从现在开始说起,在不远的将来,也许是10年,也许是15年,当我们的肝炎病毒被得到非常好的控制以后,脂肪性肝炎就可能完全超越其他的因素,成为肝癌的第一大病因。

那么在这儿呢,我要隆重的向大家介绍出一个观点。从肝炎到肝癌的转换过程中,肠道微生态的失衡,我们称之为Dysbiosis是一个很重要的推手,这也是我们今天的主题。

观众当中可能有人知道,我是做代谢组学的。我们实验室从2003年开始,学习和开展代谢组学的研究。
那么什么是代谢组学呢,用一句很简单的话来概括呢,代谢组学其实就是利用一种或者几种高分辨率、高灵敏度的分析仪器,对一个生物样本内所有的代谢产物进行全谱定量的分析。
那么更重要的是,我们还要分析和检测这些代谢物在不同的时间、不同的病理生理条件下的动态变化。
那么在几年前呢,我们实验室建立了一个全自动、全定量的肠道菌代谢组的检测方法,这个方法可以检测200~250种菌群和宿主共代谢的产物。
我们认为这样的方法,是基于宏基因组研究菌群代谢功能和疾病机制的一个重要的方法学上的补充。
有了代谢组学,我们可以非常快速的检测一些病人的血液、尿液甚至是唾液。
我们来看一看肠道细菌是否在病理生理过程当中扮演着一些重要的角色,我给大家介绍几个案例。
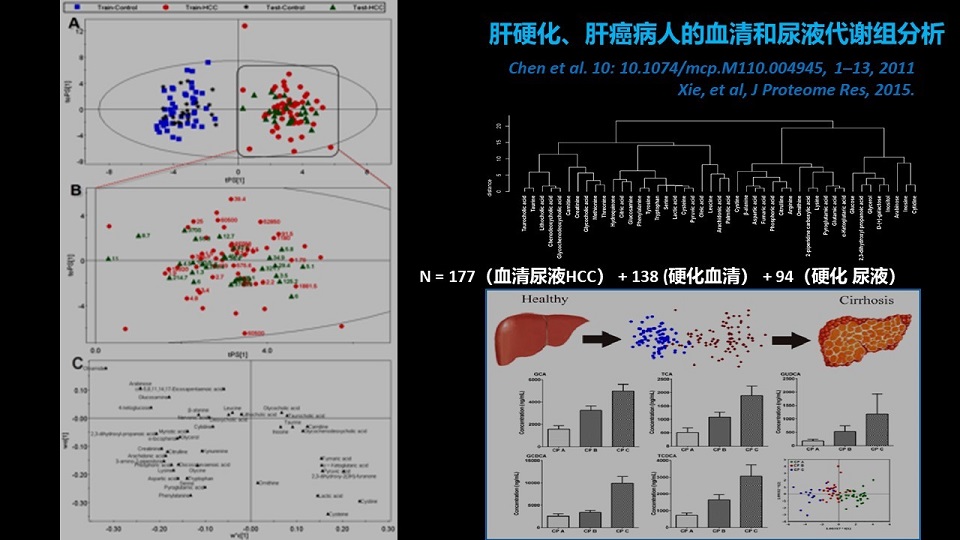
那么我们采用代谢组学,分析了177例包含了健康对照、良性肝脏肿瘤还有肝癌病人的血清和尿液的代谢组,这是全谱的代谢组学检测。
我们发现很多跟肝癌高度相关的代谢变化,都来自于肠道细菌的代谢产物。其中最最显著变化的6个肝癌的Biomarkers(生化标志物),全部是胆汁酸,其中有三个还是肠道菌群代谢过的次级胆汁酸。
那么我们又做了第二个队列的验证,分析了138例肝硬化患者的血清样本,那么这样的验证非常成功,我们同样发现胆汁酸是肝硬化病人的非常显著的生物标志物。
那么最后我们还用了94例肝硬化病人的尿液样本,我们来看一看,在尿液样本当中,胆汁酸是不是依然是显著的变化。
结果是非常显著,而且肠道菌群代谢过的次级胆汁酸,可以完美的区分肝硬化的三个不同的病理分期。
也就是说,胆汁酸代谢,尤其是肠道菌群的胆汁酸代谢,与肝病的发生和发展是密切相关的。
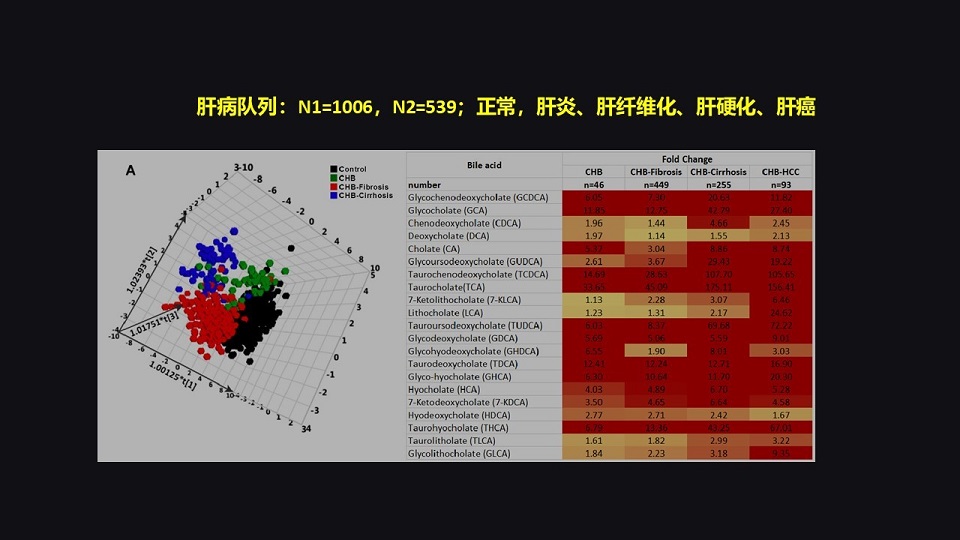
我们后面集中火力,对一个比较大的肝病队列进行胆汁酸的全谱分析。这个对列是包含了1006例正常对照、肝炎、肝纤维化、肝硬化的病人。
那么我们看到,几乎是所有的胆汁酸都非常显著的升高,在不同的病理阶段全面升高。
那么为了要验证它,我们又获得了一个539例的独立的队列,它是肝纤维化和肝癌患者。
那么在这个队列里面,我们同样也看到了几乎是完全一致的检测效果,那就是说胆汁酸全面升高。
那么既然胆汁酸如此重要,那么我们就要看一看,它是如何与我们肠道菌发生关系。
当我们吃饭,尤其是进食带有脂肪的食物的时候,我们的胆囊就会分泌胆汁进入小肠,这个胆汁里就是胆汁酸。
那么它们不仅仅是帮助我们消化和吸收食物当中的脂肪,它们还会与肠道细菌进行互相作用。
它们同时也会杀灭一部分肠道细菌,因为它们还是有抑菌性的;但是反过来,它们又被肠道细菌所代谢。
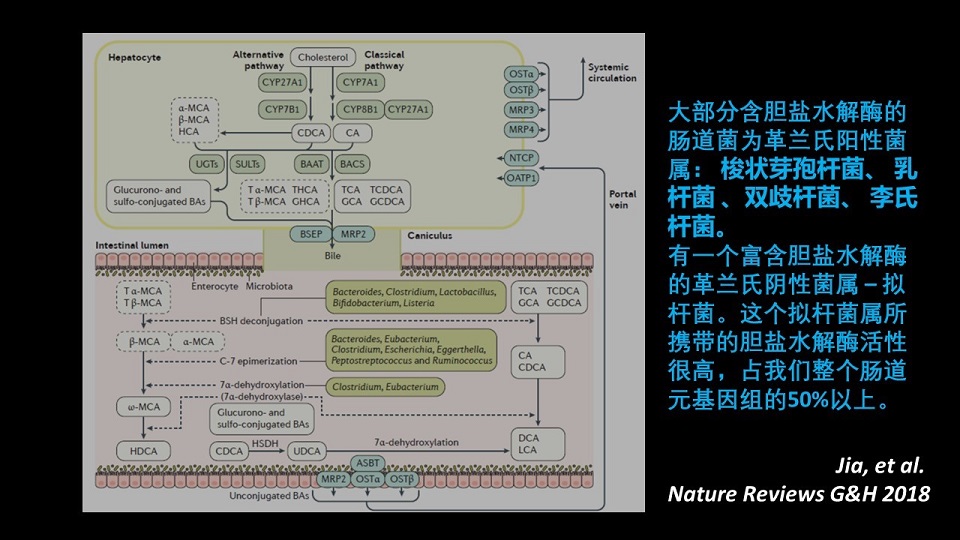
那么这个代谢主要分两步,第一步是氨基酸的解离反应,肠道细菌把甘氨酸和牛磺酸从胆汁酸上切开来。那么我们需要一种酶,叫胆盐水解酶,Bile Salt Hydrolase(BSH)。
那么另外一步也是很重要,它可以把游离的初级胆汁酸变成游离的次级胆汁酸,那么这一块需要一个酶,叫7α-Dehydroxylase,就是7α位上的脱羟酶。
所有能够代谢胆汁酸的肠道细菌都拥有这两个酶,或者至少是两个酶当中的一种。
那么我还要介绍的呢,就是大部分含有Bile Salt Hydrolase(胆盐水解酶)的肠道菌都是革兰氏阳性菌。
那么革兰氏阳性菌属当中,含有Bile Salt Hydrolase(胆盐水解酶)的细菌,包括了梭状芽孢杆菌、乳杆菌、双歧杆菌、李氏杆菌等等。
还有一个富含胆盐水解酶的革兰氏阴性菌也非常重要,它叫拟杆菌,大家也许非常熟悉。
为什么说拟杆菌特别重要呢,因为它所携带的胆盐水解酶的活性非常高,占了我们整个肠道宏基因组的50%以上。
我们再介绍一个大的队列研究,我们夏威夷大学癌症中心的癌症流行病学的一批同事们,牵头开展了一个大型的多种族的队列研究。
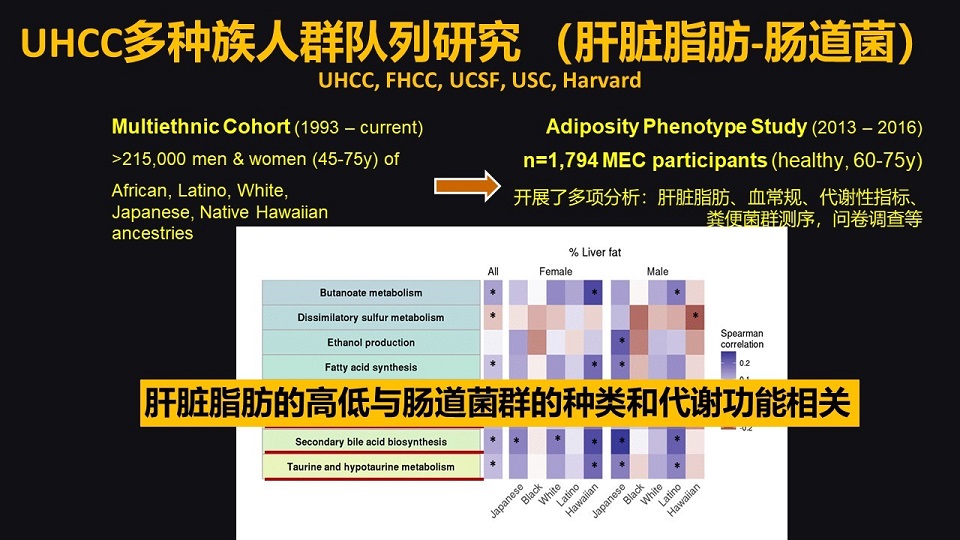
我们筛选了215,000个人,这215,000人包括了非裔美国人、拉丁美裔、白人、日裔,还有就是夏威夷本地人。我们从中精选了1794个健康的合格的个体,年龄在60~75岁。
我们针对这个人群开展了多项分析和研究,我们检测了他们每一个人的肝脏脂肪情况,我们检测了每一个人的血常规,我们检测了每一个人的代谢性的指标。
更重要的是,我们检测了粪便样本当中的菌群序列。最终这个研究发现,与肝脏脂肪堆积程度正相关的、最显著相关的是肠道细菌当中的次级胆汁酸的代谢功能。
另外也有几个相关的代谢功能,包括甘氨酸代谢、牛磺酸代谢,大家都知道这跟胆汁酸都有关系。那么还有就是Lipopolysaccharides(脂多糖)的代谢。
所以我们发现的最显著的几条代谢通路,或者说几个代谢功能都是跟胆汁酸代谢有关系。也就是说,我们肝脏脂肪的高低与肠道菌群的种类和代谢功能,尤其是次级胆汁酸代谢的功能密切相关。
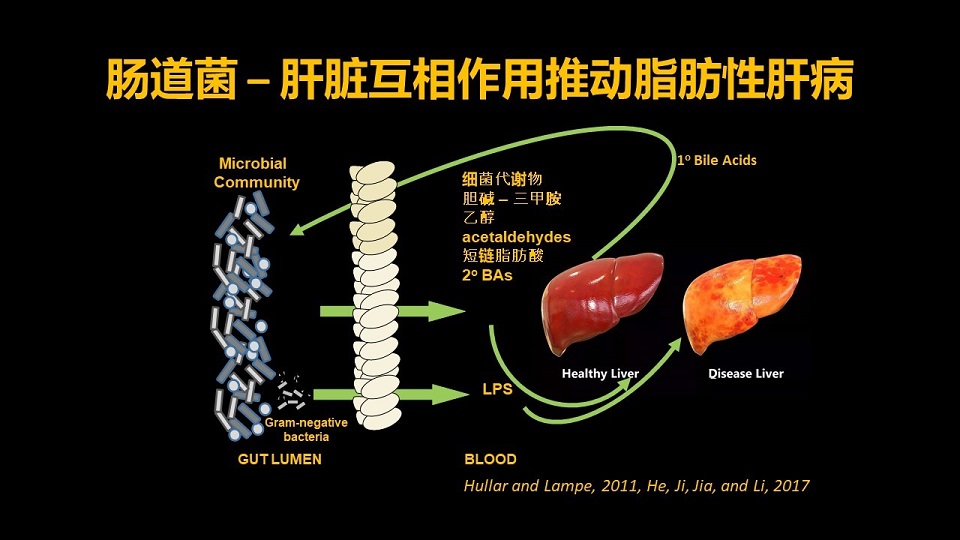
那么这张图告诉我们,肠道菌和肝脏互相作用,其实是通过它们的代谢产物来实现的。这些代谢产物呢,包括了来自于胆碱的三甲胺、乙醇、乙醛类的代谢产物。
那么也许有人要问,哪来的乙醇呢?哪来的酒精?那么我们能够设想一下,肠道细菌在我们的体内就是一个菌群组成,肠道就是一个发酵罐。
我们食物进来,经过发酵,肯定有酒精产生。那么酒精的下游代谢产物,就是乙醛,醛类物质。
那么还有短链脂肪酸,那么更重要的还有次级胆汁酸,还有一类物质,也是刚才提到的LPS,Lipopolysaccharides,就是脂多糖。
那么这些肠道细菌的代谢产物,通过肠屏障,通过门静脉进入肝脏,可能参与推动脂肪性的肝病的发展,从慢性肝炎到纤维化、硬化和肝癌。
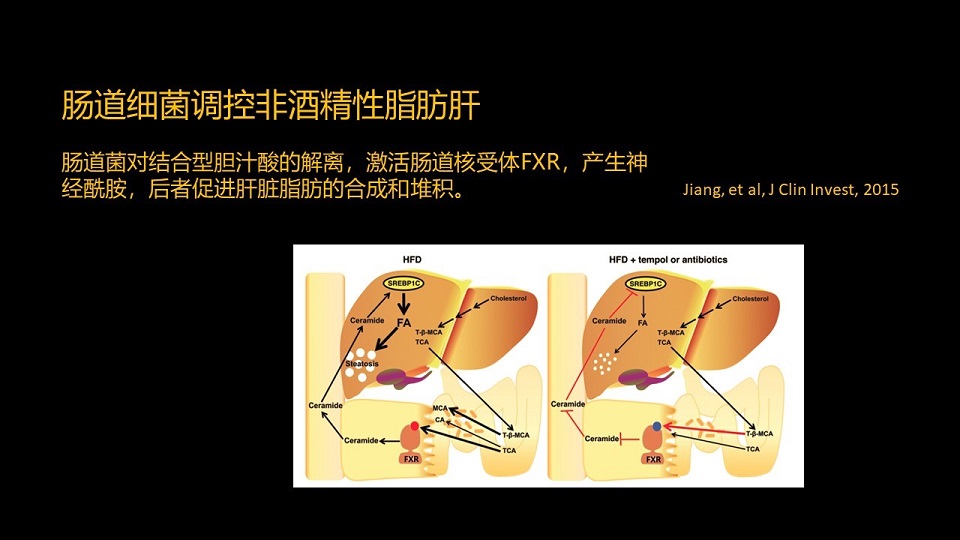
介绍一个相关的研究,我们北京大学的学者姜长涛和他在美国国立卫生研究院的合作者——Frank J. Gonzalez 一起合作研究。
他们发现了肠道菌对结合型胆汁酸的解离,也就是说产生出来的游离的胆汁酸,尤其是次级胆汁酸可以激活肠道核受体FXR(法尼醇X受体),产生一种物质叫神经酰氨。那么这个神经酰胺进入肝脏以后,可以促进肝脏脂肪的合成和堆积。
那么这个是非常漂亮的一个机制性的工作。
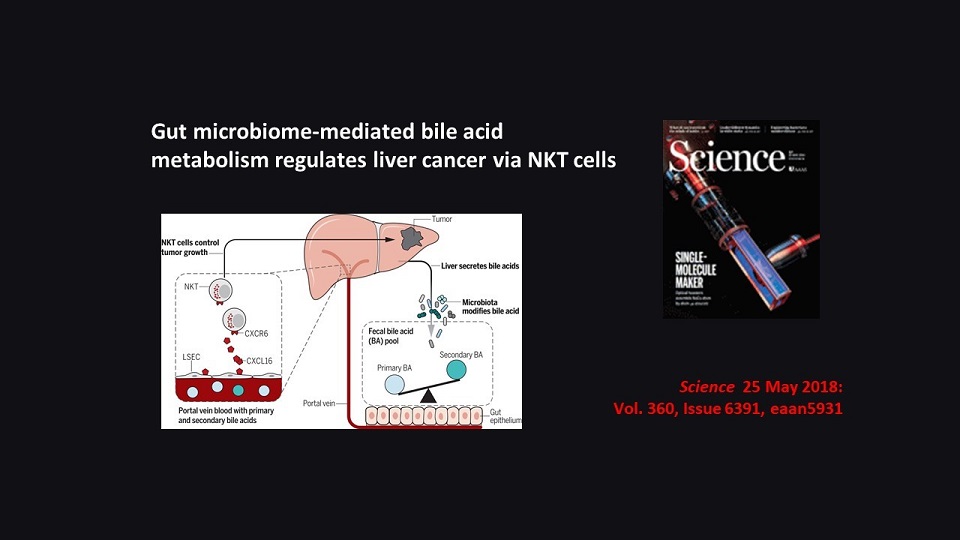
最近还有一篇文章发表在Science《科学》上面,我认为也是非常非常有意思的。
那么这个故事呢,讲的是从肝脏产生的初级胆汁酸,和被肠道细菌代谢过的次级胆汁酸,这两类物质其实存在着一个平衡。
初级胆汁酸可以激活一种蛋白,叫CXCL16,这个蛋白可以激活一个很重要的免疫细胞,叫NKT免疫细胞(自然杀伤T细胞),它是可以抑制肝脏肿瘤的。
那反过来,我们的次级胆汁酸能抑制这个CXCL16蛋白,从而抑制NKT细胞的增殖和积累,当然结果是促进肝脏肿瘤的发生和发展。
所以,这就是一个非常非常重要的平衡关系。也就是说,肠道细菌可以通过对于次级胆汁酸的生成的多和少,来调控我们肝脏里面非常重要的免疫细胞,进而调控肿瘤的升还是降。
基于前面种种种种的发现,我们现在要跟大家讲,我们的科学假说是什么。
我们认为,与肝病高度相关的肠道菌群的一个重要特征,是含有Bile Salt Hydrolase(胆盐水解酶)和7α-Dehydroxylase(7α-脱氢酶)。
那么这样的一个菌群结构可以推动脂肪性肝炎往纤维化、硬化和肝癌方向发展。
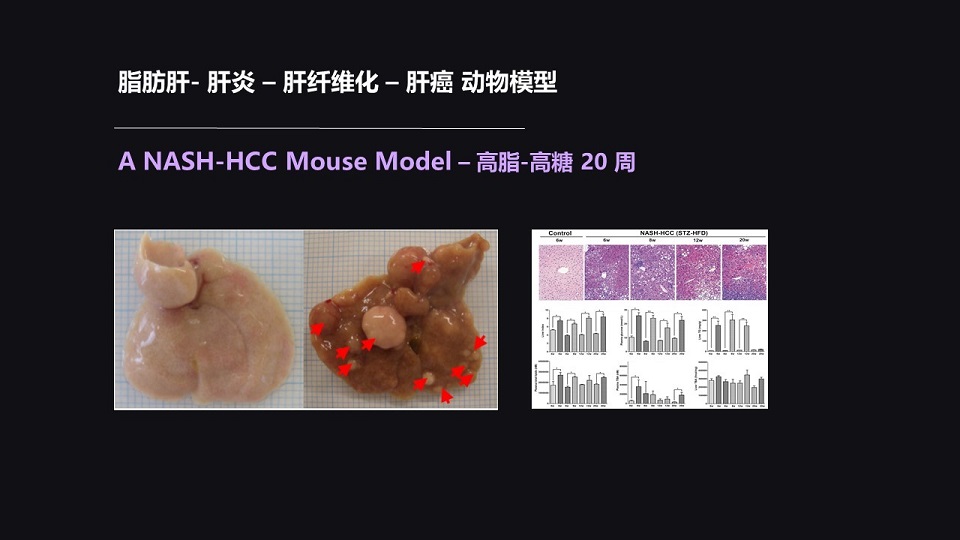
针对这样的一个假说,我们采用了一个动物模型——高脂高糖20周这么一个非常快速的产生肝癌表型的模型。
很重要的呢,是这个动物模型可以产生出脂肪肝、脂肪性肝炎、肝纤维化、肝癌4种表型。
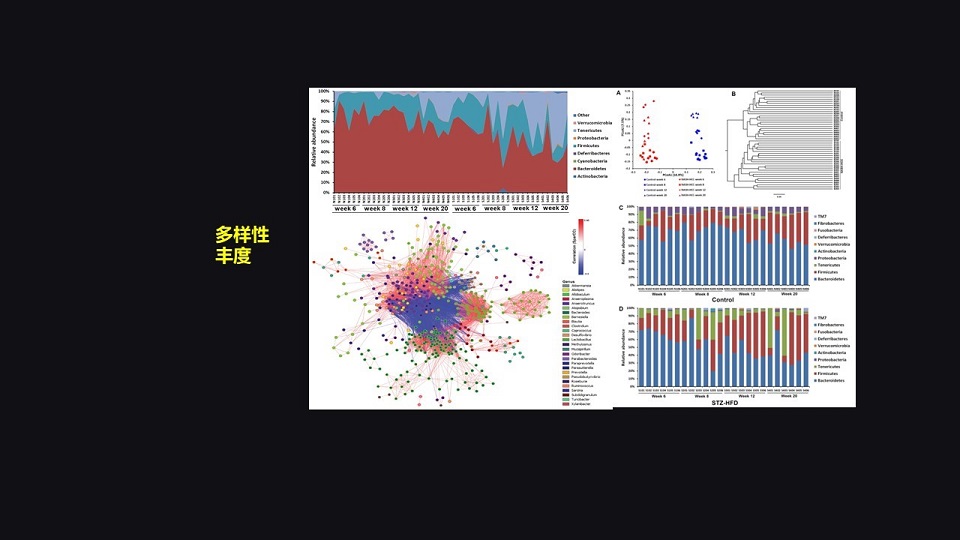
那么经过肠道菌群测序,我们发现肠道细菌的多样性和丰度,随着肝病的发展是逐步下降的。
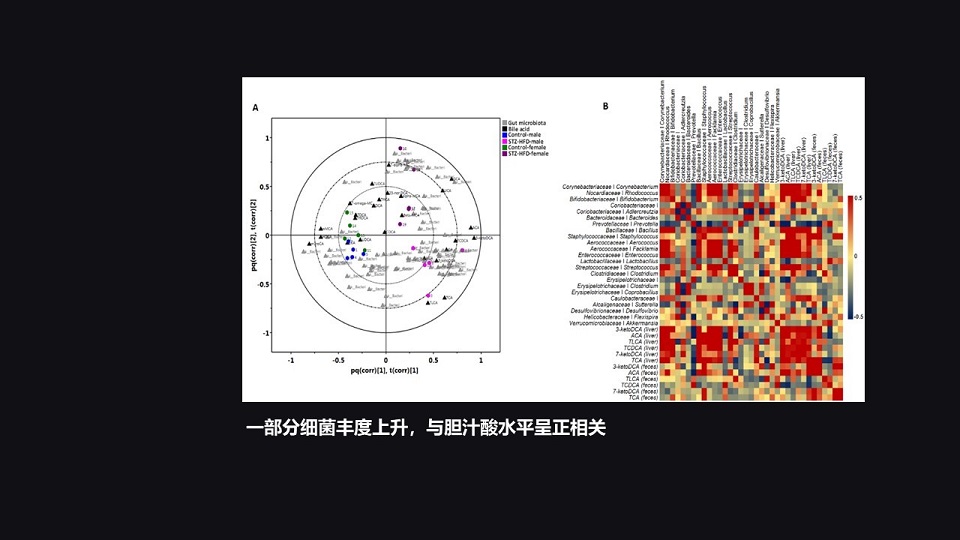
那么,尽管总的丰度在逐步下降,其中还是有一部分细菌的丰度是逐步上升的,而它们跟胆汁酸水平呈正相关。
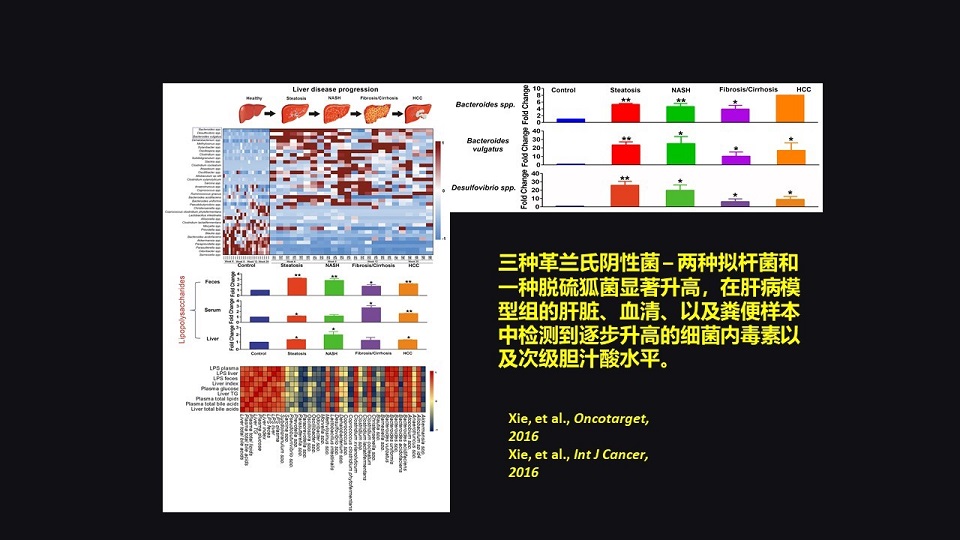
它们是什么呢?那么我们仔细分析下来,发现最重要的有三种革兰氏阴性菌、两种拟杆菌和一种脱硫弧菌显著升高。
我们知道,这三种革兰氏阴性菌具有胆盐水解酶,可以降解胆汁酸产生次级胆汁酸;我们也知道,它们因为是革兰氏阴性菌,他们会产生LPS脂多糖。
那么果然,我们在肝病的这个模型组当中,我们发现肝脏、血清以及粪便样品中,我们都能够检测到逐步升高的细菌内毒素,以及逐步升高的次级胆汁酸水平。
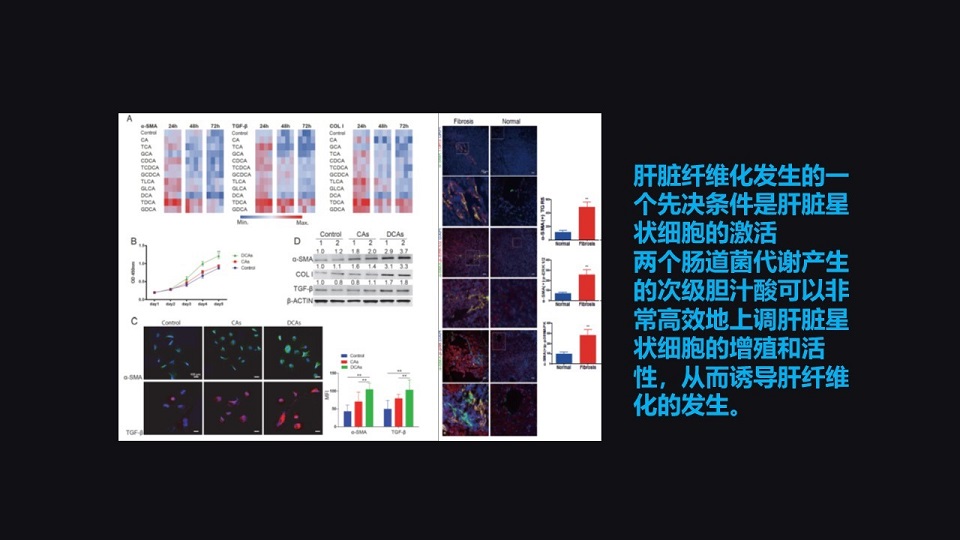
那么我们还知道,肝纤维化的发生要有一个非常非常重要的步骤,有一个先决条件。那就是肝脏的星状细胞需要被激活,它有大量的生成。
那么很有意思呢,我们发现有两个被肠道菌群代谢产生的次级胆汁酸,可以非常高效地上调肝脏星状细胞的增殖和活性,它们能够非常高效地诱导肝纤维化的发生。
那这也是一个非常重要的机制性的发现。

所以针对肠道胆汁酸的代谢,我们也做了很多干预的措施。比如说,我们用了抗生素,发现它确实可以显著降低肿瘤的发生。
但是很重要的,或者很有意思的一个措施,我们用了一种离子交换树脂,用来吸附肠道细菌产生的次级胆汁酸。
我们发现它可以非常有效地降低肠道内的次级胆汁酸的水平,可以非常有效地改变肠道菌的结构。但是更为重要的是,它完全阻断了肝纤维化和肝癌的发生。
当然这是一个非常惊人的实验结果,我们重复了好几次,发现都是这样的。

我们来总结一下。
肠道菌与肝脏疾病高度相关,但是没有证据显示肠道细菌直接导致肝癌。所以我本人并不认为有一个因和果的关系在这里,肠道细菌并不直接导致肝癌。
但是它扮演的角色呢,是一个推波助澜的作用,它是一个推手。
在肝病的发展过程中呢,肠道菌群结构发生特征性的改变。这些改变促进了肝病从简单的炎症往纤维化和肝癌的方向转化。
那么肠道菌与肝脏的相互作用,是通过它一系列的代谢产物来实现的。这些产物包括了次级胆汁酸,包括了脂肪酸,包括了脂多糖等等,它们能够促进肝病往纤维化硬化和肝癌的方向进展。
了解了肠肝代谢作用的机制,我们可以设计全新的疾病诊断和干预方法,来达到早期诊断、早期治疗这么一个目的。
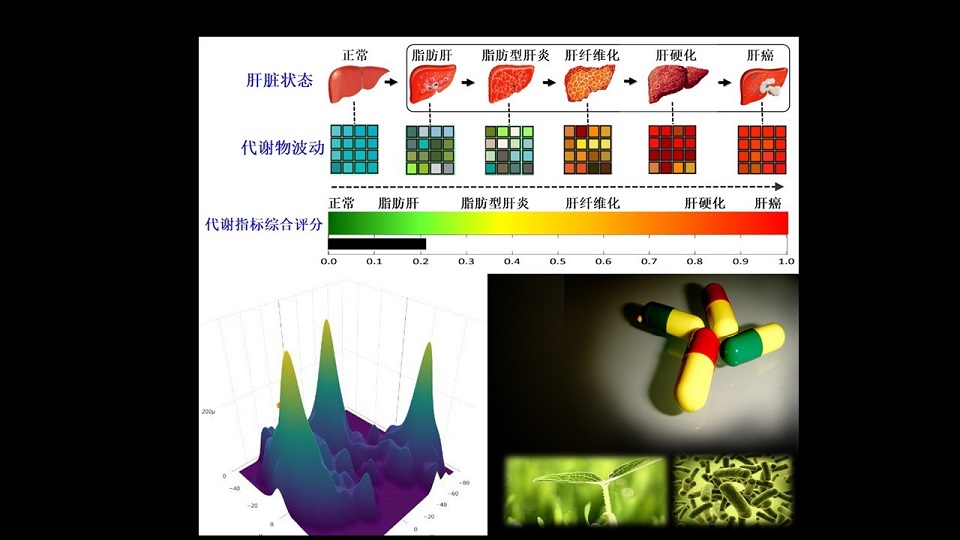
那么基于我们的前期的研究结果,我们最近建立了一种快速的、无创的、精准的诊断肝脏疾病的分期的一个体外诊断试剂盒。
不需要做穿刺,只需要一滴血,借助于我们的分析仪器、质谱和我们的工作软件,我们可以在肝脏的疾病谱当中,把病人的病理状态准确地进行定位。
同时针对肠道菌群的胆汁酸的代谢,我们又开发了靶向性的治疗药物。那么,这可能也是一个全新的策略,就是说肝病肠治。
这些诊断技术和治疗技术,我们都已经申请了国际和国内专利,目前处于产业化的阶段。

最后我要感谢我们课题组所有参与相关研究的人员,以及我们一些重要的合作伙伴,比如英国帝国理工大学的Jeremy K. Nichoson教授,美国北卡大学药学院的Kim Brouwer教授,还有我们上海中医药大学的刘平教授。
最后要感谢热心肠的科普平台,谢谢大家!


