
大家好,我叫司同,是中国科学院深圳先进技术研究院合成生物学研究所研究员。
非常感谢热心肠研究院的邀请。今天想和大家分享一下我们在自动化合成生物技术与人类来源微生物活性天然产物方面的研究。

首先什么是天然产物?我们为什么要关心微生物天然产物?
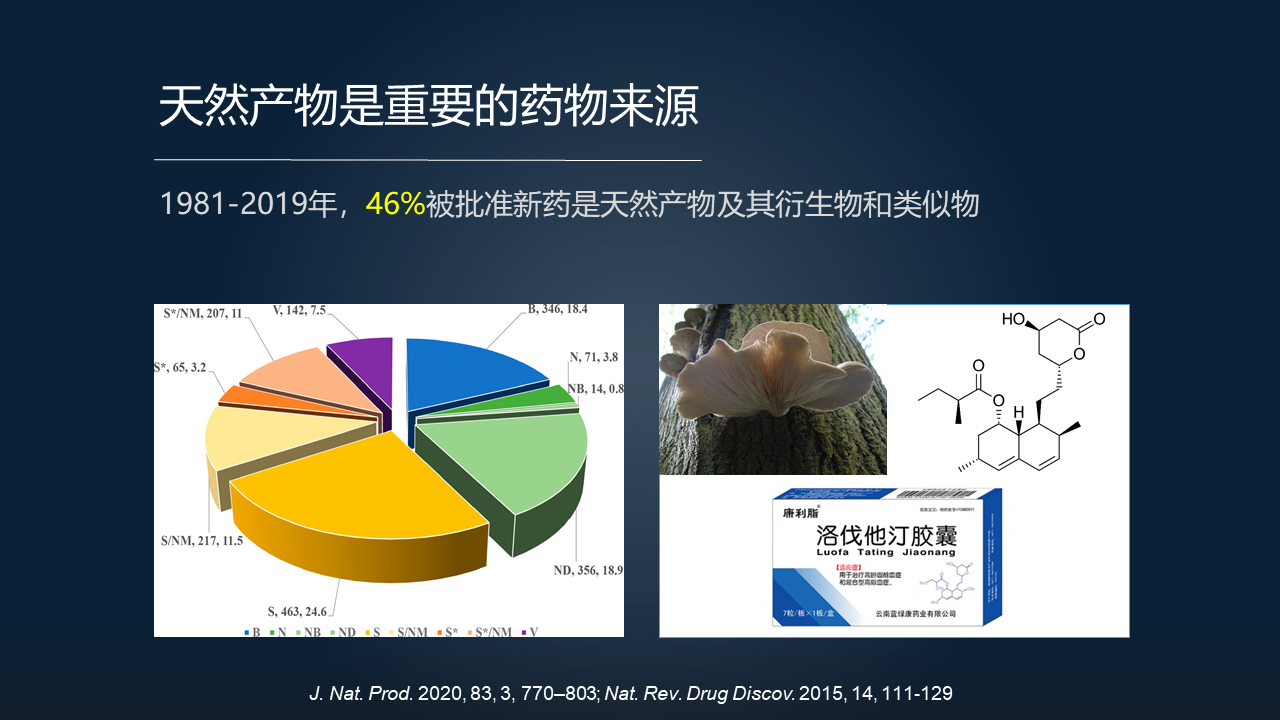
天然产物是指由微生物、动物、植物经过次生代谢所生产的一些小分子。
和绝大多数生物所共有的初级代谢的分子相比,天然产物具有更为丰富的分子结构、更为多样的生理生态功能等等。据统计,1981~2019 年被批准的新药当中,有近 50%是天然产物及其衍生物或者类似物,所以天然产物是重要的药物来源。
比如说大家看到右边的这样一个洛伐他汀的分子,它是由天然的真菌——长得像蘑菇这样的一个生物所生产的。它具有降低胆固醇的效用,可以用于冠心病的预防和治疗等等。
目前,主要的天然产物是来自于环境,包括土壤、海洋等等。
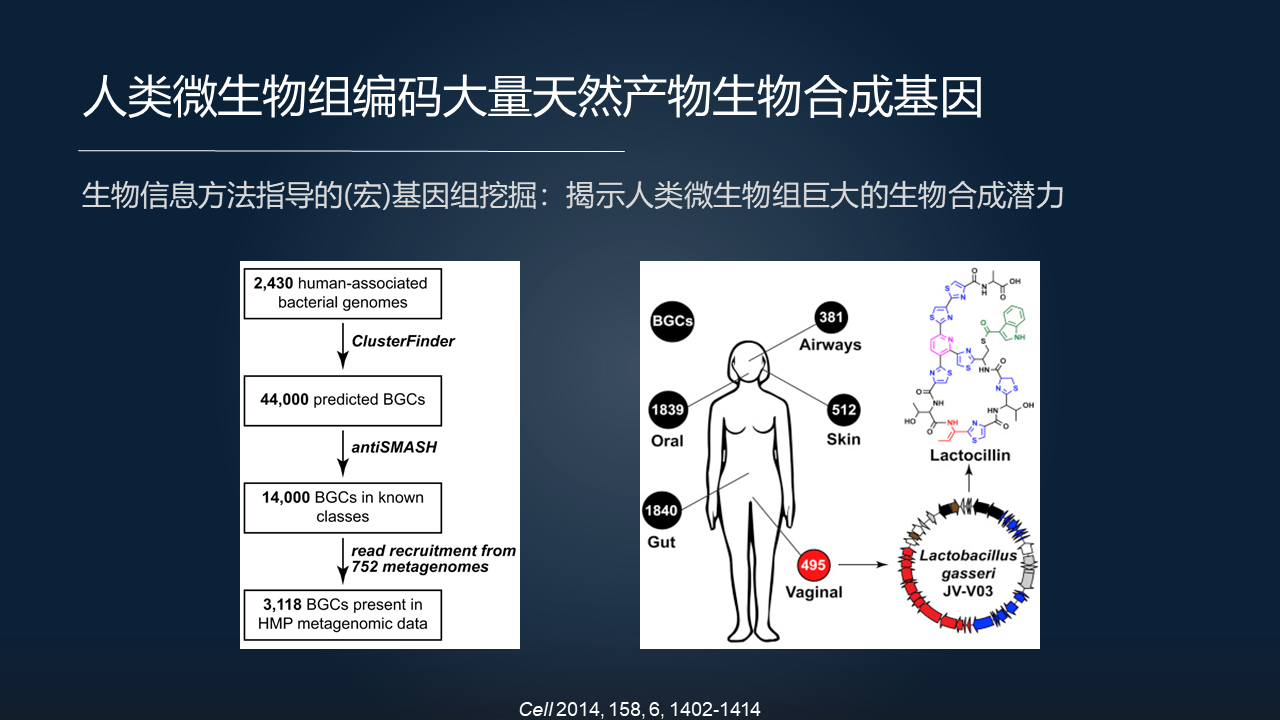
另一方面,我们知道,在人体当中有和人体细胞数量接近相同量级的微生物细胞,这些微生物是不是在人体当中也会生产这样的天然产物?
2014 年,Michael Fischbach 研究组他们通过生物信息学的方法,分析了和人类相关的细菌的基因组,然后发现,在其中存在大量的天然产物生物合成的基因和基因簇。通过分析发现,这些在人类相关的宏基因组当中也大量存在,证实了在人体当中这些微生物存在着巨大的生物合成的潜力,可以生产这些次级代谢的产物。
那么在人体的不同地方有成百到上千的天然产物生物合成基因簇,他们从其中也分离得到了这样一个结构复杂的乳酸菌来源的天然产物。

这样的研究很自然而然地会给我们提出一个问题,就是这些分子在我们人体当中到底有没有相关的功能?会不会影响我们的疾病与健康?
目前绝大多数的微生物组的研究还是基于一个相关性研究,比如说最经典的来自 Jeffrey Gordon 团队的研究,他们从不同的肥胖程度的双胞胎当中提取肠道微生物,把它们转接到无菌小鼠当中去,发现相关的表型也可以通过肠道菌群的移植进行传递。通过测序发现,他们菌群的组成不一样。
但是目前大部分研究仅限于此,我们并没有办法知道这些不同的菌群是通过什么样的机制导致了宿主的不同的表型。
目前既然知道微生物有可能产生这样的天然产物,那么很有可能这些产物就提供了一个思路,帮助我们理解微生物组与人类健康或者疾病的相关到分子机制的研究。

下面我们稍微转换一下相关的话题,来了解一下自动化合成生物技术与天然产物研究的关系。后面我们会讲为什么微生物组天然产物研究需要用到自动化合成生物技术。
首先,什么是合成生物学?什么是合成生物技术呢?

合成生物学是指,采用工程化的理念和手段来构建具有特定功能的人工生命系统。
它是希望将工业化的标准化、模块化的这样一些理念,包括设计、构建、测试、学习这样工程化的方法,引入到生物学的开发和研究当中去。
举例而言,大家知道青蒿素是抗疟的重要分子。我国科学家屠呦呦先生因为青蒿素的相关研究获得诺贝尔奖。传统而言,青蒿素是通过黄花蒿的种植,通过 18 个月的生产周期,然后进行种植、分离、提纯才能够得到。
但是另一方面,我们可以用合成生物学的方法来构建人工微生物,来生产这一植物天然产物。UC Berkeley 的 Jay Keasling 教授,他将青蒿素合成的生物合成相关基因,导入到人工的酵母当中去,可以实现在工业发酵罐中用人工酵母发酵。在几周的时间内,100 立方的工业发酵罐中,就可以替代 5 万亩的农业种植,展现出这样变革性的、颠覆性的技术。
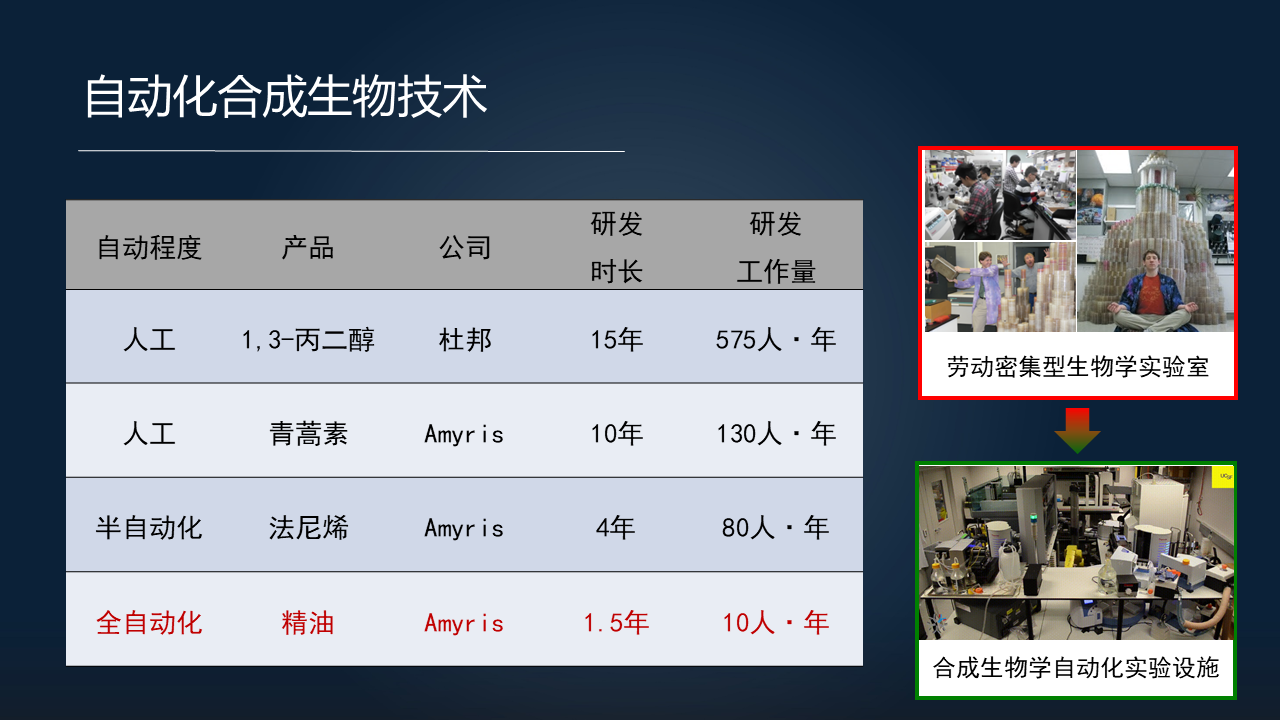
虽然它体现到了这样一个颠覆性的潜力,但目前由于生命体还是过于复杂,我们无法进行理性设计,所以需要通过海量工程试错的方法来进行研究。
在这种情况下,就需要耗费大量的时间、人力和研发经费。比如说,将人工酵母生产青蒿素这一技术进行商业化的 Amyris 公司,对于人工酵母的这样的一个研究花费了 130人/年,就是说,用 13 个人的研究团队研究 10 年时间,才攻克了这一技术难题。
主要的原因,一个是刚才提到的,缺乏理性的设计,需要大量的试错。另一方面,目前的生物学研究还是劳动密集型的,或者小作坊式的。
但如果我们将工程化、自动化、标准化引入到合成生物学研究当中来,用机器人和自动化来做生物实验,就可以大大的加快合成生物学的研究的进程。比如说大家看到屏幕右下角 UCSF 做噬菌体或病毒相关的这样一套全自动的合成生物学实验设施。
Amyris 公司也采用了这样的相关的自动化设施,在他们的研发过程中,大家可以发现在青蒿素以后,其他的天然产物如法尼烯或者植物精油等,研发时长和研发工作量都得到了一个大大的提升,展现了自动化合成生物技术在天然产物生产的过程当中发挥了重要作用。

由于自动化合成生物技术及其相关的工程化平台对于合成生物研究乃至生物研究有重大的促进作用,在 2019 年,来自 8 个国家的 16 个公立的自动化合成生物设施,他们这些研究机构共同发起成立了 Global Biofoundry Alliance——全球合成生物设施联盟。我所在的中国科学院深圳先进技术研究院也是我国的发起单位之一。
这个联盟的建立就是为了促进不同设施之间的合作,通过建立标准、共享技术等等来推动自动化合成生物技术的开发。

这里展示了目前在全球比较具有代表性的自动化合成生物研究平台,包括美国 UIUC、美国的 Gingko、Zymergen、Amyris 等公司,以及英国的帝国理工大学、爱丁堡大学,以及在建的中国中科院深圳先进技术研究院的深圳合成生物研究重大科技基础设施等等。其中标红的是我有在其中参与的两个设施。

首先介绍 UIUC,也就是伊利诺伊大学香槟分校的一套设施。我在 UIUC 赵惠民教授研究组进行博士和博士后研究期间参与设计、搭建、运行和升级了全球学术界首个全自动的合成生物研究平台 iBioFAB,全称是 Illinois Biological Foundry for Advanced Biomanufacturing。
这里有一个视频给大家来看一下。这是我们做的第一代原型机,大家看到屏幕中央的是一个机械手臂,这个机械手臂可以将不同的生物学实验所需要的设备进行连接。
具体来讲,在设计的时候,我们将分子生物学和合成生物学中常用的实验步骤进行拆解,把这些实验步骤与不同的设备进行匹配,把它们放在同一个平台上。另一方面,用机械手臂将标准化的实验材料在不同的设备之间进行穿梭,然后进行柔性的连接,从而完成不同的步骤。
目前看到的是一个 DNA 组装的相关流程,大家看到的 96 孔板,刚才是从冰箱当中将它取出,然后是在密封的储存条件下,通过一个撕膜仪将它上面的膜撕掉,然后机械手臂进一步将这些实验材料以及所需要的实验耗材逐步搬运到自动化液体工作站或者液体操作机器人设备上。
我们看到的像旋转木马的这样一个设备是一个自动化的载架,它可以用来放置不同的自动化实验所需要的实验材料以及耗材等等。
通过中心的计算机控制的系统,我们可以将所有这些实验材料以及耗材的运动路径进行编程,一旦设定之后就可以自动化、高通量的完成相关的实验。
在这个过程中,需要各种各样的设备。大家看到的目前还是这些封膜仪和撕膜仪,但是除此之外,还有我们实验室常用到的 PCR 仪、离心机、酶标仪等等。这些设备当中,最重要的就是大家现在看到的这台叫做液体工作站。
在液体工作站当中,它通过移液机器人可以对 96 孔板当中的样品进行高通量的操作,用 8 通道、96 通道乃至 384 通道。使用液体工作站可以大大提高移液的精度、准确度等等,特别是当我们涉及到需要进行组合优化的时候,这个时候需要对不同板的、不同来源的样品进行混合,这对于我们传统的手工实验或者对于研究者来讲,是很难去进行跟踪和设计的,但是我们通过程序设计是非常方便的,可以用机器人来完成这些动作。
刚才我们提到的更多的是像一个原型机,就是说我们通过搭建全球首台全自动的平台,验证了用机器人平台进行合成生物学研究的可能性。
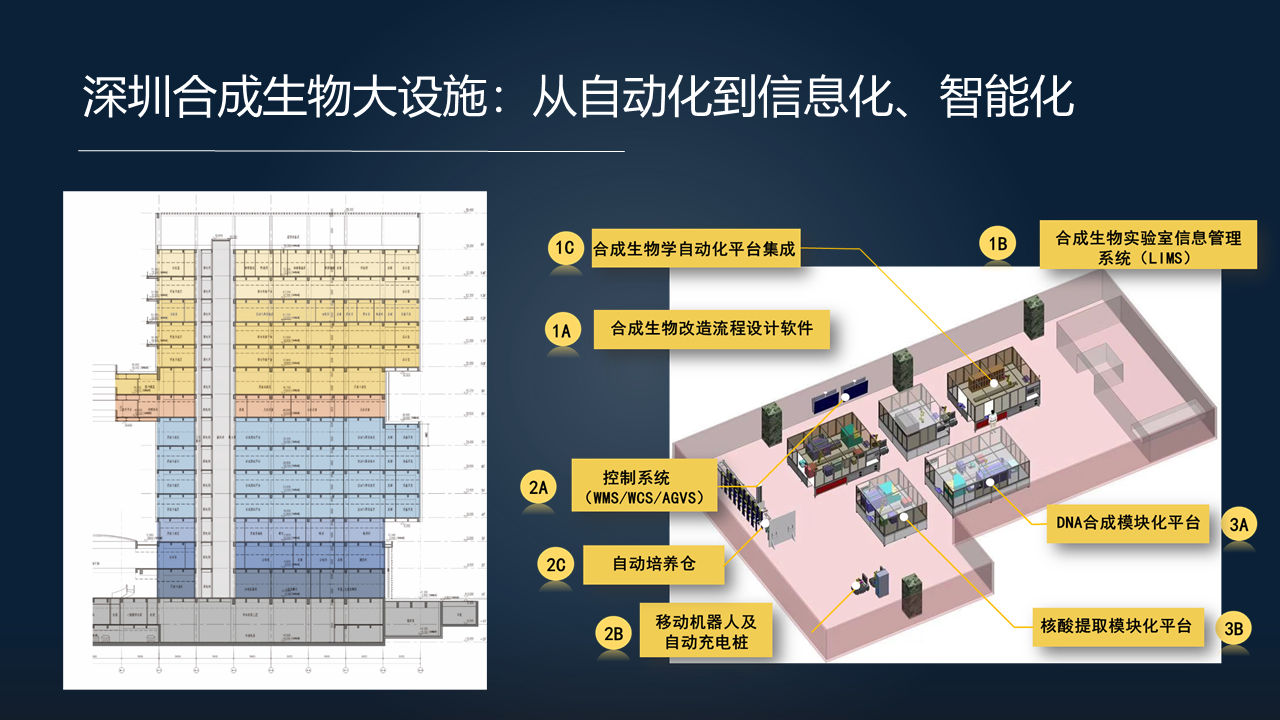
我从去年(2019 年)4 月份回到中国科学院深圳先进技术研究院之后,目前我们正在建造“深圳合成生物研究重大科技基础设施”,或者叫“合成大设施”。我们希望构建下一代的自动化合成生物的技术,不但是引进自动化,而且将工业 4.0 当中的信息化、智能化、云端实验室等等这样的一些新的概念整合进来,进一步加强合成生物学自动化、智能化的研究。
大家目前看到的是一个理想的效果图。刚才视频中看到的那个平台,将会是“合成大设施”这样一个平台当中的一个“功能岛”。
下一部分,我们会将相关的一些常用的用于同一流程的设备,集成在一个功能岛上,这样可以进一步提高研究效率,比如说分子克隆,或者说酵母的操作、细菌的操作,或者细胞的在线测量,或者对于它离线测量的样品准备等等,会有专用的功能岛对于不同的流程进行专门的设计。
另一方面,在这些岛之间,它的物料传输,用人、研究者或者自动化的移动机器人、ATV 小车来进行连接,从而可以将整个流程当中的过程数据以及所产生的标准化的生物数据,进行全流程的控制。
通过物料、信息等等这样的一个自动化的、信息化的综合系统,我们就可以实现云端实验室。研究者将来仅需要在电脑的终端前面输入你相关的人工生命体的设计,后面的构建和测试完全由机器人来开展。然后另一方面,在合成生物学当中不但需要这些功能岛,我们还有相关的测量,比如说光学测量、化学测量、发酵放大等等。
左边这个楼当中,在不同的楼层就会针对不同的生物研究对象进行开展,比如说细菌、酵母或者我们人类肠道的厌氧的非模式细菌等等,包括它的光学平台、质谱平台以及发酵放大平台等等。
整个楼体的设计也充分考虑到了自动化的整合,比如说相关的实验耗材和材料可以在不同楼层之间进行自动化的传输,然后传输到每个楼层之后由自动化的移动机器人进行对接和在不同功能岛之间的分配。
所以我们想,这样的一个大设施将从根本上改变我们对于生物学研究、开发的目前的过程。

在这个过程中,还将指出的一点就是,目前在原型机概念验证的阶段,我们还是采用了标准化或者说常用的商业的设备以及集成方案。但是目前,自动化解决方案主要面对的,是自动化测序或者像临床检测等等这种非常标准化、固定化的流程。
但是合成生物研发更多的是需要有柔性的连接。这主要是基于两个原因,一是它的实验对象多样,另一方面,合成生物学还是一个快速发展的学科,所以不断的有新的仪器设备以及工艺流程需要进行整合。所以我们需要对它进行从底层有深度化的定制。所以在进行工艺流程开发的同时,我们也对仪器设备以及整合的系统进行底层的自主可控的设计,来特殊的满足我们合成生物研究的相关需求。

以上是对自动化合成生物技术的一个简短的介绍。下面我想具体讨论一下,它将如何助力我们研究人类来源微生物活性天然产物。

这是人类来源微生物活性产物研究的一个技术路线,大家可以看到,分为上面和下面两个部分。
一个部分是关注天然的微生物。这需要我们去收集人类相关的样品,然后进行大规模培养。因为我们并不知道每一种菌在实验室当中需要什么样的条件进行培养,所以需要进行一个大规模的筛选。在筛选过后,将相关的产物进行收集、分离和提纯,然后进行活性筛选。
另外一个技术路线是从基因组序列出发。我们现在已经积累了大量的人类微生物组相关的微生物基因组和宏基因组,我们可以通过生物信息预测的方法将相关的通路预测出来,用合成生物学的方法对它进行工程化的改造。改造之后,我们就可以用标准化的异源底盘对它们进行研究。所谓标准化是指我们可以用已经长期进行研究的酿酒酵母、大肠杆菌、链霉菌等等。这样我们就可以用少数的几个标准化的细胞,来对不同来源的通路都进行研究。最后,通过比较代谢组学的方法来找到相关的产物。
这两种技术路线都有自己的优缺点。
对于第一个来讲,我们首先受限于样品,我们需要有实体样品。另一方面,如果是肠道菌的话,它需要厌氧的环境,在实验室条件下可能不生长,或者相关的生物合成基因不表达,导致无法拿到这样一个产物。另一方面,由于我们没有办法提前知道它产生什么样的化合物,所以很有可能会导致化合物的重复发现。
对于第二条路线,从工程化的角度出发,我们可以充分的利用全球科学家所积累的测序数据,然后利用工程化、标准化的细胞底盘,这样就可以进一步的利用自动化、高通量的平台,对上万条的基因进行同时的检测测试。另一方面,我们还可以在研究之前就对它的新颖性进行预测和评价,保证我们可以获得以前没有发现的新的分子。
我们特别是对于第二个路线,基于我们自动化平台进行了一些开发的相关的流程。
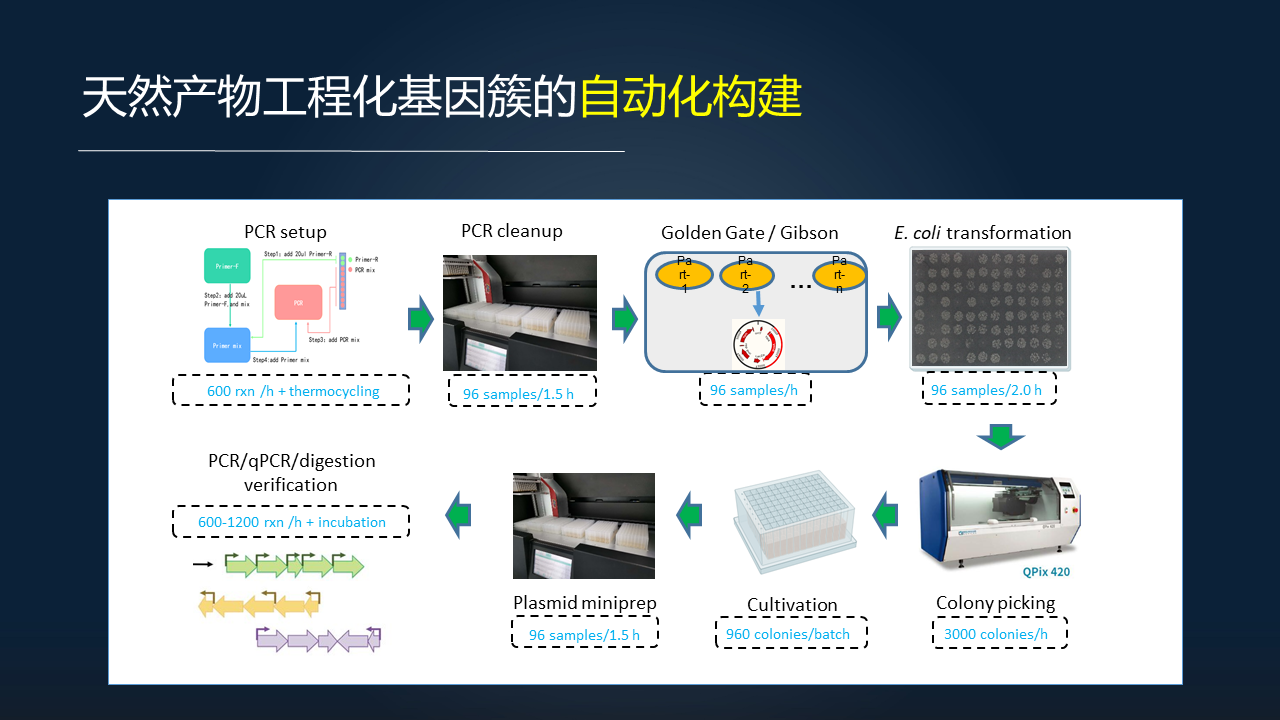
这里举几个例子。
大家目前看到的这个是咱们分子生物学非常熟悉的流程,包括从 PCR 反应的建立开始,然后 PCR 反应的纯化,然后获得了这样的一个基因组装的元件,当然也可以用合成基因片段。然后第二步,用不同的体内或者体外的组装方法,包括 Golden Gate 或者 Gibson Assembly 等方法进行组装,然后用大肠杆菌作为克隆的工具细胞,然后克隆之后通过挑克隆、培养,然后质粒提取等等方法得到这样的组装产物,然后对它进行高通量的验证,从其中得到我们想要的设计好的工程化基因簇。
在每一步,大家可以看到,利用自动化的这样一些设备和平台,与人类相比,对于这样的通量有大概 10~100 倍的提升。目前我们设施还是在建设期间,但是已有的这样一个小的验证性平台已经有了这样一个非常好的通量。在设施建成之后,可能还会再有至少 1~2 个数量级上的提升。
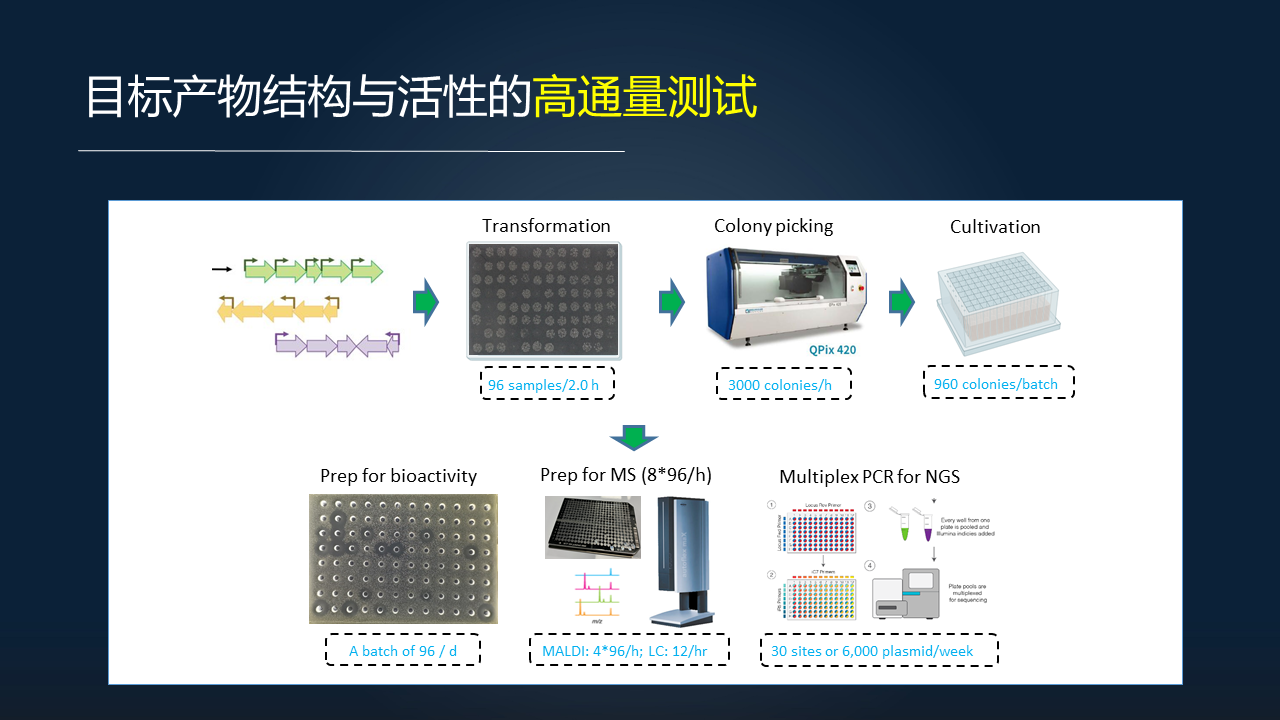
当我们获得了这些工程化的基因簇之后,我们还是可以利用自动化的研究平台,将它们转化到我们常用的工程底盘当中去,包括大肠杆菌、酵母和链霉菌等等,然后对它们进行大规模的培养。
另一方面,我们也开发了这种自动化的样品处理方法,所以可以对相关的基因表达、它的代谢产物以及相关的活性进行高通量自动化的研究,从而加速或者说助力人类微生物组非常复杂体系当中化学的分析和研究。

最后还想讲一点,除了第二个路线之外,我们第一个路线虽然更具挑战,但是同样有它独特的优势。就是说,我们可以拿到相关的菌,它自己本身或者它的产物可以用作后面的医药相关的这样一些应用。所以我们也正在设计这样的自动化的厌氧平台,用于人类肠道微生物培养组的研究。
大家看到的是目前已有的一些例子。在这个过程当中,其实有非常多的工程的难度,因为在厌氧的条件下,包括它相关的操作,包括目前的一些设备,比如说,它如果需要用空气动力的话,它会引入这样的一个含氧的空气,以及如果有一些这种样品传递、设备的维修或者配件的更换,由于在厌氧培养箱当中人手可能很难去进行这样的一个操作,所以我们科学家、工程师一起去想相关的一些解决方案,希望可以构建这样的自动化厌氧平台,从而促进我们人类肠道微生物培养组乃至工程化的这样一些研究。
最后想讲的一点是,我们这样一个大设施实际上对咱们国内外所有的合成生物学研究者以及微生物组相关研究者是完全开放的,所以希望通过这样的一个设施给大家提供一个助力大家各自不同需求的资源。

谢谢大家!



