
大家好,我是来自北京大学人民医院消化科的陈宁。今天想给大家介绍一下炎症性肠病比较新的发病机制——口-肠轴的作用。
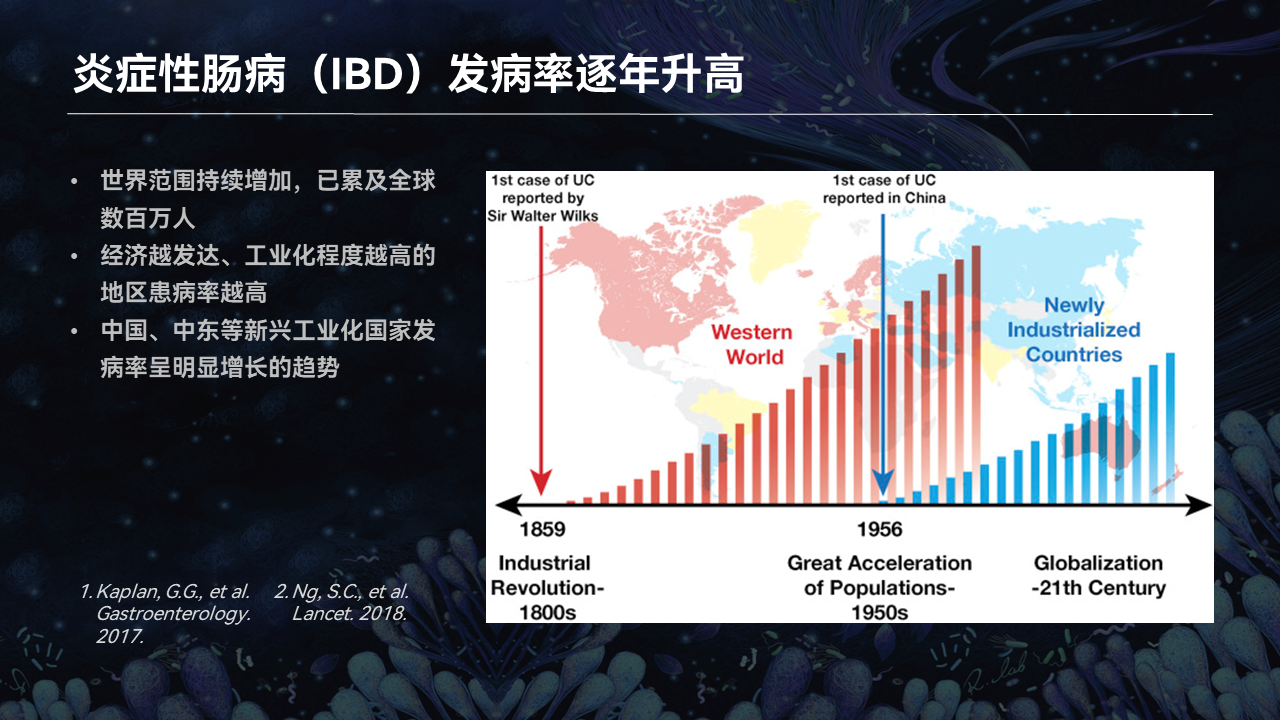
炎症性肠病,简称IBD,我们知道在世界范围内这种疾病的发病率是逐年升高的。在过去,西方经济发达地区的IBD相对发病率要高。近些年,在包括我们国家在内的新兴的发展中国家,IBD发病率也是呈现了迅猛的增长趋势。
为什么会有这种现象?
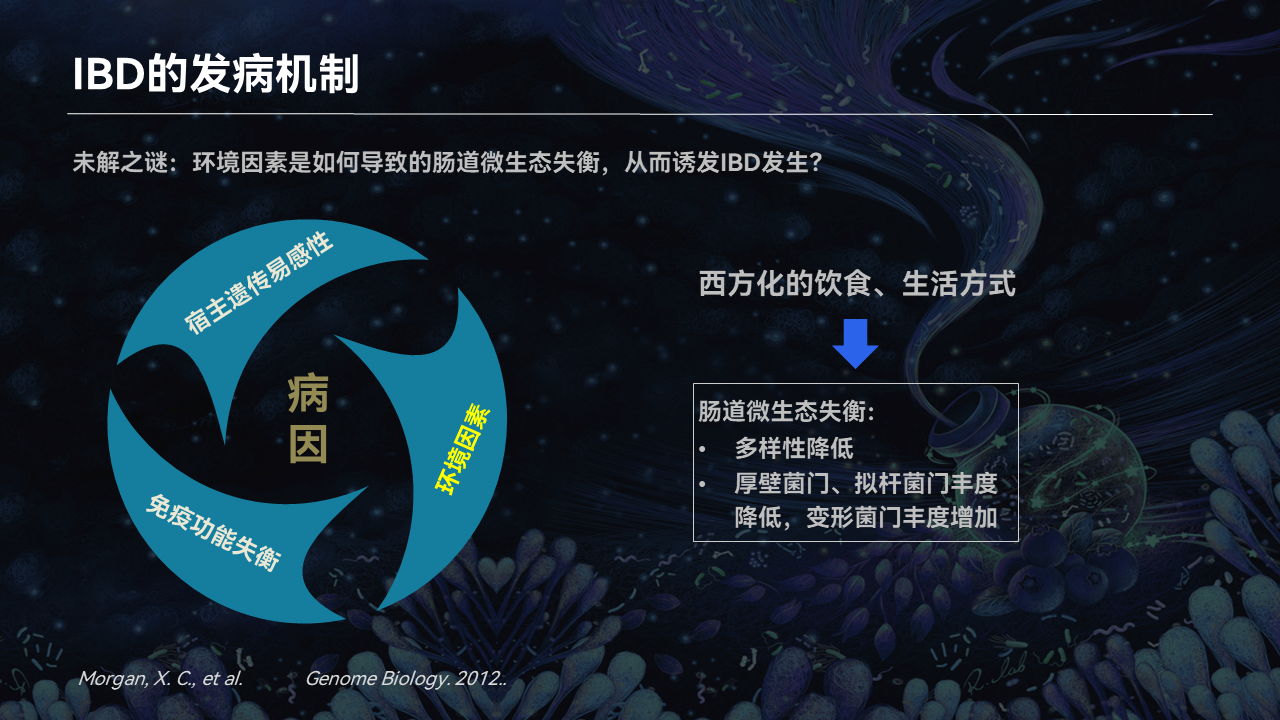
我们知道,炎症性肠病的发病机制到现在为止仍然不十分清楚。但总体上来说,是在具有遗传易感性的个体身上,由于环境因素所导致的免疫失衡,失衡的免疫导致了肠道过度的炎症发生。
尤其是对于像中国,这种过去的发病率很低而现在发病率逐年升高的态势情况下,环境因素在IBD发病当中就占有了非常非常重要的因素。
具体是哪些环境因素?
现在还是认为主要是西方化的饮食,还有我们的生活方式,这些环境因素导致了肠道菌群的失衡。具体可以表现在肠道菌群多样性下降,还有包括像厚壁菌门、拟杆菌门等等的丰度降低,还有一些变形菌门细菌的丰度增加等等。
环境究竟是如何导致了肠道菌群的失衡?
这仍然是我们在研究的IBD发病机制当中的一个未解之谜。

在我和我的团队进行IBD发病机制的研究当中,我们把目光锁定了口腔。
为什么会锁定口腔?
肠道其实从上到下跟外界的空气只有通过口腔和肛门相通,因此我们就认为,口腔应该是连接环境与肠道之间的一个最主要的媒介。
其实胎儿在母体内时,肠道是并不具备有微生态的。随着胎儿离开母体、生产过程当中,到新生儿产生跟外界的环境相沟通,再到2~3岁,这才是肠道微生态逐步所建立的过程。
具体的建立过程其实就是通过口腔到肠道途径,包括像埃希氏菌、链球菌,这些叫做兼性厌氧菌,这些菌通过口腔到达了肠道,并实现了永久的定植。这是肠道微生态在婴幼儿时期所建立的最主要的过程。
基本上在3~5岁之后,人体的肠道微生态就趋于一个比较稳定,已经建立的比较成熟的过程了。但是后续即使是到了成年人,其实外界的环境仍然会通过口腔来对肠道产生各种影响。比如说经过食物或者是跟唾液所相混淆在内的外来的病原微生物,就可以通过口腔进入到肠道,也可以进一步地去影响肠道微生态的动态更替的过程。
除此之外,口腔其实是消化道的广义的起始部分,所以口腔黏膜的情况在一定程度上也可以反映肠道炎症的情况。另外口腔局部微环境的异常,比如说最常见的牙周炎,也可以促进肠道炎症的发生。
基于此,我们在关于IBD,尤其是环境因素又怎么样去影响IBD的发生当中,锁定了口-肠轴这样的新兴的发展方向。

下面就给大家介绍一下,我和我的团队以及国际上一些其他的研究团队,最新的关于口-肠轴在IBD当中的作用机制的研究。

2015-2016年,我们就关注到了口腔有可能会参与到IBD的发病当中。
我们发现,IBD患者唾液的菌群跟健康人的唾液菌群之间存在着很多差异,包括物种多样性的降低,在某一些特定菌的丰度上的改变,以及这些细菌的功能都会存在着很多的异常。
后面我们还经过进一步的分析,发现了一系列的IBD相关的口腔菌种的指示菌种。在对于IBD患者进行有效的治疗之后,过了3个月我们再去复测这些IBD患者的唾液菌群就会发现,这些IBD相关的口腔菌种的指示菌种,更趋向于健康人的指示菌种。
我们发现的这个现象提示的作用很大,比如说口腔是个取材很方便的地方,跟IBD所受累的器官结肠相比起来。我们知道做结肠镜检查相对还是一个比较痛苦的过程,而口腔的微生态比肠道的微生态,相对稳定性还是要更好。
因此当时我们就觉得这个领域大有前景,未来说不定IBD的无创标记物,就有可能从口腔的取材当中所进行。

我们所发现的这些IBD患者口腔微生物群的变化,它到底是IBD引发的系统炎症导致的一个继发的在口腔的改变,还是说具有更为积极主动的作用,它本身就导致了IBD的进一步的促进作用呢?
我们知道口腔是消化道的一个“门户”,外来的微生物都是通过口腔到达肠道,来去影响肠道的多样性。因此我们认为,口腔微生态有可能更为积极主动地去参与了IBD的发病。
2018年的时候就有国际上的学者提出来这个观点,口腔微生态可能具有潜在致病菌发挥“蓄水池”的作用,就像右边的这张图。作为上游的口腔,它源源不断地把这些潜在的致病菌,经过消化道或者其他途径到达肠道,从而促进了肠道的各种致病作用。
这种“蓄水池”的功能不仅仅是在IBD身上,其实在结肠癌,包括肝硬化在内的许多系统疾病,都会发现肠道菌群的异常来自于口腔菌群的异常。
但是这只是从系统进化树的发育领域当中所推测出来的,并没有直接的证据表明口腔的微生物真正能够到达肠道。
从这个理论上来说,所谓的“病从口入”是真正的实现了,而更实际上是口腔菌从口入,从而导致了系统性疾病,包括IBD的发生。
【可能机制】异位定植
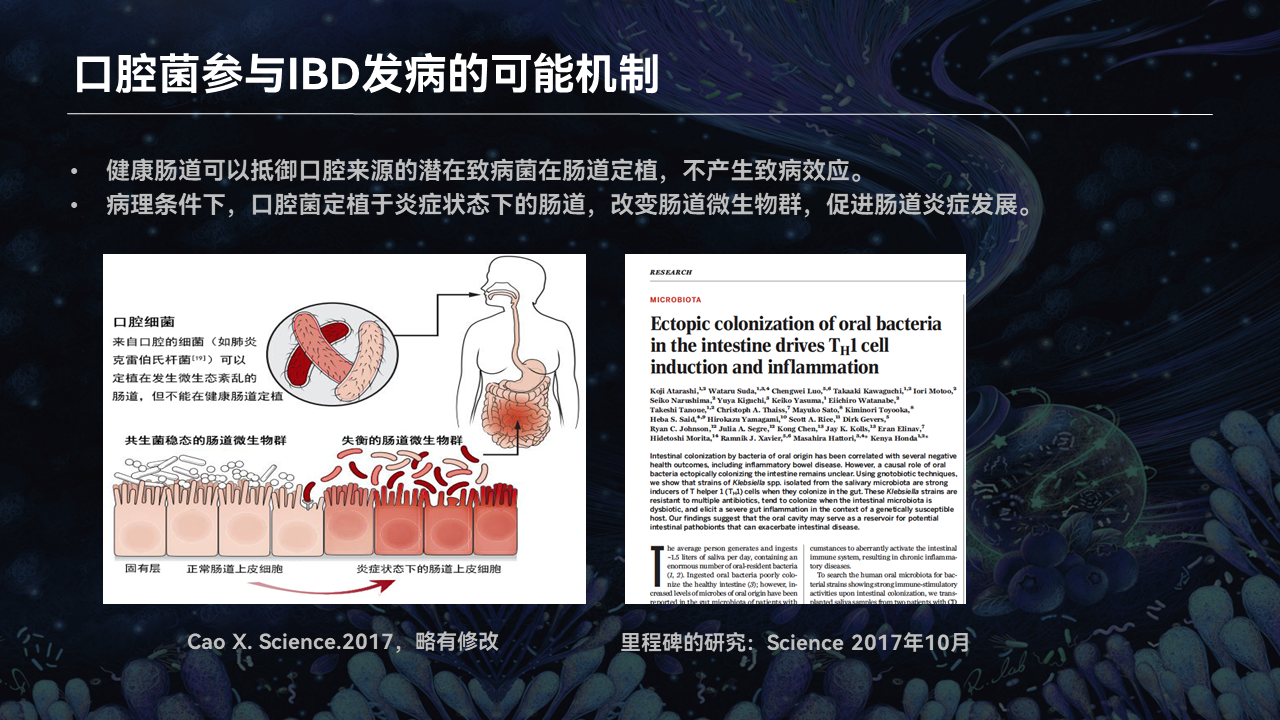
2017年,《Science》杂志上有一个很著名的综述提出了口腔菌参与IBD发病的可能的机制假说,就是图中所显示的。
在健康的情况下,我们的肠道是健康的,所以潜在的这些来自于口腔的致病菌,它们并不是那么容易在肠道发生定植,从而它们不产生致病作用。
在病理条件之下,首先肠道的上皮屏障功能或者是本身的炎症,导致的口腔来源的这些菌很容易在肠腔当中定植,从而对肠道的微生态产生影响,进一步加重炎症的产生。
虽然这是假说,并没有直接的证据,但是学者们纷纷在这个方面去进行努力。

在2017年《Science》的同一篇期刊上,就有一个里程碑式的研究,具体给大家看一下。
这是来自于西班牙的团队,在无菌条件之下,他们将IBD患者的唾液给无菌小鼠进行灌胃。饲养6周之后,从小鼠的粪便当中分离出来了8种不同的菌,其中的一种克雷白杆菌的菌种再进一步喂养给IL-10消除的转基因小鼠。
我们知道这种转基因小鼠是有自发性结肠炎的倾向的。经过喂养之后发现,克雷白杆菌加重了小鼠的结肠炎。
这个研究本身设计不难,但是它所带来的意义特别的大。也就是说头一次人类证实到了,口腔来源的菌是能够直接地通过消化道,在肠道发生所谓的异位定植,从而给口腔菌很积极主动地参与IBD发病这个理论奠定了基础。
【潜在致病菌】变异链球菌
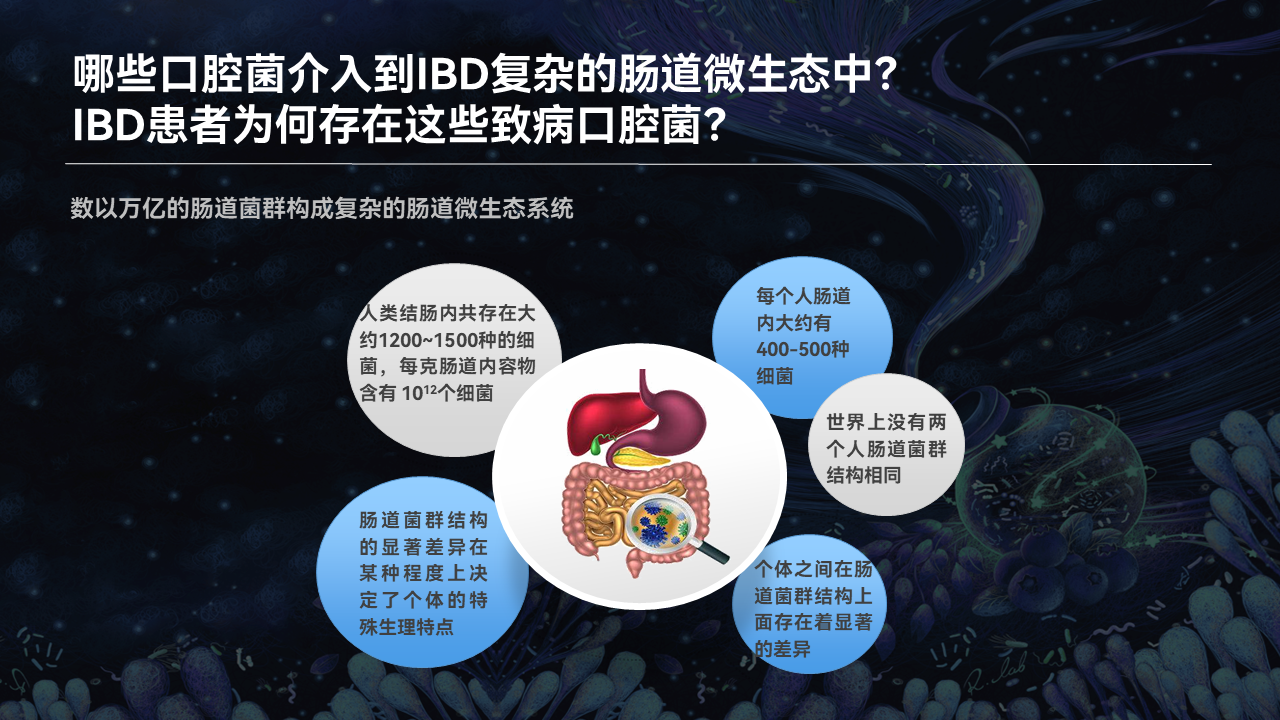
我们知道,肠道是存在着有数以千万计、亿万计的菌群,没有两个人的肠道菌群构成是完全一样的,菌群的多样性代表了人体的各种生理病理的功能。肯定不仅仅只有《Science》这篇文章当中所提到的克雷白杆菌能够发生异位定植,参与到肠道菌群的失衡。
但是对于IBD这么复杂的肠道微生态,究竟有哪些口腔的潜在致病菌介入到了这个过程当中?而且IBD的患者为什么会存在着这些潜在的口腔致病菌?这些仍然是我们没有从《Science》这篇文献当中所得到的答案。

也是鉴于此,我和我的团队又在这个方面进行了进一步的研究。
我们知道,其实口腔也是IBD最常见的一个肠外受累器官。有文献报道,甚至高达80%的IBD患者都在一定程度上存在着口腔病损,包括口腔溃疡或牙周炎等等。而且口腔病损的状态跟IBD的病情是平行的关系,IBD的病情缓解,口腔的状态就会更好。
在2020年的《Cell》还有一篇文章,提示IBD的患者和牙周炎之间有相互促进的作用。IBD严重程度重,牙周炎就会更重;牙周炎更重的时候,IBD的病情也会更重。

所以我们再进一步去研究口腔菌的时候,就把目光锁定到跟牙周炎和龋齿特别息息相关的一种菌,就是口腔变异链球菌。
其实前期的研究当中,我们就已经发现IBD患者的唾液当中,口腔变异链球菌的丰度和功能跟健康人群之间是有很大差异的。
我们进一步从59名IBD患者的唾液当中进行分离,最终分离出来了有30株变异链球菌的菌株。经过全基因组的测序,再去进一步从系统进化树的分类上面去进行聚类发现,这些菌群主要集中在3个大的分支上。
我们把分离得到的这些变异链球菌,进一步在体内和体外进行了关于肠道方面的一些研究。比如说,我们发现它在体外能够促进肠上皮细胞炎症的作用。
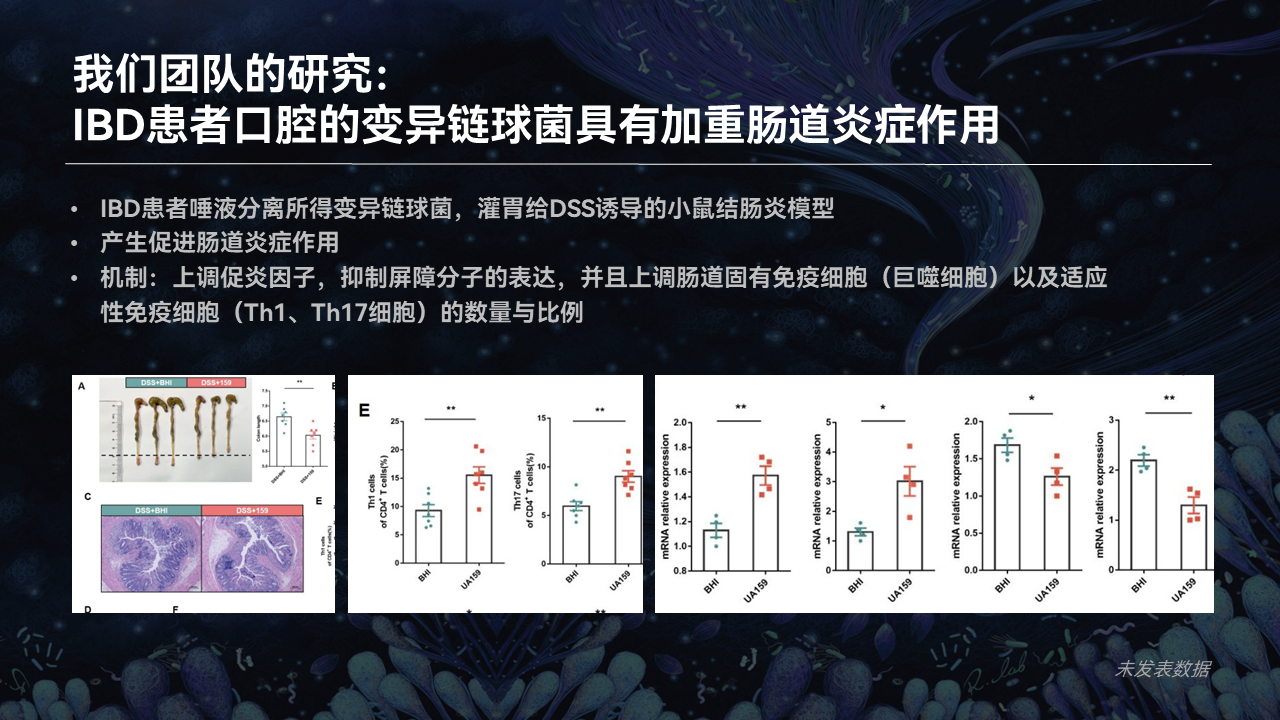
我们所分离得出来的这些变异链球菌,进一步在小鼠体内进行了对IBD促进肠道炎症的验证。
结果果然如我们所料,这些来自于IBD患者口腔当中的变异链球菌,具有促进小鼠IBD肠道炎症的作用。具体的机制涉及到了上调促炎的细胞因子,下调屏障功能的因子,还有促进一些适应性免疫细胞,包括Th1、Th17的表达等等。
【可能途径1】唾液外泌体
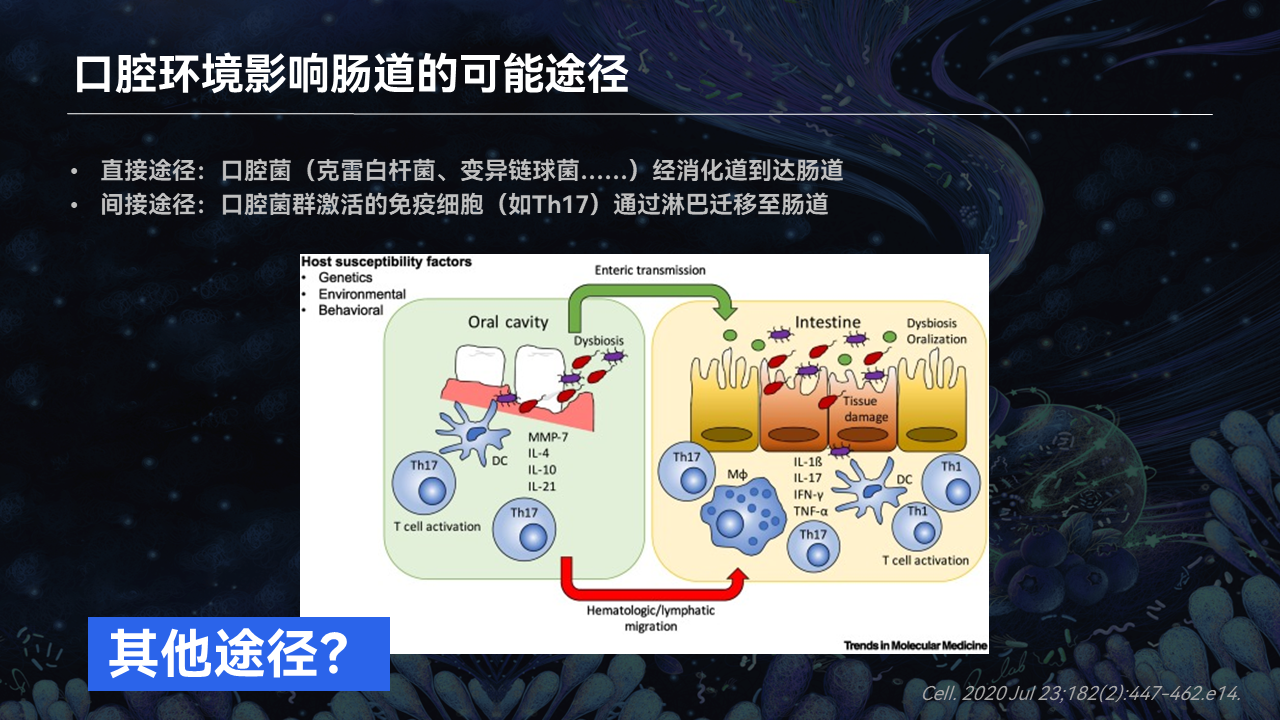
至此我们就知道,口腔的环境可以影响肠道,通过的途径有可能是通过口腔来源的菌,包括《Science》文献当中所提到的克雷白杆菌,也包括我们自己研究当中的变异链球菌等等。
除此之外,在2020年的《Cell》这篇文章当中也提到了,他们通过口腔菌所激活的免疫细胞Th17发现,这样的细胞可以通过淋巴迁移途径到达肠道,从而达到促进肠道炎症的作用。

除了直接途径和间接途径,我们在口-肠轴的研究,是不是还有其他的可能性?
口腔当中其实除了口腔的微生态以外,也还有其他的物质存在的,比如说外泌体。
外泌体是存在非常广泛的一类微小的囊泡,它当中可以包括有蛋白质,有miRNA、脂质等等一系列的物质。外泌体具有很好的稳定性,它的外膜非常的稳定,能够保证在机体之间进行一个长距离的传输。
其实目前关于外泌体的研究重点是在基于液体活检这一概念,可能在很多局部的或者系统的疾病当中,都具有潜在的检测的应用前景。
唾液本身也是存在外泌体的,而且唾液的取材又非常的方便。所以也有初步的研究提示,唾液外泌体有可能是作为系统性疾病的检测试剂盒。比如说胰腺癌,比如说干燥综合征,都有研究团队提示唾液外泌体可能会具有一定的提示作用。

我们的团队也是在这一方面做了一些工作,我们在2017年的时候发表了一篇文献。从活动期的IBD患者唾液当中所分离出来的唾液外泌体,跟健康人群相对比发现,这其中含有8种非常特异的蛋白,这些蛋白在健康人的唾液外泌体当中表达量是0。
基于此,我们开发了辅助诊断IBD的唾液试剂盒,而这个试剂盒也获得了国家发明专利。它最大的优势就是在于,基于唾液的检测,无创而且比较稳定。
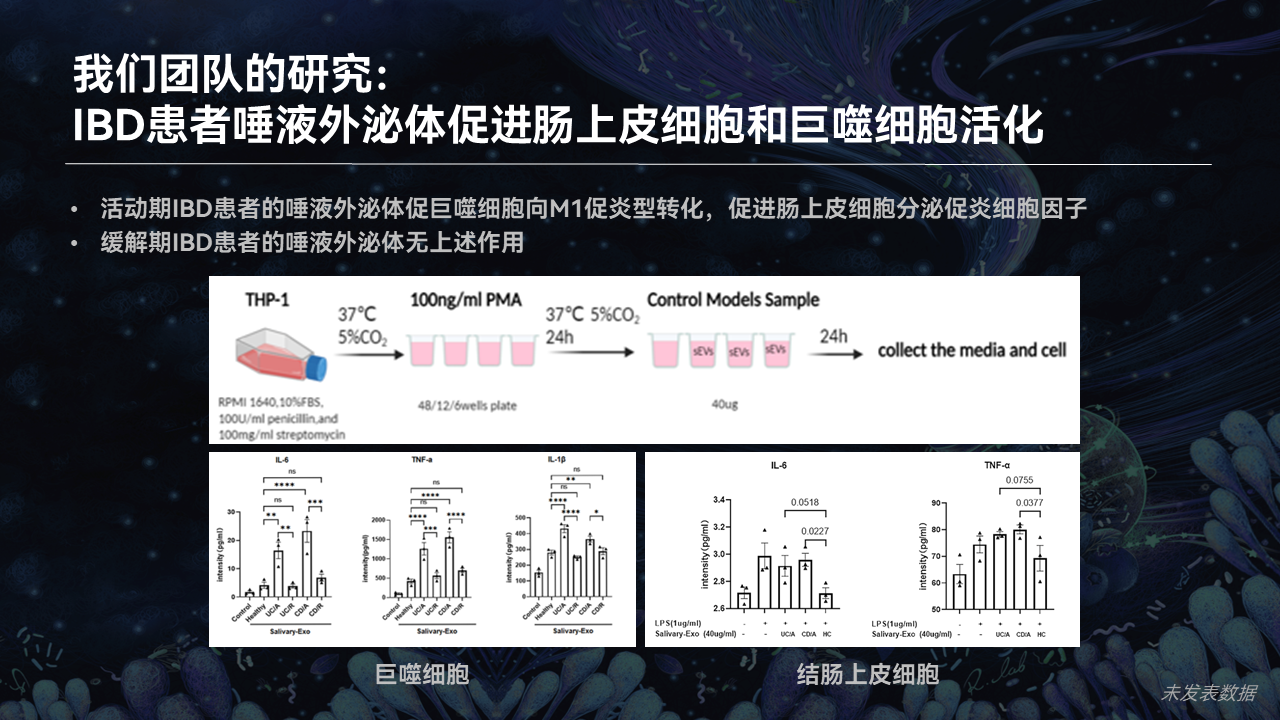
在此基础之上,我们又进一步去拓展了IBD患者唾液外泌体对IBD发病机制的一些影响。
我们发现在体外这些来自于活动期IBD患者的唾液外泌体,它能够促进肠上皮细胞的促炎作用,它能够使巨噬细胞向M1促炎型转化;而来自于缓解期的IBD患者的唾液,就没有这种作用。所以这是非常神奇的一件事情。
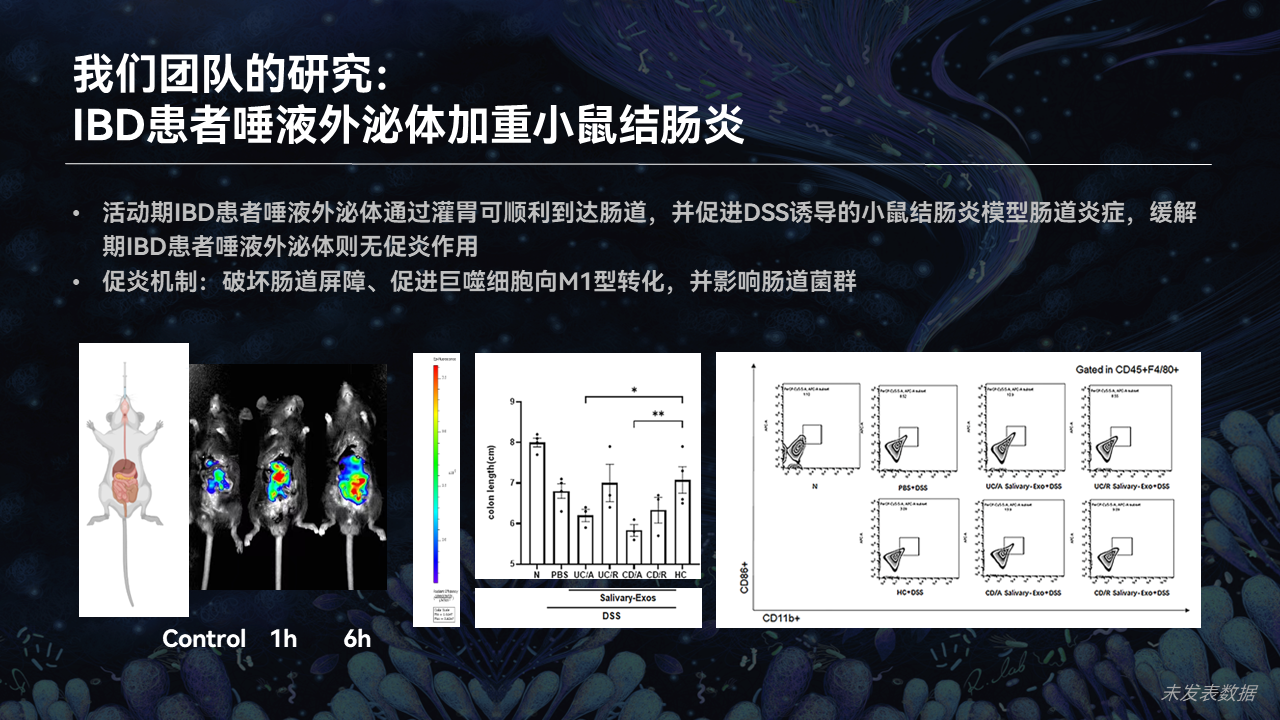
我们进一步把这些来自于IBD患者的唾液外泌体,在体内给小鼠去进行喂养。一方面发现,果不其然外泌体非常的稳定,它能够逃脱小鼠的胃酸、逃脱小鼠的肠液等等消化酶,能够完好无损地到达肠道。另外一方面,它到达肠道之后,可以促进小鼠的IBD的肠道炎症。
具体的机制也涉及到了巨噬细胞的转化,也涉及到了对肠道菌群的影响。
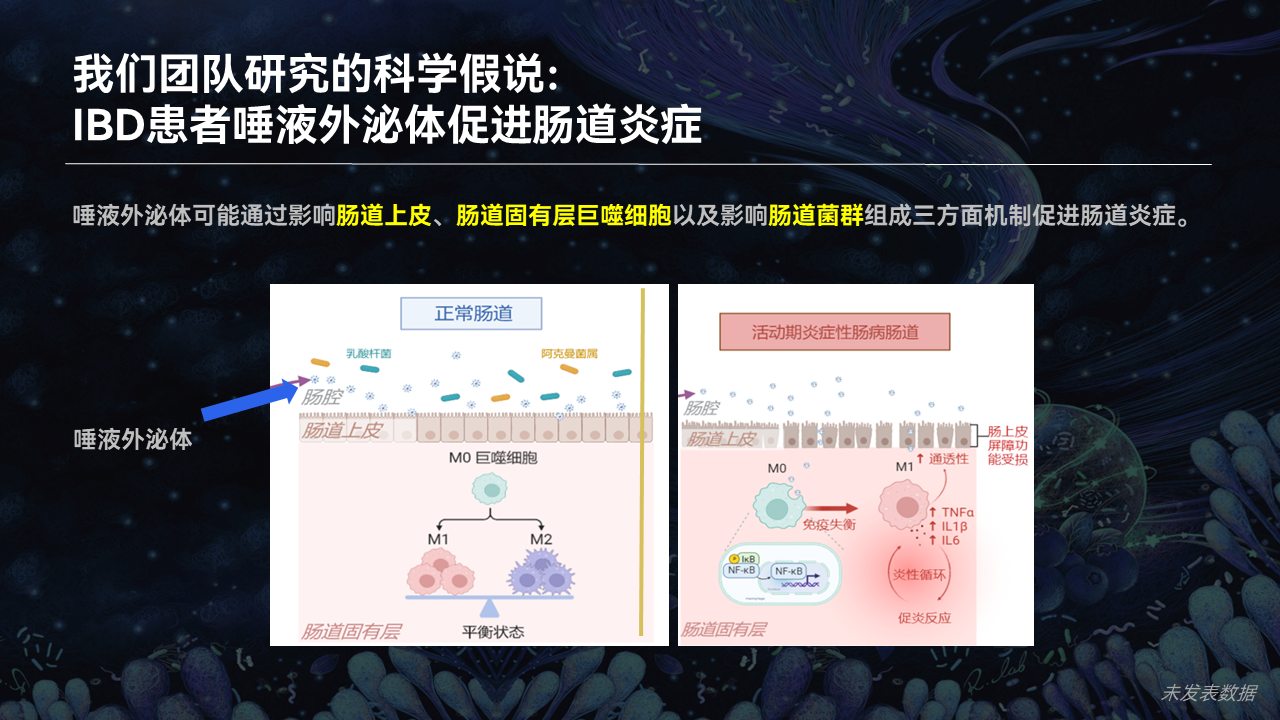
基于上面的研究,我们进行了如下的假说。
来自于患者的唾液外泌体在相对健康的肠道,并不能够对肠道产生任何的不好的影响。但是如果本身肠道就存在着炎症,或者肠道上皮屏障功能存在着一定的障碍,这些唾液外泌体到达了肠道的表面,通过肠道上皮到达固有层,与巨噬细胞进行作用,并同时对肠道菌群功能产生影响,最终导致了肠道炎症的加重。
这有可能就解释了,为什么IBD患者持续地发生肠道炎症,并反复迁延、持久不愈。
【可能途径2】口腔微环境
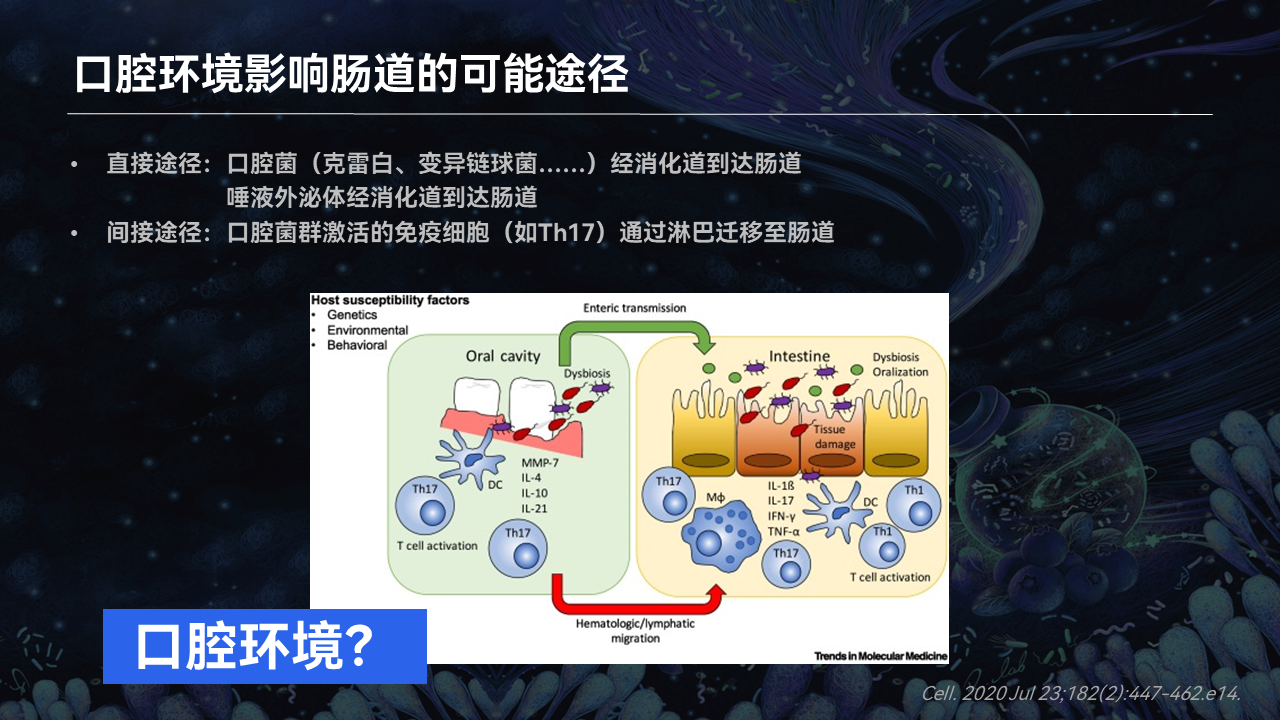
我们知道,口腔当中唾液每天的含量是非常高的,每天人可能要吞到1.5升的液体。这些唾液所裹挟的大量的唾液外泌体,很有可能就是IBD发病、迁延不愈的一个关键的因子。
至此,我们现在知道了口腔可以通过口腔菌,可以通过可能的唾液外泌体,也可能通过所激活的免疫细胞,导致肠道的各种炎症的发生。
那么我们还有一些事情没有解决,就是到底什么原因导致了口腔会发生这些异常,从而去影响肠道?口腔微环境到底是怎么样变的异常的?什么状态的口腔微环境会对IBD的肠道产生影响?
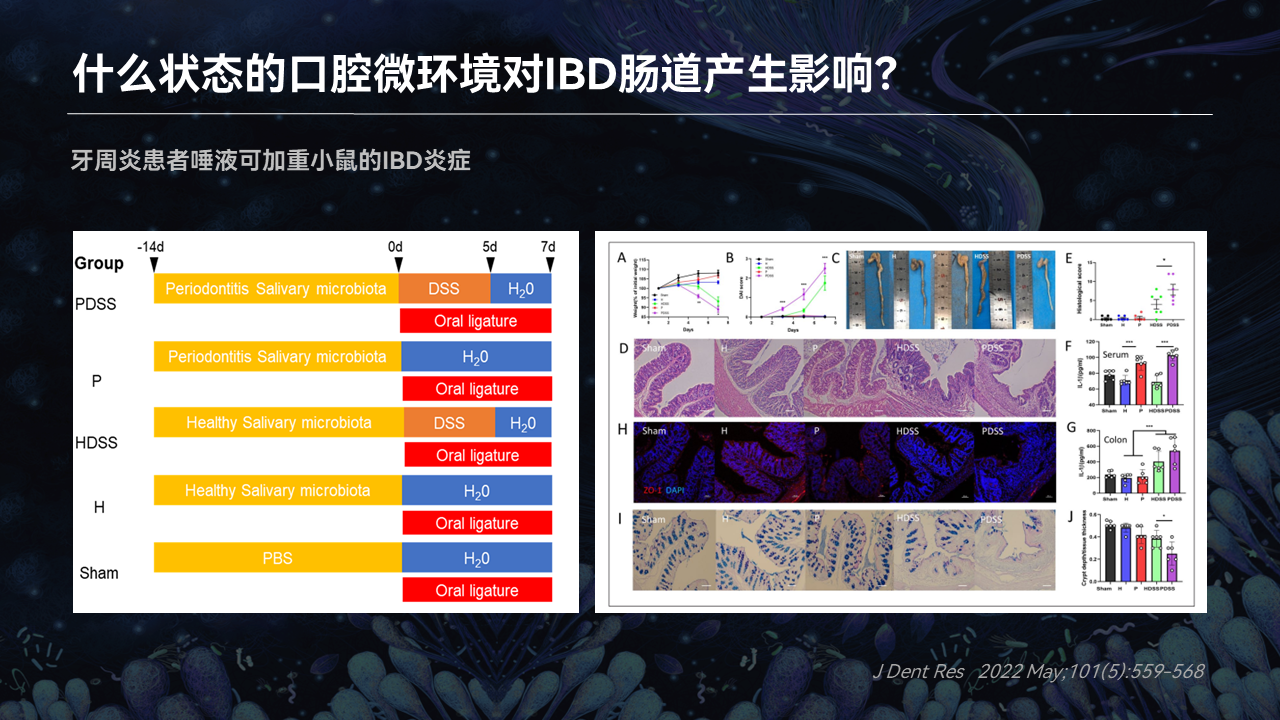
在2022年的时候,JDR杂志有一篇文章发现,牙周炎患者的唾液就可以加重小鼠的肠道炎症。这也跟我们刚才所提到的牙周炎和IBD之间相互促进,是进行了一个印证。
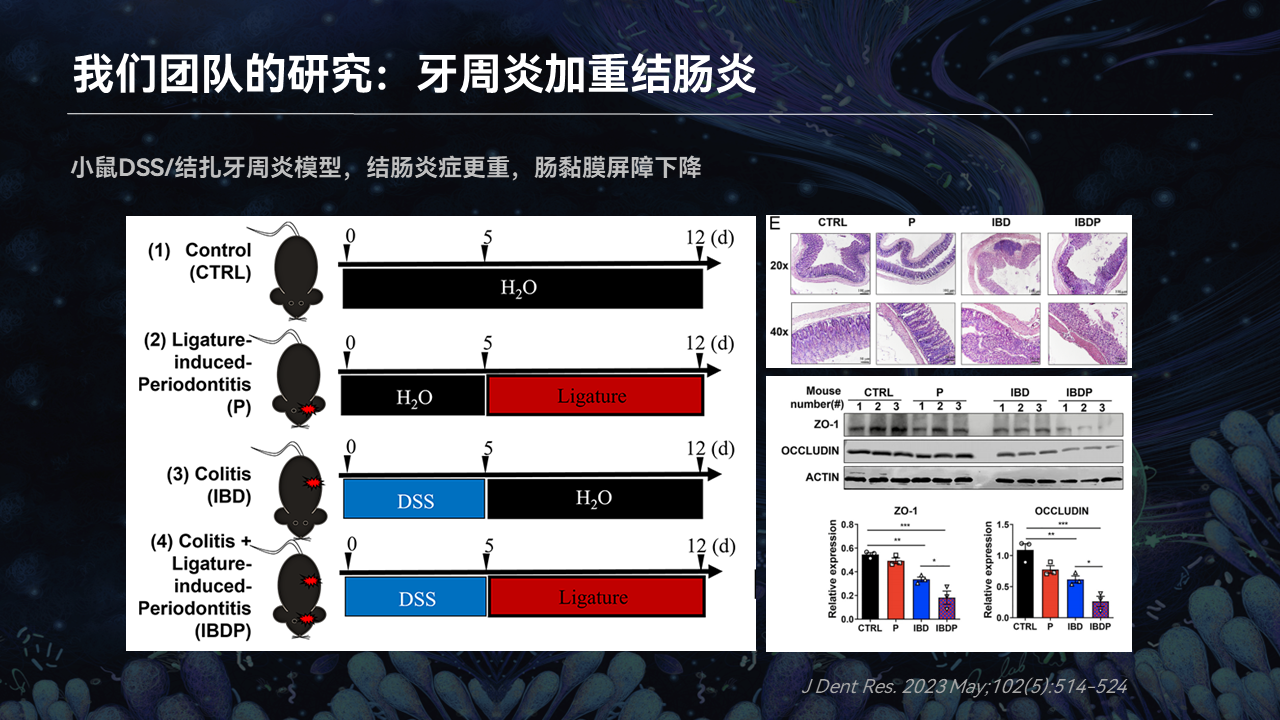
我们在这个基础之上,又进一步去观察了牙周炎到底怎么样去加重了结肠炎。
我们设定了既有IBD又有牙周炎的双重的小鼠模型,一方面我们发现这样的模型当中结肠炎的表型,确实是要比单纯的IBD的小鼠模型的炎症要更为重。
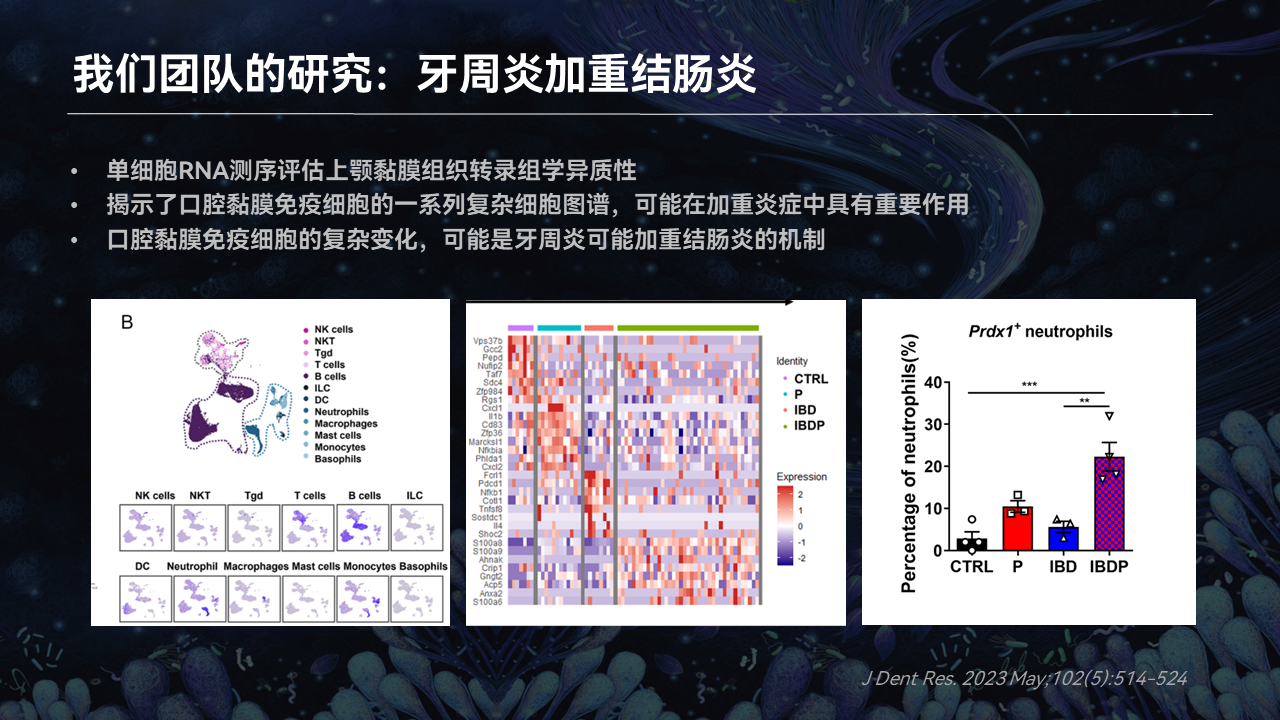
同时,我们对上颚黏膜组织的单细胞测序也发现,存在着又有IBD又有牙周炎的这部分小鼠,它们的口腔黏膜免疫会有一系列非常复杂的细胞图谱。
通过单细胞测序,我们测定到了一共有12种细胞亚群,这里面涉及到了不同的巨噬细胞、中性粒细胞等等免疫细胞的异常。而正是由于这些复杂异常的免疫细胞的变化,可能就是导致牙周炎最终加重IBD的原因。

我们的这个研究很荣幸在2023年的5月份刊登在了口腔的顶级期刊JDR杂志上,而且是作为封面期刊所报道的。
我们根据假说,画了一个卡通图。上游的话就是像大坝一样,上游就是口腔。口腔跟肠道之间是有一个坝存在的,这里边的很多不好的免疫激活细胞,其实在正常情况下是不能够到达肠道,也就是下游的。
由于种种原因,口腔的微环境导致了各种炎性的细胞因子,包括免疫细胞失衡的异常。它们就通过了大坝,最终导致了肠道炎症的发生,也就是在下游起到了不好的作用。
小结来说,通过我们自己的团队以及国际上其他的一些专家团队,对口-肠轴这个领域的研究,我们发现:
一方面,口腔当中有一些潜在的致病菌,比如说克雷白杆菌,比如说变异链球菌,它们会直接到达肠道,引起肠道炎症。
第二个方面,唾液外泌体可能会源源不断地随着唾液到达肠道,起到促进肠道炎症的作用。
同时由于口腔微环境的异常,比如说牙周炎的持续发生,所激活的局部口腔的免疫细胞也可以到达肠道,导致肠道炎症加重。
我们的这一个研究,一方面丰富了IBD发病机制,同时由于基于的是口腔或者唾液这样的发病领域。唾液也好口腔微生态也好,它可以作为一个非常有前景的辅助我们诊断IBD的试剂盒,因为它的无创性,以及它的短期内多次重复性。
最后也可能是这样的新的发病领域,未来会指引我们在针对口腔微环境异常方面,去进行一个潜在的治疗靶点的开发。

我们上面的这些研究也得到了包括国家自然基金、科学基金等等一系列的基金资助。
我们的研究团队除了北京大学人民医院消化内科,还有北京大学口腔医院微生物实验室、北京大学基础医学院免疫系,还有北京大学精准医疗多组学研究中心。

这就是我今天给大家介绍的内容。谢谢!


