
大家好,我是来自江南大学附属医院,也是来自江南大学无锡医学院的张烽。那么我今天跟大家分享的题目是《从肠道菌群角度重新去认识生物利用度》。

生物利用度,我们可以理解为,日常的食物或者药物中的活性成分被机体吸收的速度和比例。
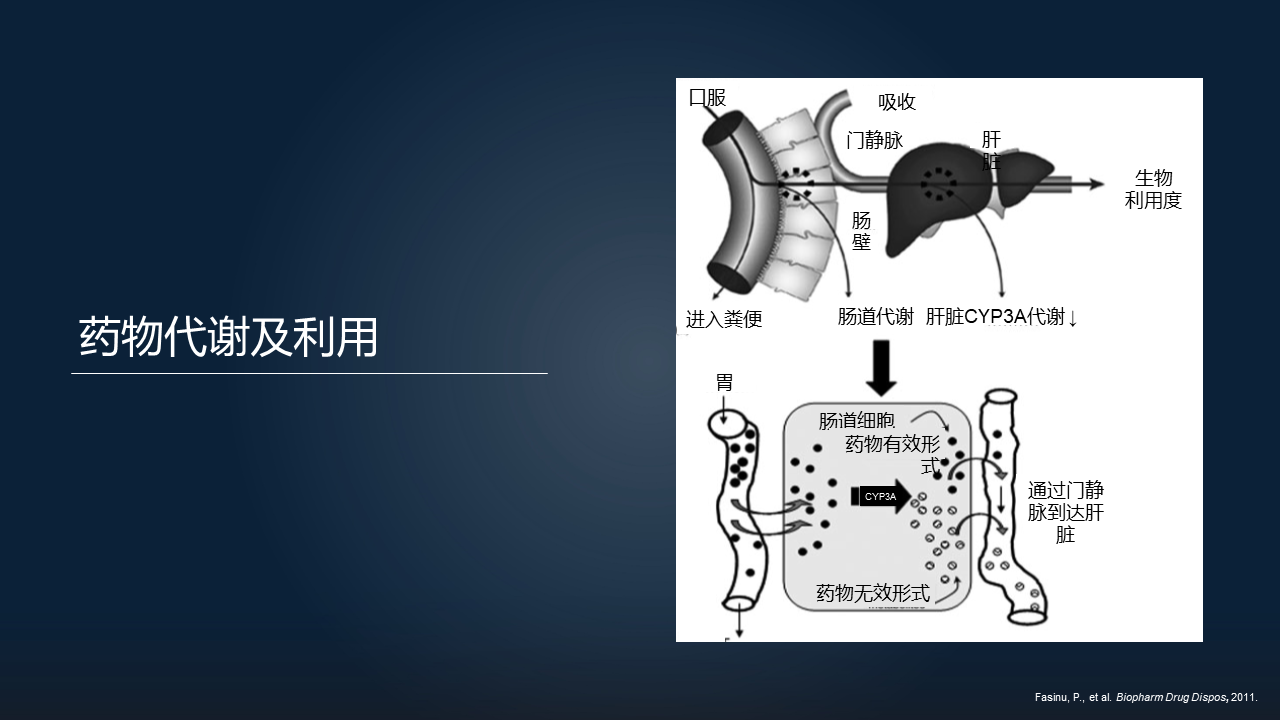
以药物为例,我们口服药物以后,有一部分药物就通过胃肠道,最后进入粪便排出体外。
大部分的药物经过肠道的代谢和肠肝循环,在肝脏里有一部分被细胞色素酶 P450 所降解,在肠道里面也有一些药物被 P450 所降解。那么药物在肝脏和肠道的这种被降解的过程,我们称之为首过消除效应。
剩下的这些到达循环系统、发挥生物学作用的这些药物占口服药物的比例,我们称之为生物利用度。

影响生物利用度的主要有两个方面,一个是胃肠道本身的生理状况,还有一个是食物或者药物本身的理化性质。
在我们胃肠道里面,主要是食物或者药物的溶解度,如果比较低、不达标的话,会影响或者降低生物利用度。另一方面,如果它们在胃肠液中化学稳定性比较低、比较差的话,也会降低生物利用度。此外,还有肠屏障的通透性降低也会有影响。
那么最最重要的一点就是刚刚说到的,肠道和肝脏里面的首过消除效应,如果太强的话,也会降低生物利用度。
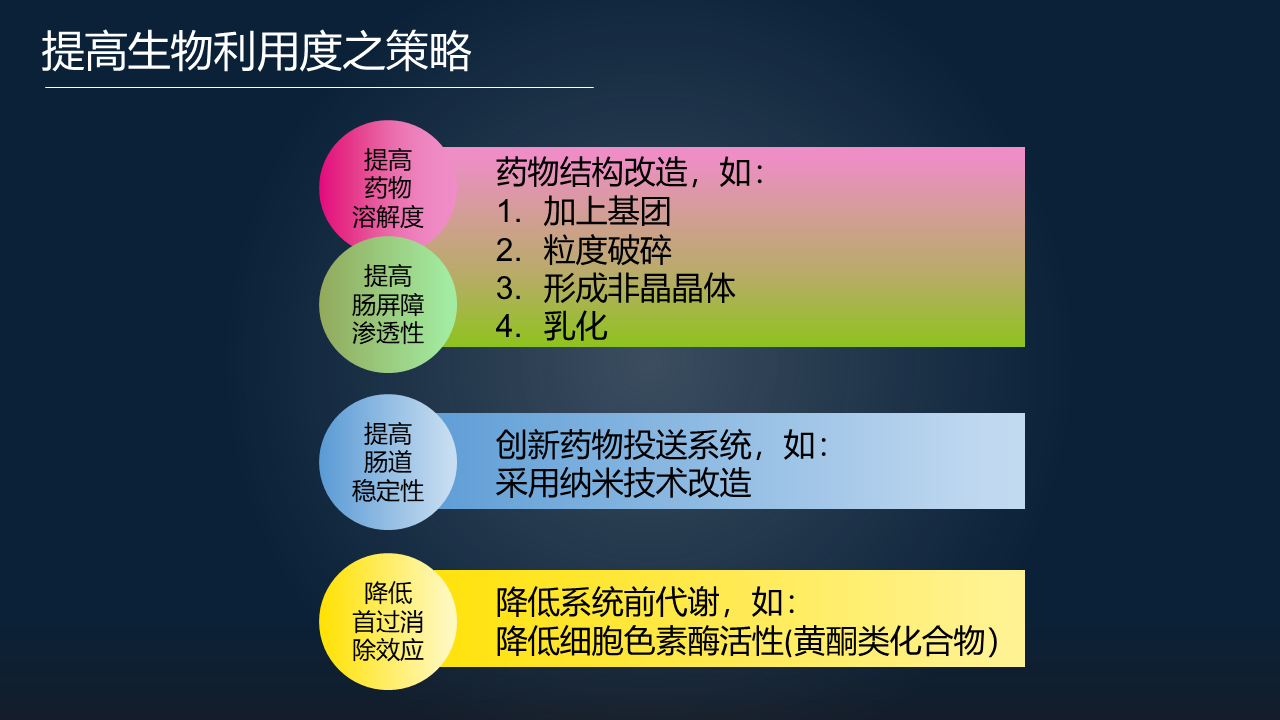
目前一般来说,经典的提高生物利用度的策略有以下几个方面。
如果我们想提高药物的溶解度或者肠屏障的渗透性,可以对药物结构进行改造。比如说,我们可以在药物上加一些基团,可以对药物的粒度进行破碎,使药物形成非晶的晶体,或者进行一些乳化的作用。
如果想提高药物在肠道的稳定性,我们可以通过对药物的投送系统进行改造。比如,现在有比较多的文献去采用一种纳米技术,改造药物的投送系统。
另外,如果想降低首过消除效应,我们也有一些办法,比如说可以用黄酮类的化合物去降低细胞色素酶活性。

但是在中药领域有一个比较特殊的现象,就是说我们有很多中药的疗效是很确定的,甚至说是一个很强的作用,但是你去检测血液中药物的浓度的话,会发现浓度很低或者甚至于完全检测不到。
也就是说,它有一个很好的疗效,但是有一个很低的生物利用度。那么这是为什么呢?这个引起了我们极大的兴趣。
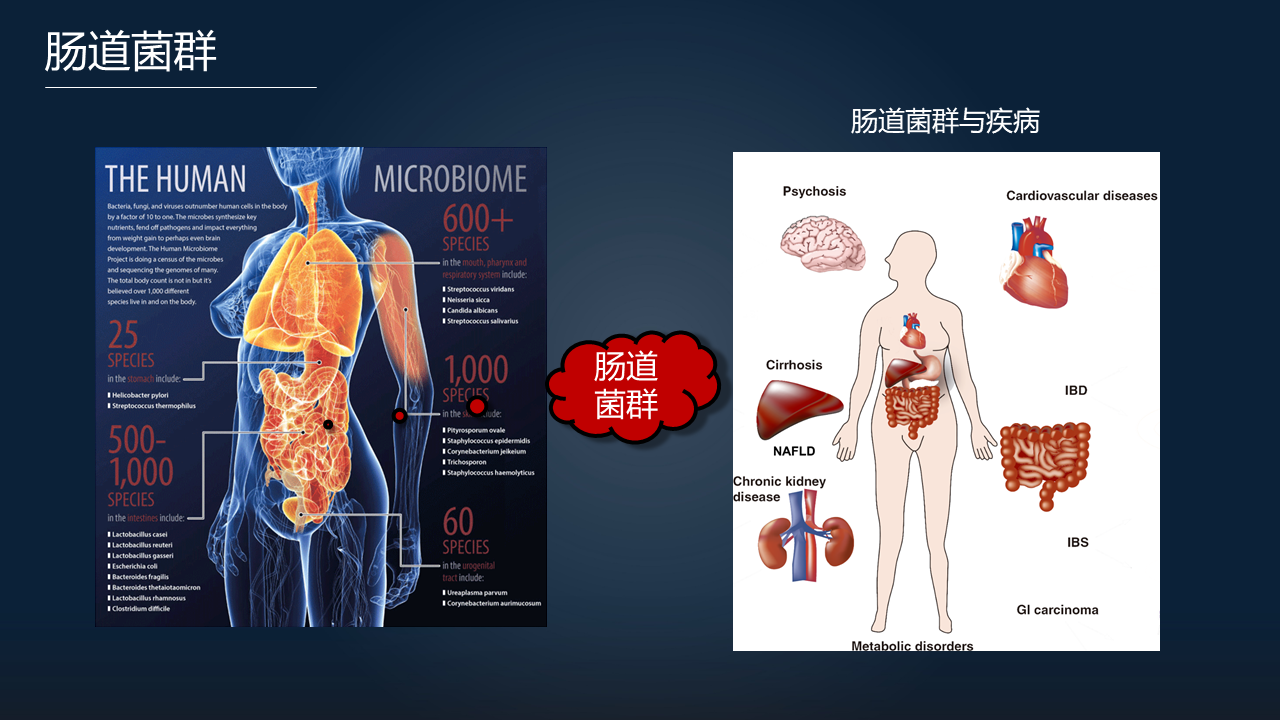
近年来,在肠道菌群领域的一系列进展,就为解释前面说到的这一种矛盾的、不一致的现象,提供了一些可能。
我们都知道人体积聚了大量的共生微生物。在肠道里面共生的这些微生物,我们称之为肠道菌群。它的种类有 500~1000 种,它跟我们人体的健康和疾病有着密切的联系,尤其是研究比较多的,是集中在肠道菌群和代谢性疾病方面。

我在博士期间在导师赵立平教授的指导下,完成了一项通过高膳食纤维的饮食对 2 型糖尿病进行干预的临床试验,然后再去分析肠道菌群在干预过程中所起的作用。
我们把 43 名 2 型糖尿病的患者随机分为两个组,一组是阿卡波糖加上一个常规的糖尿病饮食指导,另外一组是阿卡波糖,再去使用一套WTP膳食。这套WTP膳食是一套富含膳食纤维的饮食。
经过 1 周的洗脱期,然后再经过 12 周的干预期,分别去采集干预前、中、后患者的血、尿、便的样本,检测生理生化指标的变化,以及通过粪便去检测肠道菌群元基因组测序,检测肠道菌群结构和功能的变化。

我们发现,高纤维饮食可以显著的增强肠道中短链脂肪酸产生菌的丰度,进一步增加肠道里面短链脂肪酸的水平,然后短链脂肪酸可以去刺激肠道的L细胞产生 GLP-1 等肠道激素,进一步发挥改善患者糖代谢的一个功能。
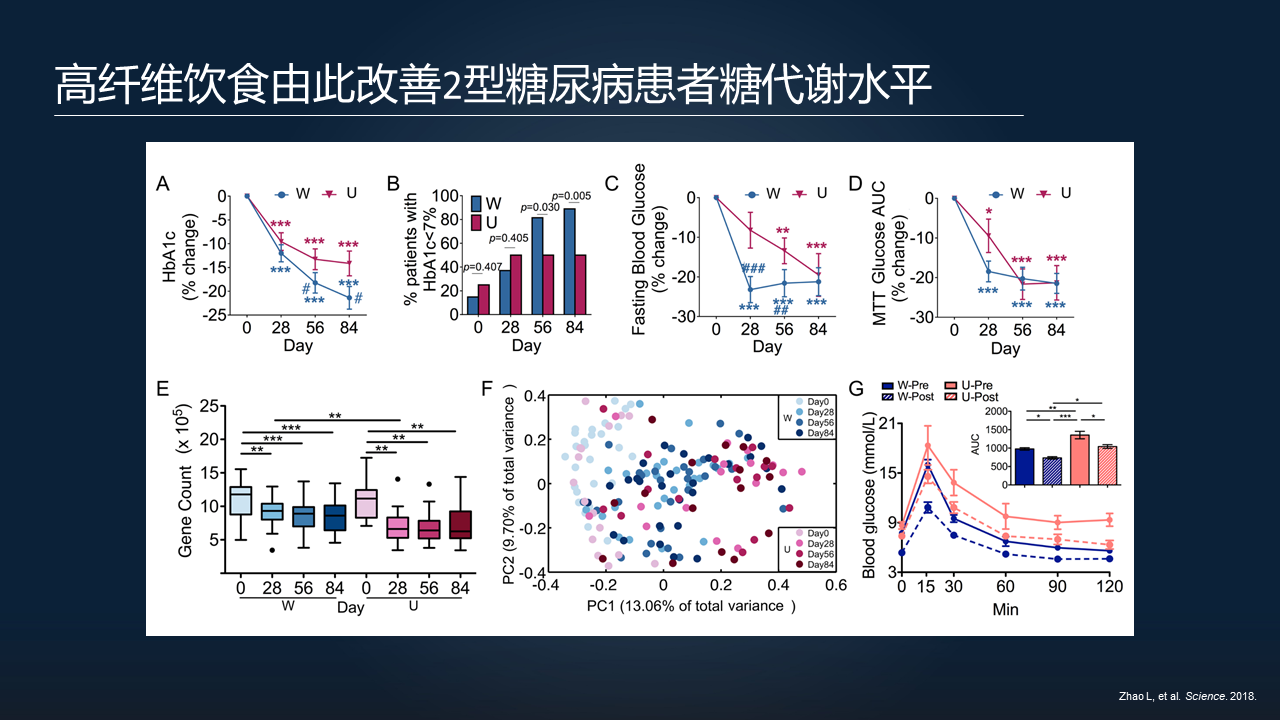
我们又把干预前和干预后的菌群,分别移植给无菌动物,最后证明,肠道菌群的失调或者改善,是 2 型糖尿病的发生发展和改善的原因,它们之间存在这样一个因果关系。这个工作我们发表在 2018 年的 Science 上。
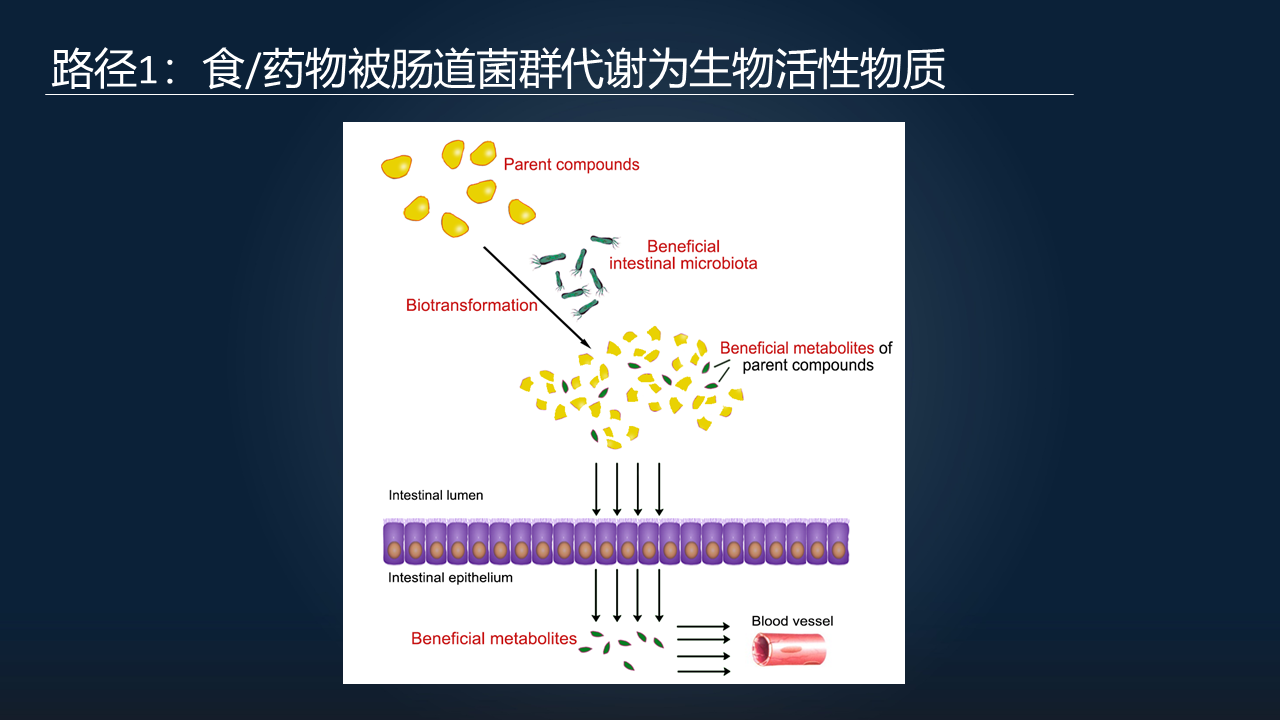
我们就对这一个路径进行了小结。也就是说,有这样一些药物或者食物、功能性的食品,它可以被肠道里面的有益菌代谢产生一系列的有益物质,最后这些有益的代谢物可以透过肠壁进入到血液,进入循环系统,到达靶器官发挥生物学的效应。
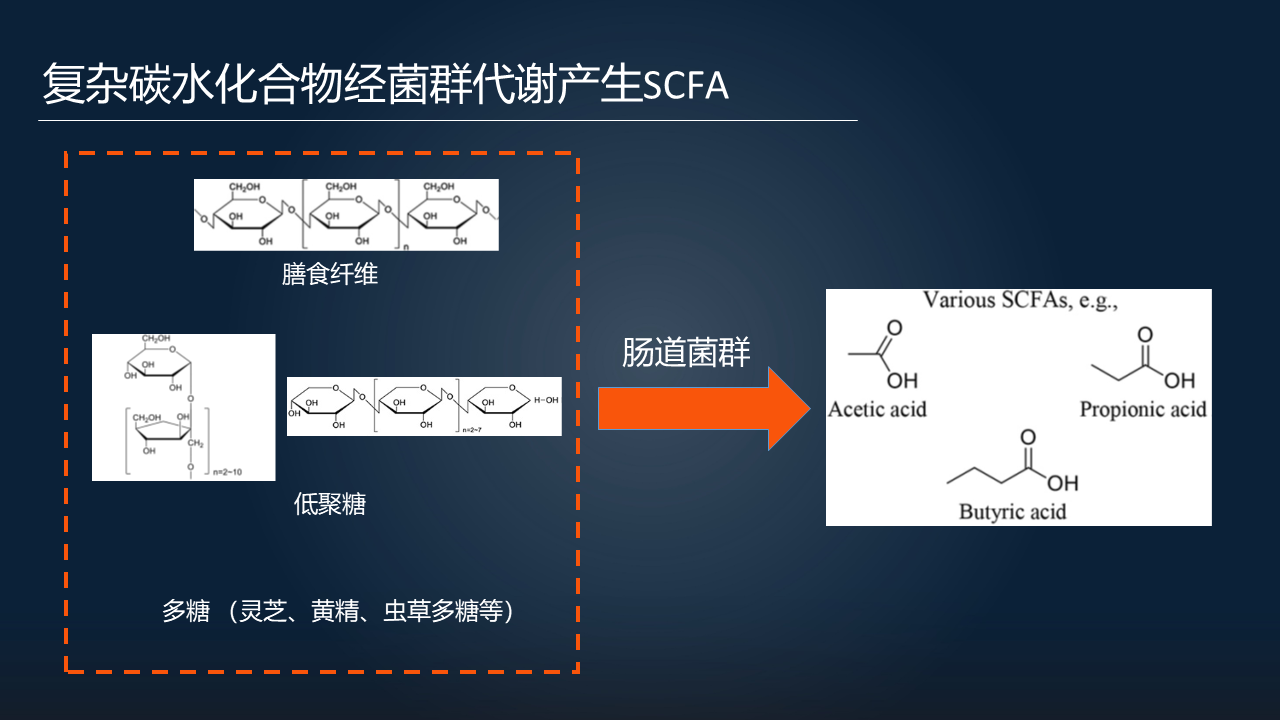
这里面研究最多的就是膳食纤维、低聚糖等等,这些复杂的碳水化合物可以被肠道里面的有益菌代谢为一系列的短链脂肪酸,比如说乙酸、丁酸、丙酸等等。
很多中药,比如说像灵芝、黄精、虫草里面提取出来的多糖,也可以被肠道菌群代谢产生这种短链脂肪酸。这也能够部分地解释,有一些中药可能是通过多糖,由肠道菌群代谢以后产生短链脂肪酸,最后发挥作用的。
另外再举一个比较有趣的例子,这个是与我合作的江南大学食品专业的赵伟教授,他的团队所做的一个研究。
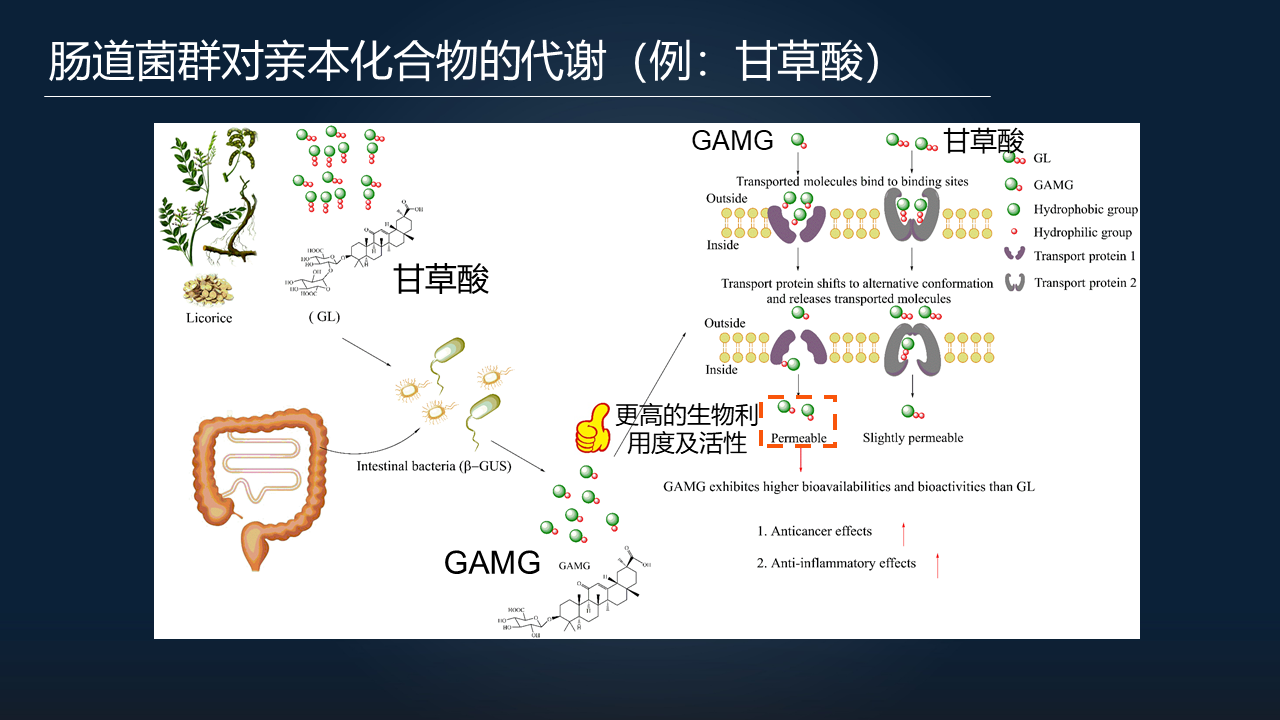
他们从甘草里面提取出来甘草酸,甘草酸是具有一定的抗癌、抗炎的作用。这些甘草酸在肠道里面很容易被降解形成一个物质叫GAMG。无论是甘草酸,还是GAMG,都可以在肠道里面与它们的受体,或者说它们的结合位点相结合。然后,透过肠壁进入血液。
但是,甘草酸的这种结合或者说再解离到血液中的作用比较弱,所以在血液中检测甘草酸的浓度是比较低的,也就是说甘草酸的生物利用度并不高。
但是如果你去检测GAMG,你会发现它可以更容易、更快、更显著的透过肠壁进入血液,去发挥生物活性的作用。也就是说GAMG有一个更高的生物利用度和生物活性,最后去发挥更强的抗癌、抗炎作用等等。
讲到这里大家应该能想到,如果说我们把甘草酸作为一个药物,或者说直接注射给人的话,可能它的作用就不行、比较弱,但是如果把GAMG做成药物可能会有一个更好的效果。我觉得在中药领域可能这一类代谢的过程还是比较多的。

刚刚说到的是,食物和药物本身被肠道菌群代谢,可以产生一些生物活性物质。
那么其实还有一些药物,比如说现在研究比较多的二甲双胍、小檗碱,现在认为它们也可以去调节我们的肠道菌群。它们可以去富集肠道中的短链脂肪酸产生菌,但是这些短链脂肪酸并不是来源于这个药物本身。这些药物是调节肠道菌群,使之代谢从食物中摄取到的碳水化合物,最后生成的短链脂肪酸。所以它的亲本化合物是不一样的。
其实在很多的药物上,这两条路径也不能截然分开,尤其在中药里面。因为不能确定那些有益的物质到底是不是直接来源于中药本身,那么这也是我们值得在这个领域里面进一步研究的。
刚刚我们讲到的是,这些食物或者药物可以去调节肠道菌群,去促进这些有益菌把一些物质转变成一些有益的代谢物去发挥作用。
其实我们肠道里面也有一些有害菌,它可以去代谢一些有害的物质生成有害的代谢产物,去发挥一些有害的作用。我们也可以通过一些食物或者药物,去抑制肠道里面的有害菌代谢产生有害物质。
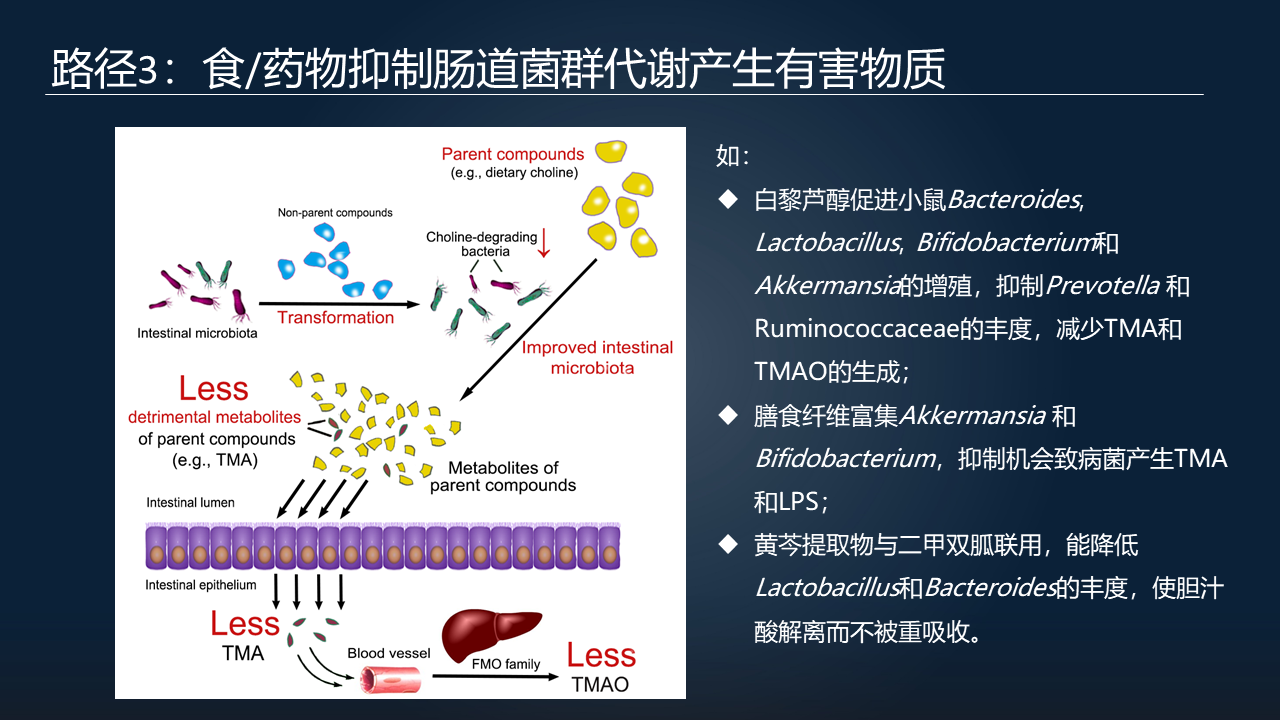
比如说,食物中胆碱可以通过胆碱代谢菌最后产生 TMA,进入血液,经过肠肝循环到了肝脏,加氧以后变成 TMAO,那么我们知道 TMAO 是与动脉粥样硬化密切相关的。我们可以通过一些食物或者药物去调节肠道菌群,抑制TMAO的生成。
比如说,通过白藜芦醇促进小鼠中 Bacteroides、Lactobacillus 、Bifidobacterium 和 Akkermansia 这些有益细菌的增殖,另一方面去抑制 Prevotella 和 Ruminococcaceae 这些有害菌的丰度,减少 TMA 的生成,进一步降低血液中TMAO 的浓度。
此外我们也可以通过膳食纤维去富集 Akkermansia 和 Bifidobacterium,抑制一些机会致病菌产生 LPS 或者 TMA 。
我们可以使用黄芩的提取物与二甲双胍一起使用,降低一些细菌的丰度,使胆汁酸被解离而不被重吸收,使次级胆酸的浓度下降。
那么这个就是第三条路径。

我们在2019年查阅文献的时候发现,Andrew Goodman实验室陆续在Nature和Science各发表了一篇论文,就是讲肠道菌群也能代谢药物变成一些无效的成分。

比如说他们发表在 Nature 的这篇文章,他们把 271 种药物和 76 种细菌在体外进行共培养,相当于一个棋盘滴定,然后他们用 LC-MS 去看代谢物的浓度。首先去看一下这些药物在培养基中还有多少的浓度,以及生成的这些有害物质或者一些小分子物质有多少的浓度。
结果他们发现,有 176 种药物能被 76 种细菌中的至少一种细菌所代谢,能够产生大量的小分子的物质,其中有一些就是有害物质。这也就是这些药物产生毒副作用的一种可能的机制。
另外,他们发表在 Science 的这篇文章做了一个动物实验。他们用无菌动物和野生型的小鼠,同时去检测药物的生物利用度。通过对比有菌和无菌,看宿主和细菌在这个过程中分别起了多大的作用。也就是它们对于药物的生物利用度的影响,它们的贡献度是百分之多少。
结果他们发现,也是让我们比较吃惊的一个地方,就是细菌或者说菌群在药物代谢中起到的作用达到了 70%。这个是一个非常高的比例,也就是说细菌的作用已经高过了宿主的作用。

我们就把这一个途径总结为第四条路径。也就是说食物和药物可以抑制肠道菌群代谢目标的药物,避免菌群将我们需要的药物转变为无效的成分;反之,如果菌群会使药物的有效成分降低、无效成分升高,它就会使生物利用度下降,另一方面也可能会产生一些毒副作用。比如说氨氯地平就是这样一个例子。
如果我们可以找到一些药物,把代谢目标药物的细菌的浓度给抑制住,那么我们就可以提高目标药物本身的生物利用度。
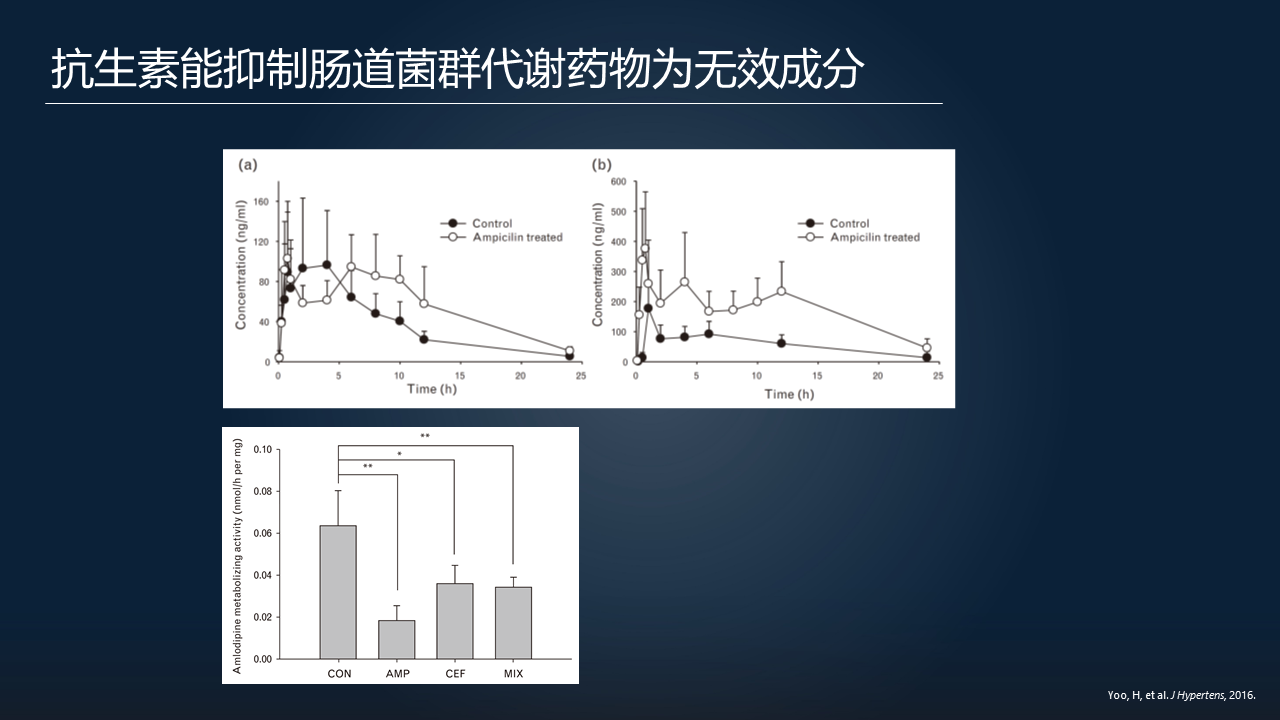
其实在这个方面已经有人做了一些探索。比如说,有人发现抗生素,无论你是用氨苄青霉素,还是头孢类的药物,都可以抑制肠道菌群代谢药物变成无效的成分,提高药物的生物利用度。
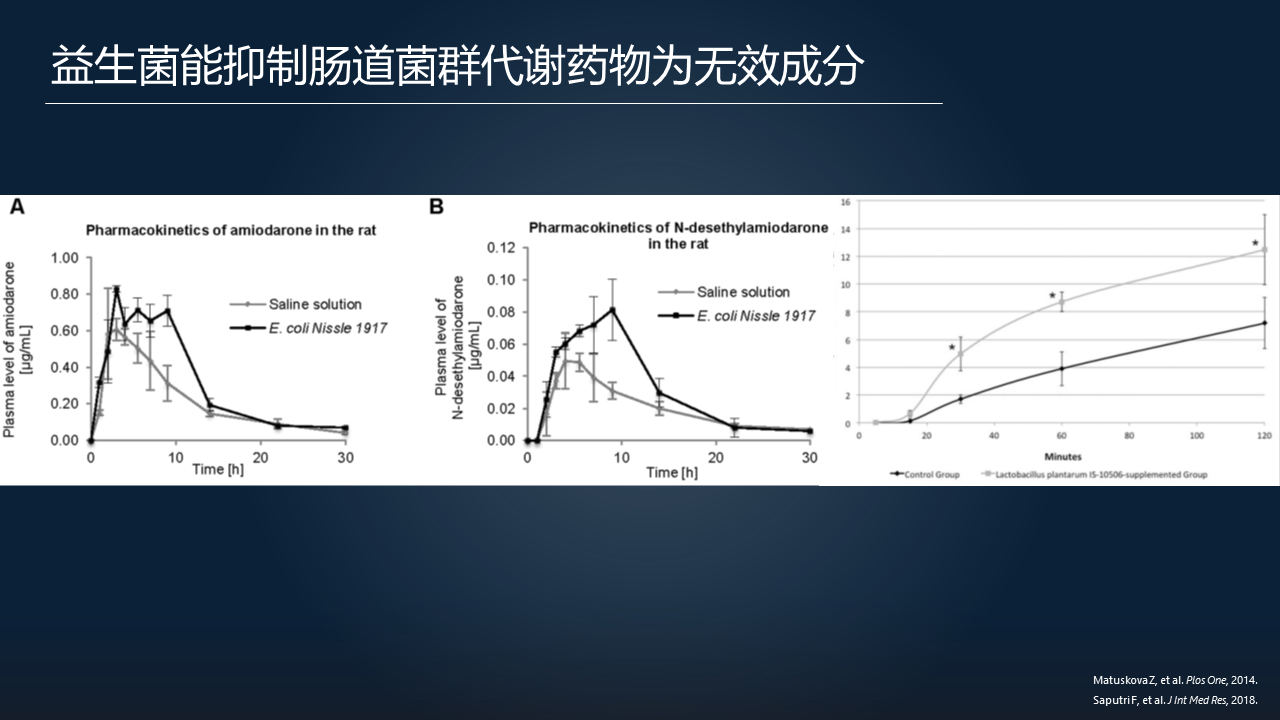
另外益生菌也有这样的作用。比如说,大肠杆菌的一个益生菌株,它可以去增加胺碘酮及其代谢物去乙胺碘酮的生物利用度。
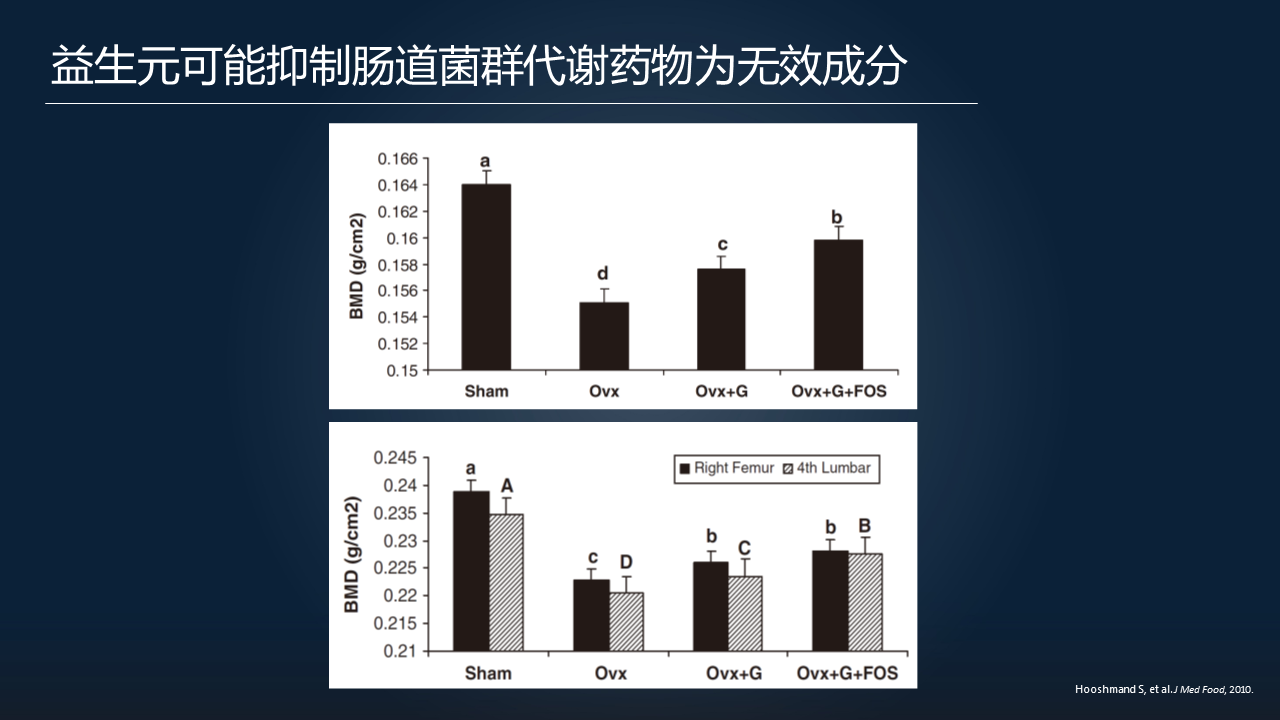
益生元在这个里面的作用,目前我们还没有找到确凿的证据。但是有一篇文章发现使用益生元可以提高药物的疗效。从另一个侧面来说,益生元可能是抑制了肠道菌群代谢药物,提高它的生物利用度。这个还是值得进一步研究的。

我们对这些途径以及方法进行一个总结。
第一个,我们可以去调节肠道菌群,使有益的代谢物水平增高,或者可以直接去使有益代谢物更多的进入到血液。
第二个,我们通过某些药物去调节菌群,使它代谢食物中的有益物质转变为更多的有益代谢物,发挥生物学作用。
第三个,我们降低产生有害物质的这些细菌。
第四个,我们抑制把目标药物降解为无效成分的这些细菌。
那么具体的策略可以分为4个方面。
第一个,如果我们已经确认某些小分子的代谢物,是有这种生物活性的,那么我们就可以直接把这种代谢物做成药物,甚至可以做成注射液直接给病人使用。
第二个,你可以把这些确定的有益菌——无论是可以直接代谢药物的,或者说是促进菌群去代谢食物中有益成分的,或者说是抑制有害菌的——这些有益菌直接去移植给宿主。
第三个,我们可以通过益生元等等这些手段,直接去富集肠道里面的益生菌或者去抑制有害菌。
最后一个,如果我们可以构建产生这种有益代谢物的工程菌,把它移植给宿主,也能发挥这样的作用。
当然这4种方法并不是每种都全部针对上面说的4条途径。那么有些可能对这4条途径都有用,但有些可能只在2种或者3种途径中可以发挥作用。

我们跟江南大学赵伟教授团队一起合作撰写了这样一篇综述,发表在今年5月份的Microbiology and Molecular Biology Reviews上面。
由于我们看到了大量的药物或者食物可以通过肠道菌群提高生物利用度,所以我们目前已经陆续的开展一系列的食物、功能性的食品或者药物,通过改善肠道菌群提高生物利用度的一系列的研究。
有些我们已经做完了,有些可能还在进行中,那么也希望将来有更多的机会通过《肠·道》这个平台与大家分享。
最后非常感谢大家。


