
大家好,我是来自于北京大学心血管研究所的郑乐民,我今天主讲的主要是“肠道菌群代谢和代谢性疾病”。
我们主要研究的是心脑血管疾病和内分泌相关疾病的相互作用和影响,这是我第二次在这个舞台上。今天跟大家分享的是我们最近两年做的研究。

所以我主要通过,第一个还是最关心的肠道菌群对心脑血管疾病的影响;第二部分是肠道菌群代谢对内分泌性疾病,比方说非酒精性脂肪肝的影响;第三部分,我想讨论一下代谢物对心血管疾病的影响,而且这些代谢物可能会和肠道菌群产生关联。

第一部分是肠道菌群代谢产物对心血管疾病的而影响。首先,我们看一下研究。

欧洲有个1000多人的研究发表在Nature Medicine上,引起了大家的关注。为什么呢?
因为大家知道,肠道菌群代谢和心血管研究其实历史不长,在2010年以后肠道菌群和心血管的相关性研究在逐渐开始。到目前,其实在很多医院,菌群、代谢相关的诊断和治疗还是缺乏的。

但是可以看到,越来越多的人关注到肠道菌群和心力衰竭、冠心病和心血管疾病相关的研究。比如说这一篇在JACC子刊上的研究,大家就讨论到了一个肠道菌群的代谢物和心衰的关系,就具体到哪个代谢物。
可见现在大家对菌群、代谢以及心脑血管疾病的关系,已经比10年前更深入了。大家希望看到更直接的肠道菌群相关的酶、代谢以及心血管疾病的影响。
TMAVA(三甲基-5-氨基戊酸)
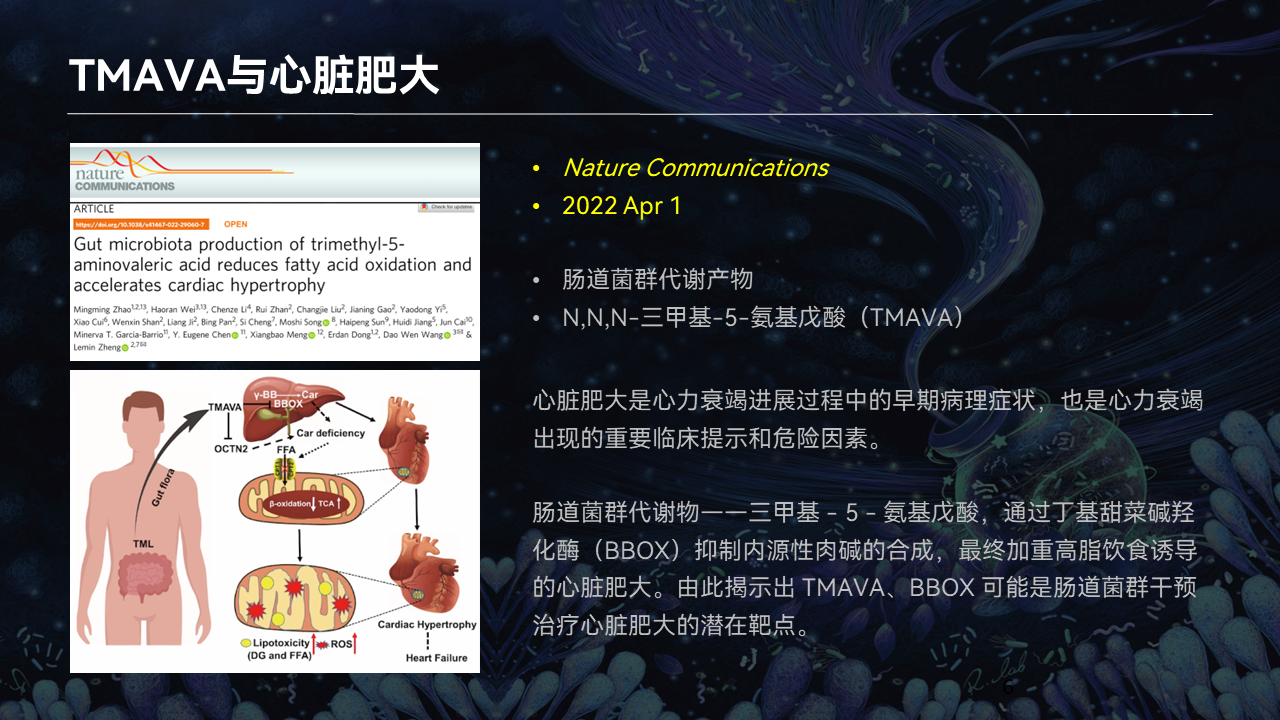
我们团队很有幸,从2010年以后也在这方面做了很多工作。
其中很重要的一个就是,我们发现了一个肠道菌群的代谢物——三甲基-5-氨基戊酸(TMAVA)。这个代谢物是我们团队在这个病生理的过程,特别在动物的过程,是首次报道的。
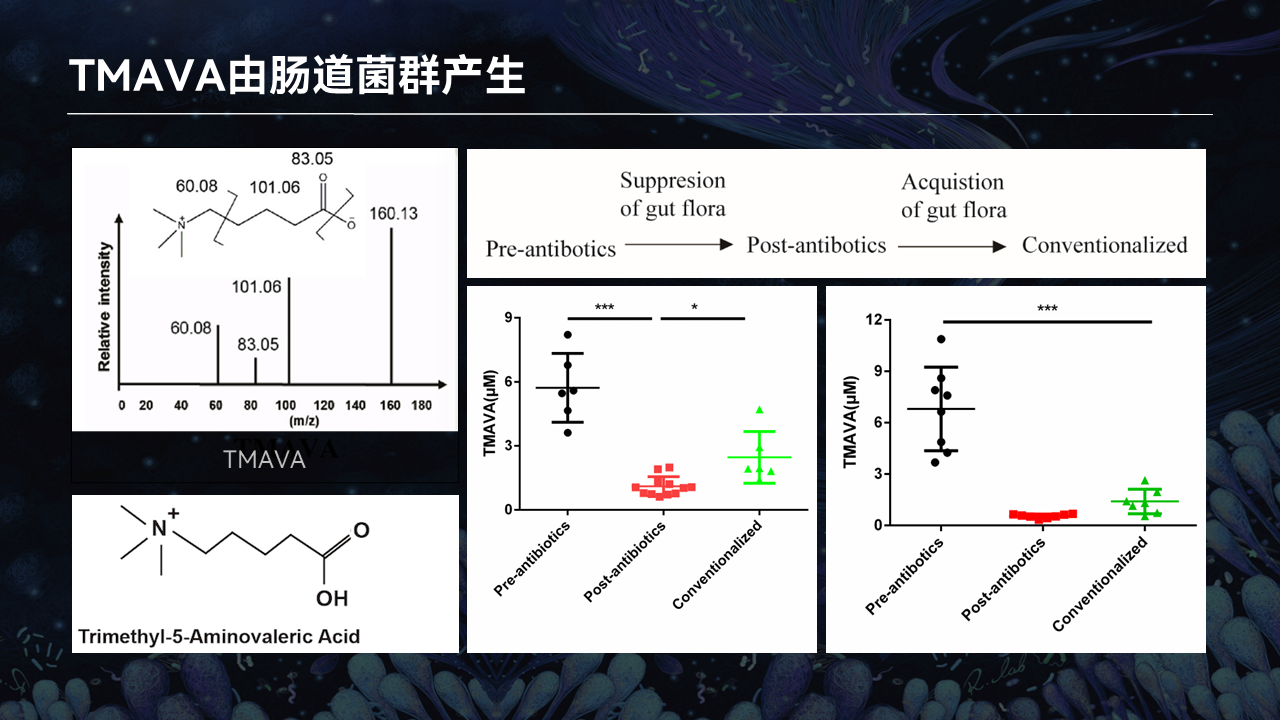
三甲基-5-氨基戊酸,它看着很像早期研究的氧化三甲胺(TMAO)。当然我们发现,它跟氧化三甲胺是不同的通路,它确实是菌群带来的,所以在无菌老鼠中,你很少发现代谢物。
另外,你通过抗生素抑制以后发现能够抑制这种代谢物,同时进行菌群移植,这个代谢物的量又提高了。
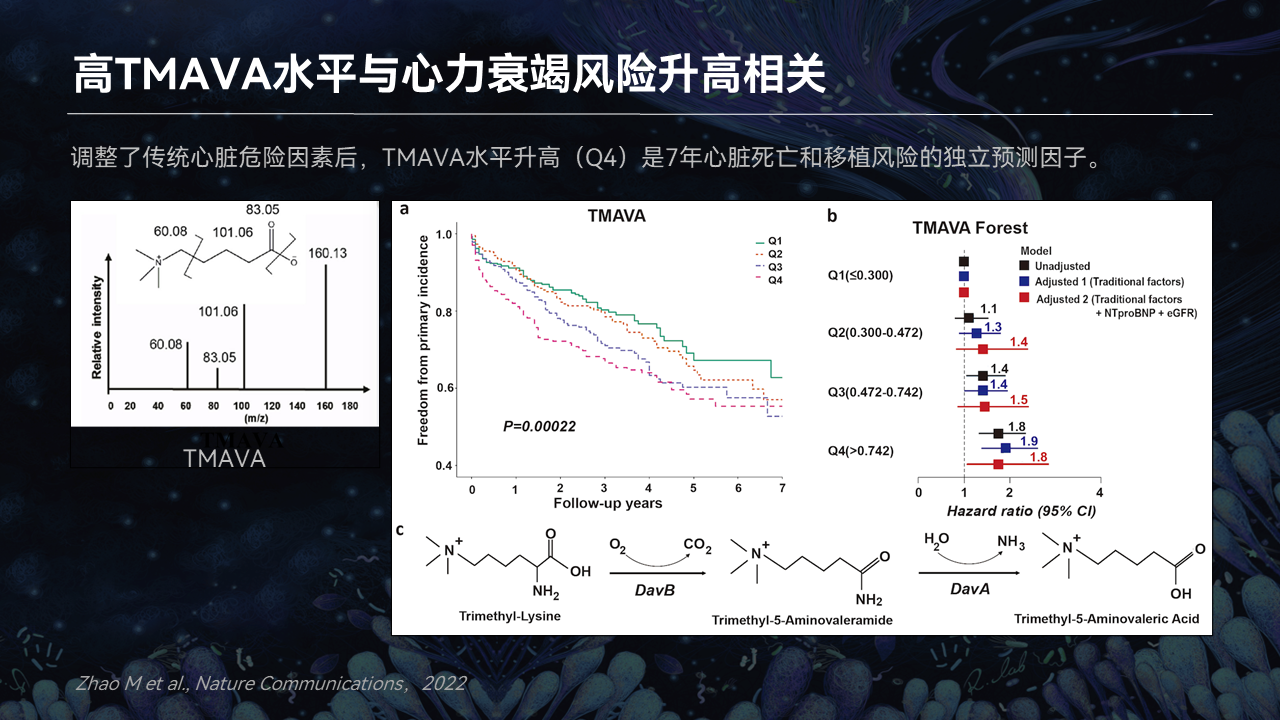
我们和武汉的汪道文老师合作,观察了样本中TMAVA的量。我们发现,在7年的病人的死亡和移植风险中,它是密切相关的。TMAVA是一个坏的因子,和心衰的风险是相关的。
另外我们也发现,菌群中存在着两个酶——5-氨基戊酰胺酶(DavA)和赖氨酸2-单加氧酶(DavB)。它们可以通过我们内源性的代谢物,然后逐步地产生了TMAVA。
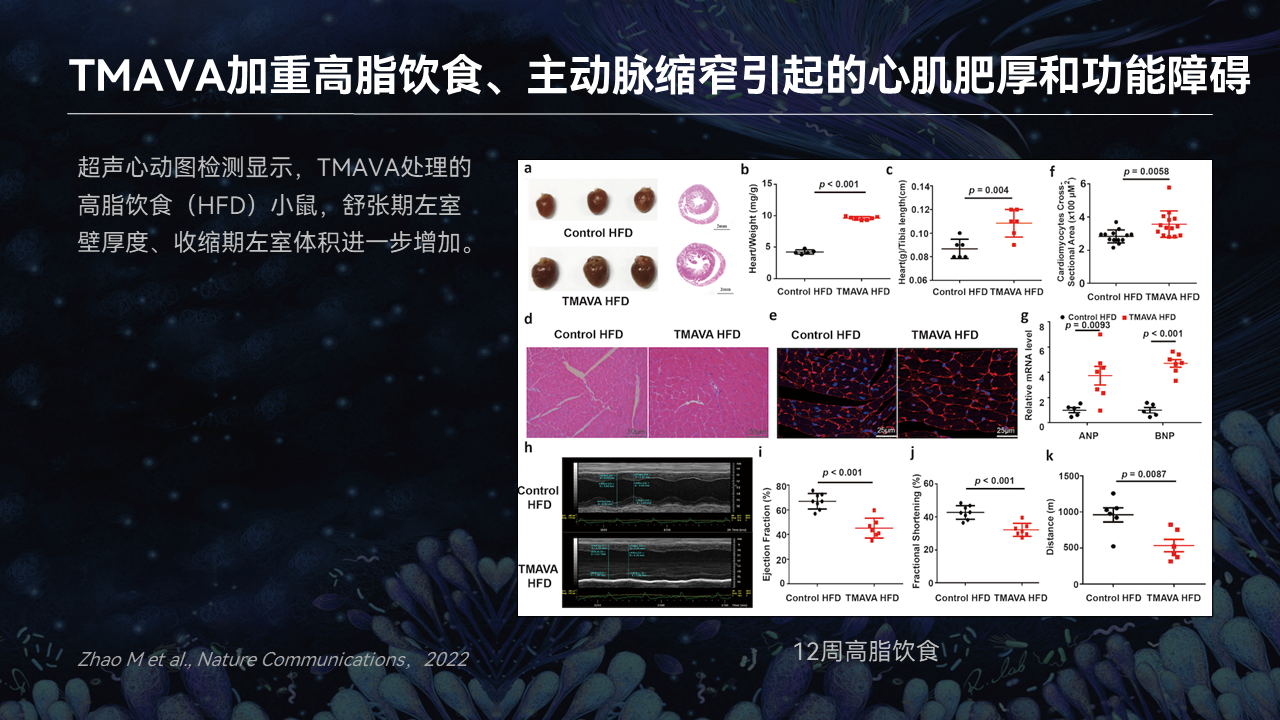
所以说,TMAVA会加重高脂饮食、主动脉缩窄引起的心肌肥厚和功能障碍。
我们可以看到,整个心脏是变大的,心肌细胞的横截面是变大的。而且我们可以看到,这种射血分数的下降以及短轴缩短率的下降,表示了显著的功能的下降。
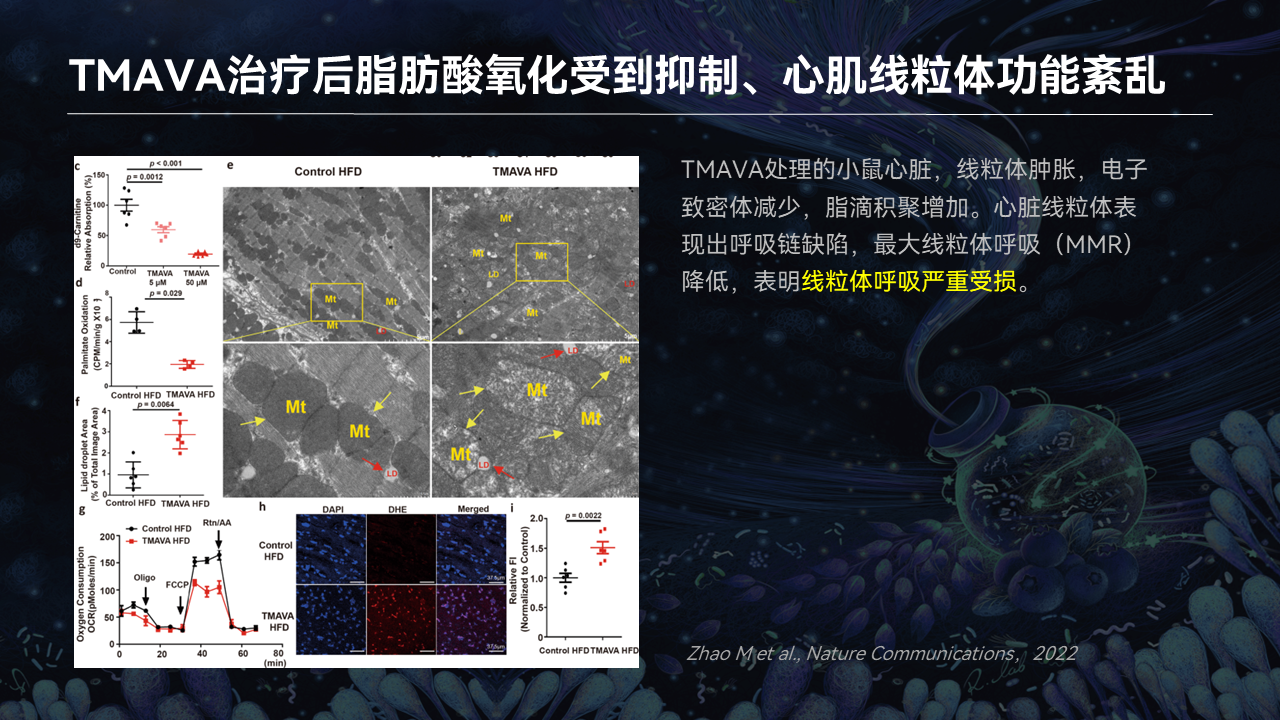
在看到亚细胞结构以后,我们发现线粒体发生肿胀,大家可以从电镜的图片中看到。
而且我们做了海马呼吸发现,线粒体的呼吸严重受损,线粒体呼吸的强度下降了,伴随的是氧化应激增高了。
所以说为什么它会出现这种障碍呢?
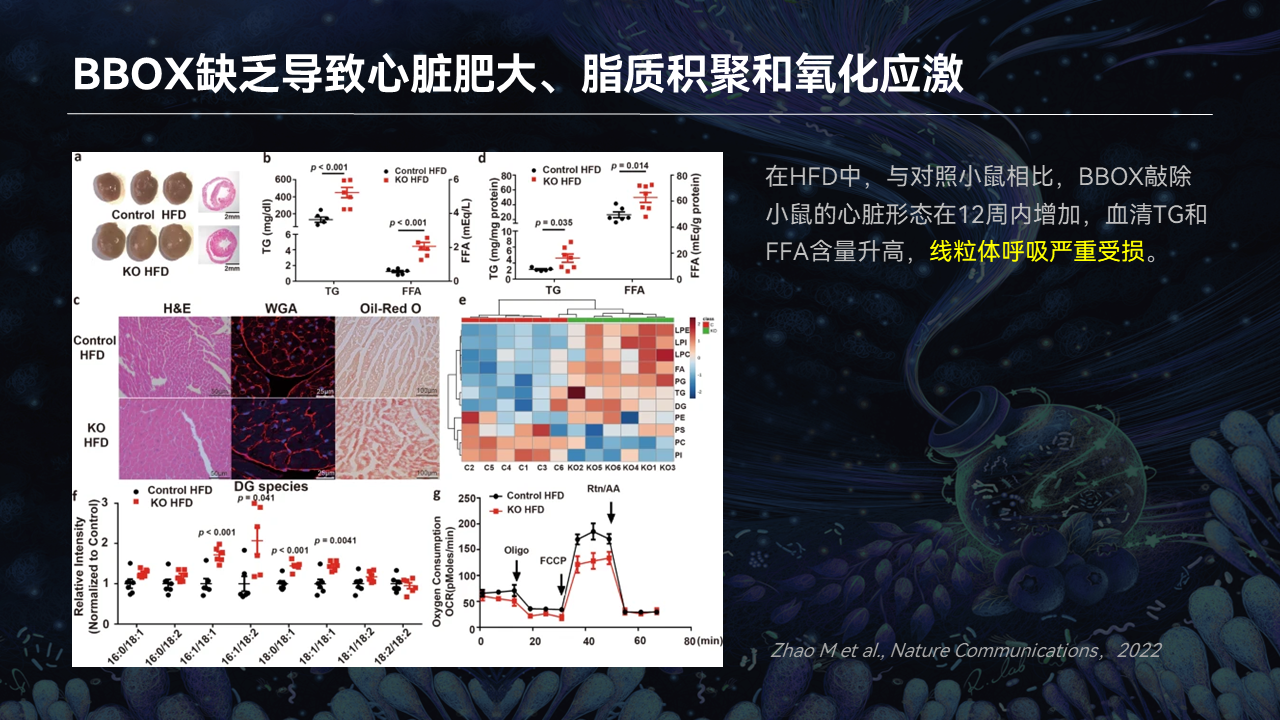
我们发现这种肠道菌群产生的代谢物,它会影响一个酶叫BBOX(丁基甜菜碱羟化酶)。我们从蛋白组学找到了这个酶,我们发现,BBOX缺乏就会导致心脏的肥大、脂质的堆积以及氧化应激的增高。
另外找到了动物进行了敲除以后,我们发现心脏的肥大也是加剧了,说明代谢物的靶点就是BBOX。
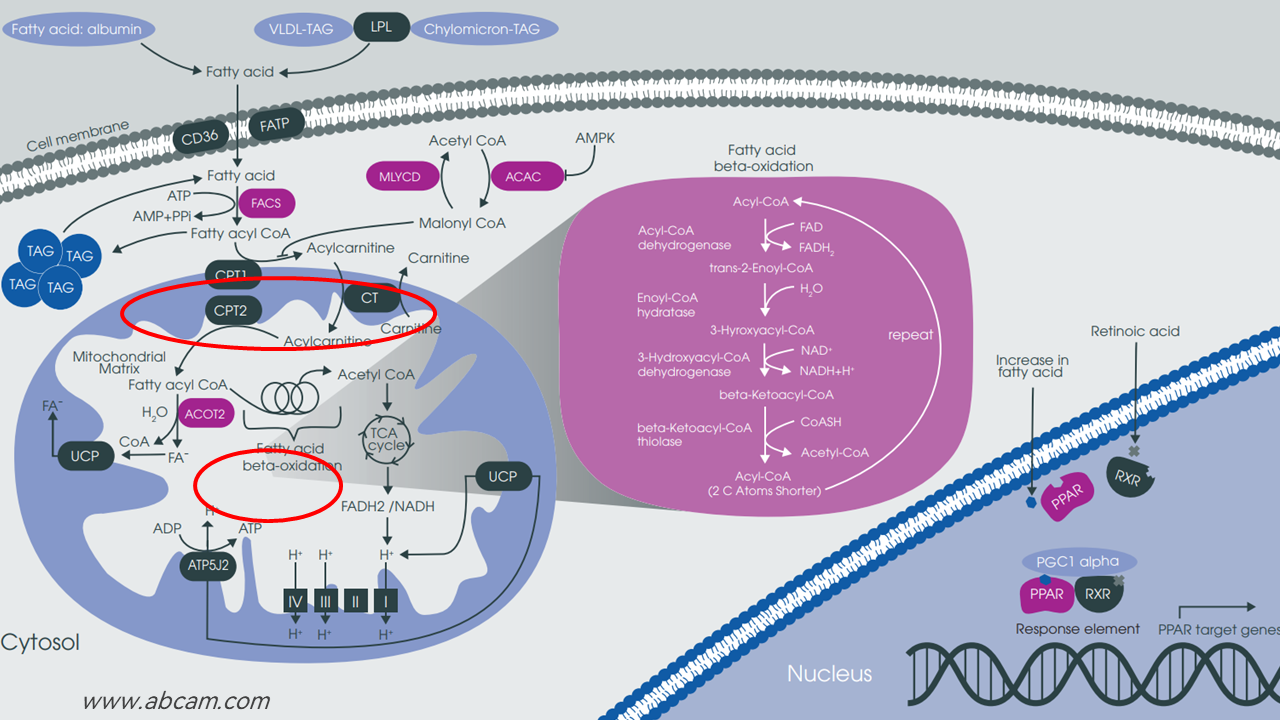
所以说,我们再看线粒体的β-氧化。
短链的脂肪酸指碳链≤12的脂肪酸,可以直接进入线粒体。但是链长大于14的脂肪酸,要通过酰基肉碱的帮忙,才能进入线粒体进行β-氧化。
我们也发现营养还是很重要的,所以我们要保证一定的红肉量、一定的蛋白质,最后会产生肉碱、酰基肉碱,能够帮助心脏和肝脏的脂肪酸β-氧化。
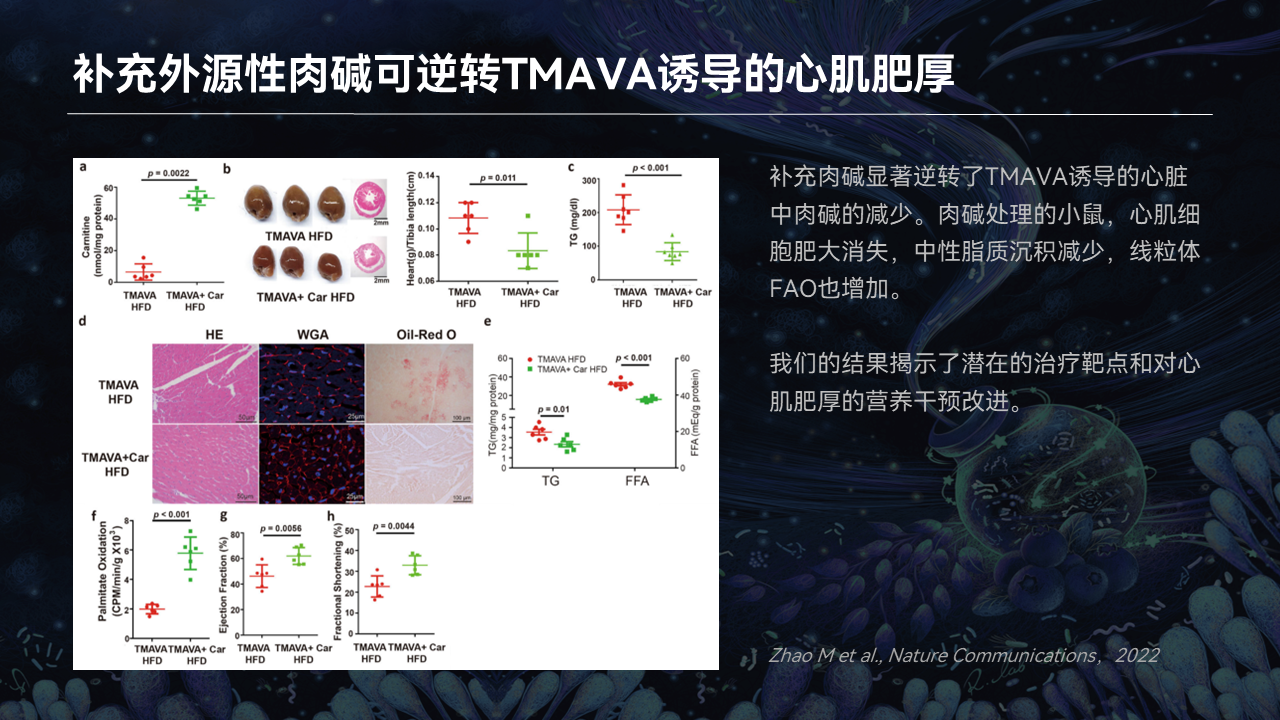
在这种TMAVA处理的小鼠中,如果再补充外源性的肉碱,我们发现可以逆转TMAVA诱导的心肌肥厚。所以,我们需要营养帮助脂肪酸的β-氧化。
而且我们的心脏、我们的肝脏,特别是我们的心脏,需要脂肪酸的β-氧化超过了对葡萄糖的需要,所以我们需要长链脂肪酸的β-氧化。
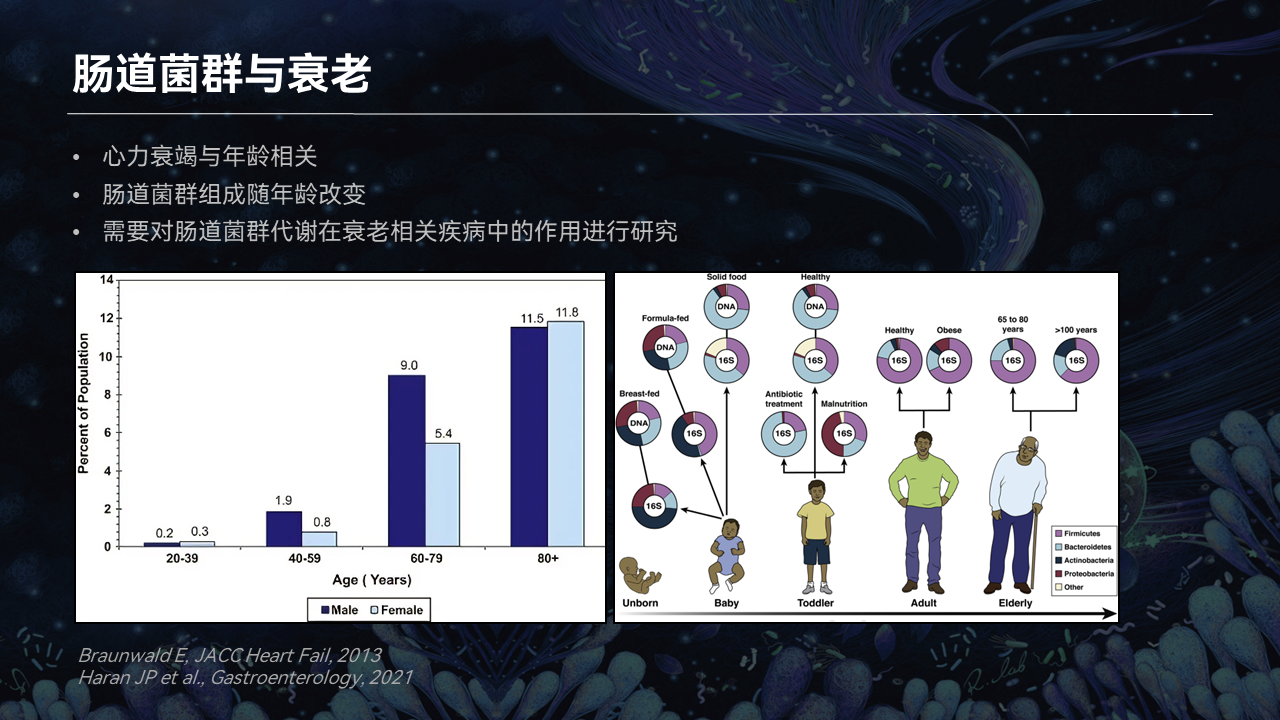
另外我们发现,肠道菌群和衰老密切相关。所以这几年大家开始研究衰老和代谢以及肠道菌群。大家知道“衰老”,无论是从医学上还是从现实的生活中,对我们的社会的影响都非常大的。
所以,这个领域也是非常火爆的领域。
TMAO(氧化三甲胺)

我们再回到2010年,大家广泛研究的,也有我美国的导师Stanley Hazen,他们发现了氧化三甲胺。
我们也在关注氧化三甲胺对心血管的影响,目前普遍认为氧化三甲胺对心血管是有害的。
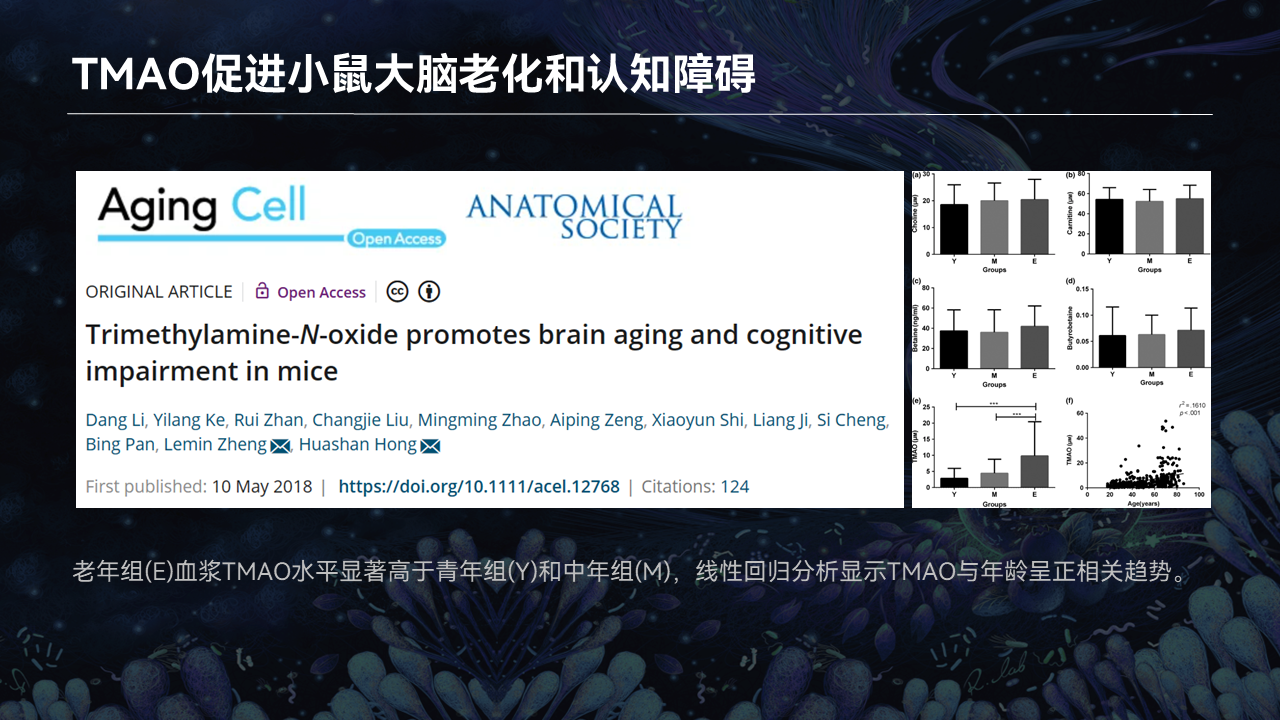
我们2018年的研究也证明了,氧化三甲胺会促进血管的衰老。
大家知道,我们的衰老60%都归咎于血管性衰老。当然还有阿尔茨海默、帕金森,但是我们不可以忽略的就是血管衰老引起的这种血管性痴呆。
我们有幸和天坛医院的王拥军院长合作,发表了氧化三甲胺对卒中的关系。
我们发现,有一类卒中的发生和氧化三甲胺密切相关。而且有一类的病人,特别是小动脉闭塞型卒中的预后,氧化三甲胺越高,则预后越不好。

这项研究我们是看到,天坛医院建立的CNSR-III的队列,这种卒中的复发,3个月、1年的复发情况和氧化三甲胺的关系。
我们得出结论:小动脉闭塞型卒中的预后,氧化三甲胺越高,预后越不好。
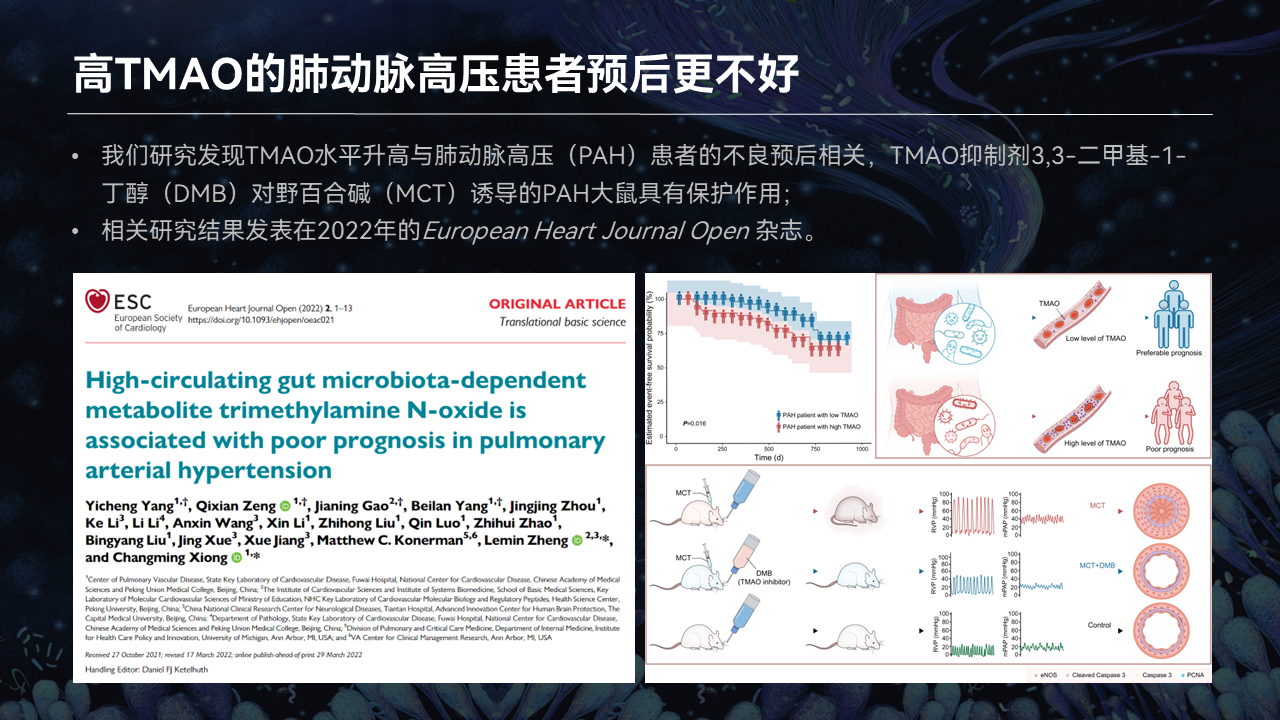
另外,肺动脉高压也是一类小动脉障碍型的疾病。
我们跟阜外医院熊长明老师进行了一些合作发现,高氧化三甲胺的肺动脉高压患者,预后不好。
另外我们也做了一个大鼠实验,给了氧化三甲胺的抑制剂,发现能够改善这种肺动脉高压的症状。
我们团队还继续研究肠道菌群对心脑血管的作用,这也是一个巨大的市场。所以我也很期待将来有更多的机会跟大家合作,研究肠道菌群代谢对心脑血管疾病的影响。

第二部分是肠道菌群对内分泌的影响。我想国内做的人很多,为什么我们对这个也比较关注呢?

大家知道,很多心血管疾病都跟肝脏功能的异常有关。所以在心血管的杂志中就曾报道过,肝脏的障碍对心血管疾病是很有害的。所以大家才会讨论到肝脏对心脑血管疾病的影响,肾脏对心脑血管疾病的影响。
所以我们2020年在《胃肠病学》上也发表了一篇文章,讨论的还是三甲基-5-氨基戊酸和非酒精性脂肪肝的影响。
其实它的机理和心脏有一点关系。肝脏也是一个重要的耗能的器官,TMAVA会影响到内源性肉碱的合成,也会影响到肝脏对长链脂肪酸的利用。如果利用的不好,就会大量的氧化应激堆积,脂肪酸的β-氧化下降,能量少了以后脂肪肝就会形成。
基于甘氨酸的三肽DT-109

我们今年有个研究,引起了很多人的关注,是我们和美国的密西根陈育庆教授团队和西安交大刘恩岐教授,我们三个团队一起做的一个研究。
我们看了3个氨基酸对脂肪肝的影响,甘氨酸-甘氨酸-L-亮氨酸(DT-109)。

我们从1000多只猴子中筛选出匹配的20只猴子,我们或者叫它脂肪肝易感。我们在20只猴子中同样进行高脂的干预,NASH的高脂干预,然后5个月再给予对照和DT-109。
我们发现,三肽对脂肪肝的效果非常好,确实引起我们的很大的关注。
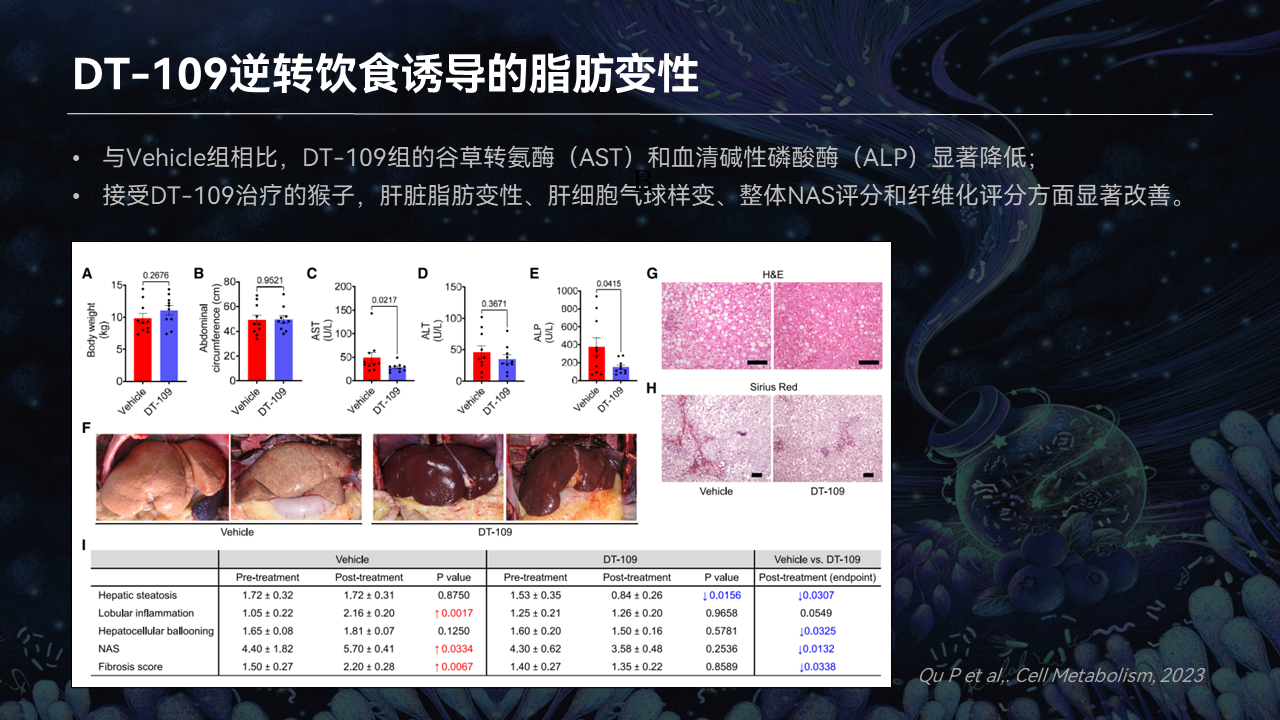
我们通过小鼠实验、猴子实验发现,它都能逆转脂肪肝。这确实让我们感觉很奇妙。
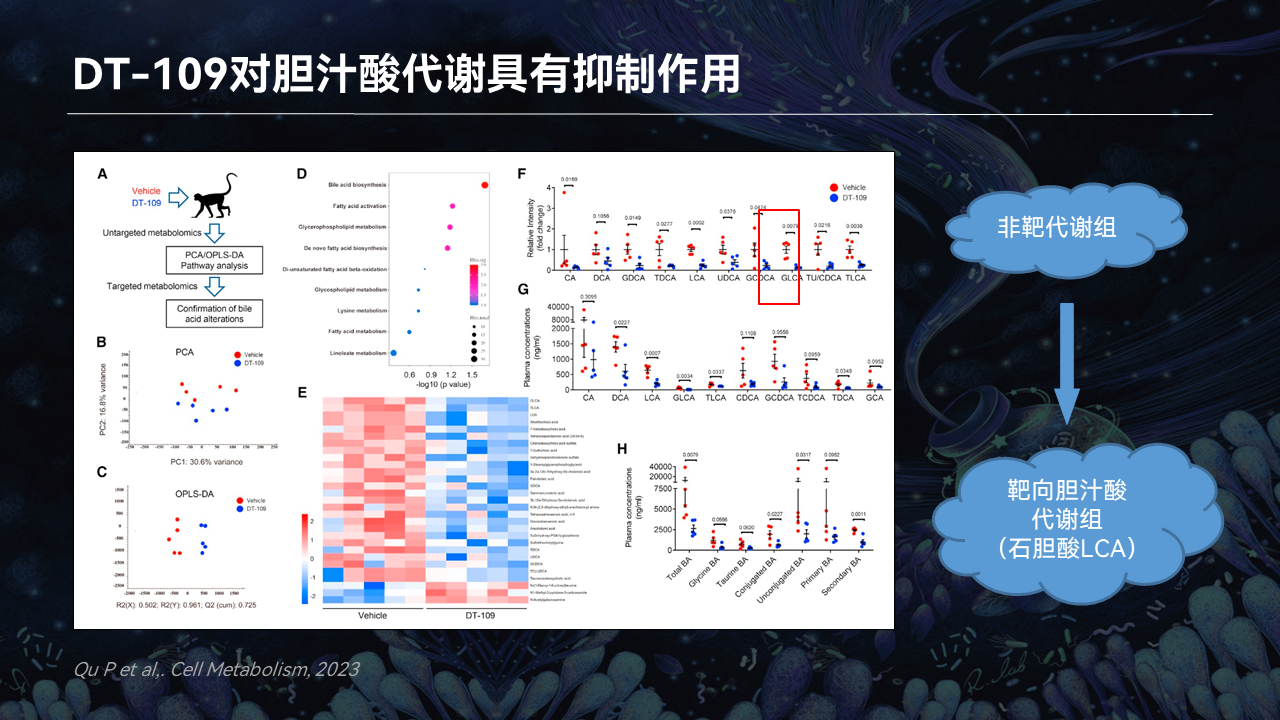
所以说我们进行了广泛的代谢组学研究以及宏基因组的研究,我们想探究一下是什么因素影响到脂肪肝。
我们发现,胆汁酸起着特别重要的作用,特别是石胆酸。
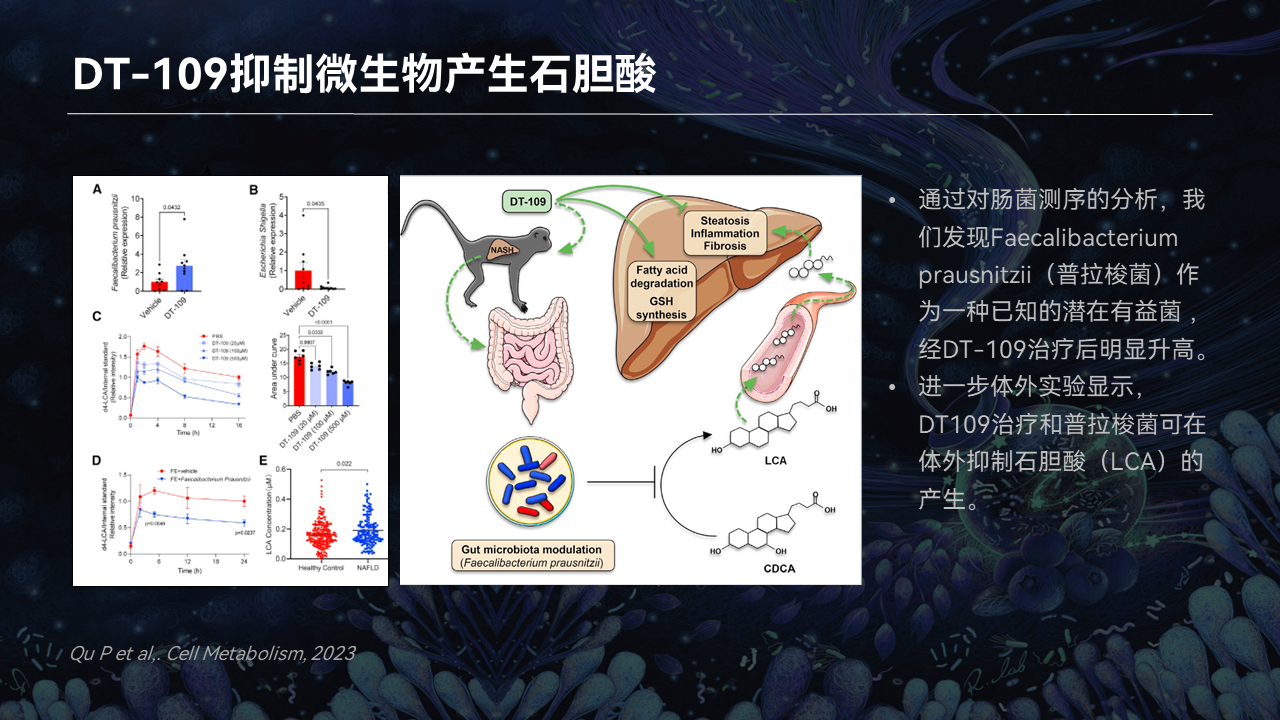
我们发现DT-109会让普拉梭菌大量的增加,另外会抑制石胆酸(LCA)的产生,而石胆酸和脂肪肝非常密切相关。我们认为,三肽会通过肠道菌群影响到胆汁酸,从而治疗脂肪肝。这个研究也被今年的Nature Review 杂志综述进行讨论。
肠道菌群对内分泌的影响,我觉得有可能比心血管病更早地进行成药。大家知道,两年前的法国对菌、对糖尿病的代谢治疗产生了很多研究。我觉得在这个领域,会比心脑血管跑的更快一些。
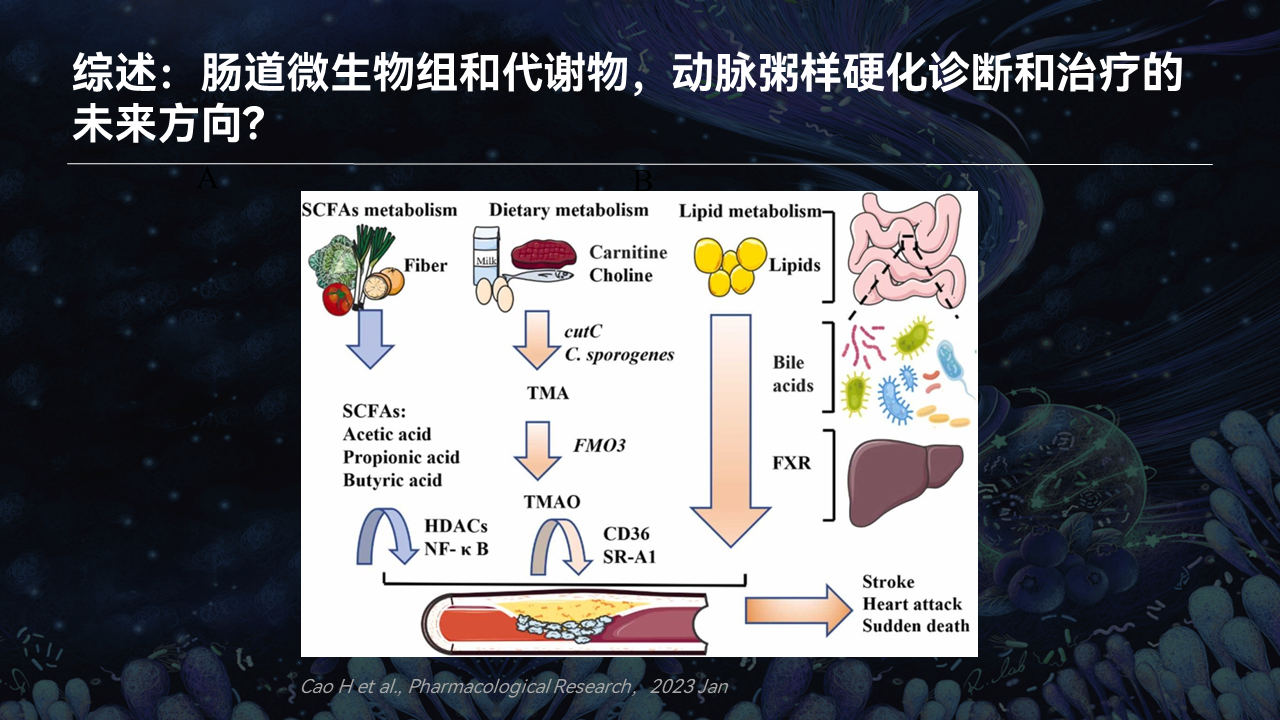
我们针对氧化三甲胺以及一些代谢写成综述。我们觉得,肠道菌群代谢不但会影响到内分泌疾病,比如说糖尿病和脂肪肝,还会影响到心脑血管。
我们认为,其实到现在还不好说哪种菌、菌里面的酶会影响到哪个代谢,会对心脑血管有直接的治疗作用。目前成药或者明确作为保健食品的还不多,还需要更多的临床验证。
我也希望跟更多的商业团队,包括临床团队合作,让我们来确定更多的肠道菌群相关的菌株,特别是对冠心病、主动脉夹层、心衰、糖心病这一系列的心脑血管疾病的影响。

第三部分,我想讨论为什么我觉得代谢对心脑血管疾病非常重要,而且在这方面有非常好的前景。
琥珀酸
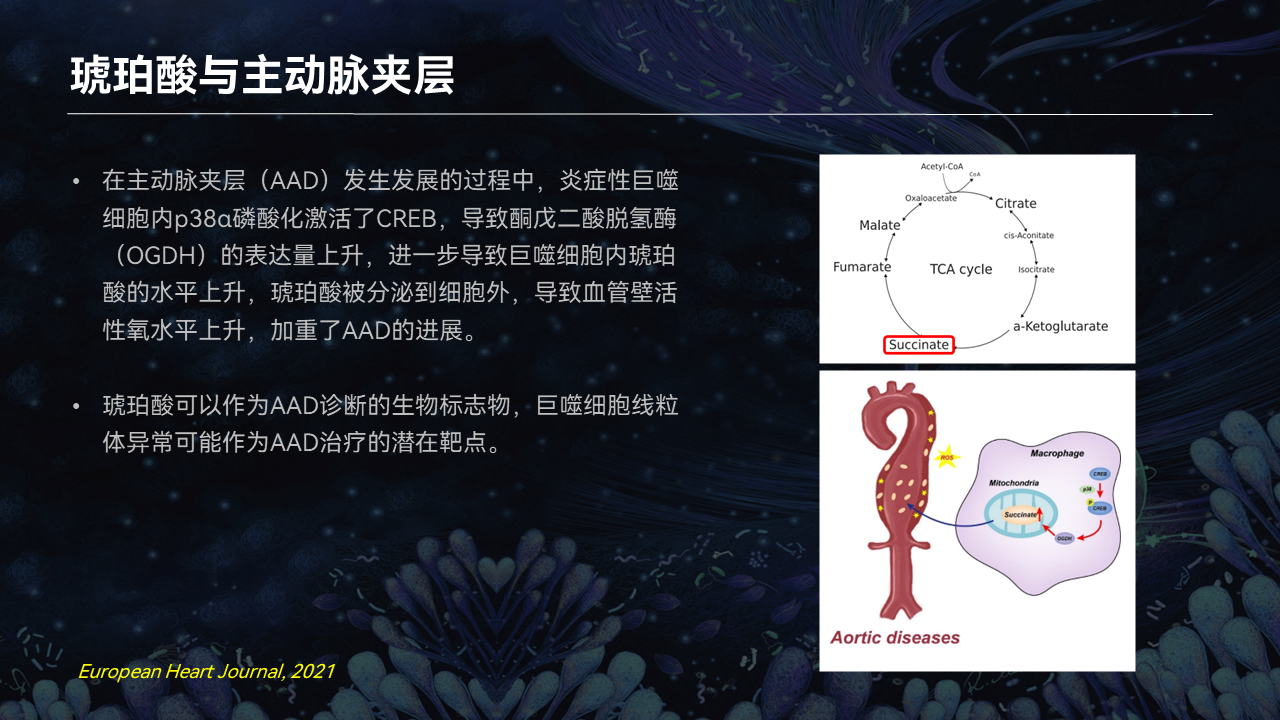
2021年,我们在目前心血管领域影响因子最高的European Heart Journal 发表了一篇文章,讨论到琥珀酸会出现堆积。
在这个研究中,我们只讨论了巨噬细胞产生的琥珀酸,但大家要知道琥珀酸也是肠道菌群产生的一种代谢物。我们发现,琥珀酸可以加重主动脉瘤和夹层。
所以可见,代谢和肠道代谢对血管的结构会产生重要的影响。
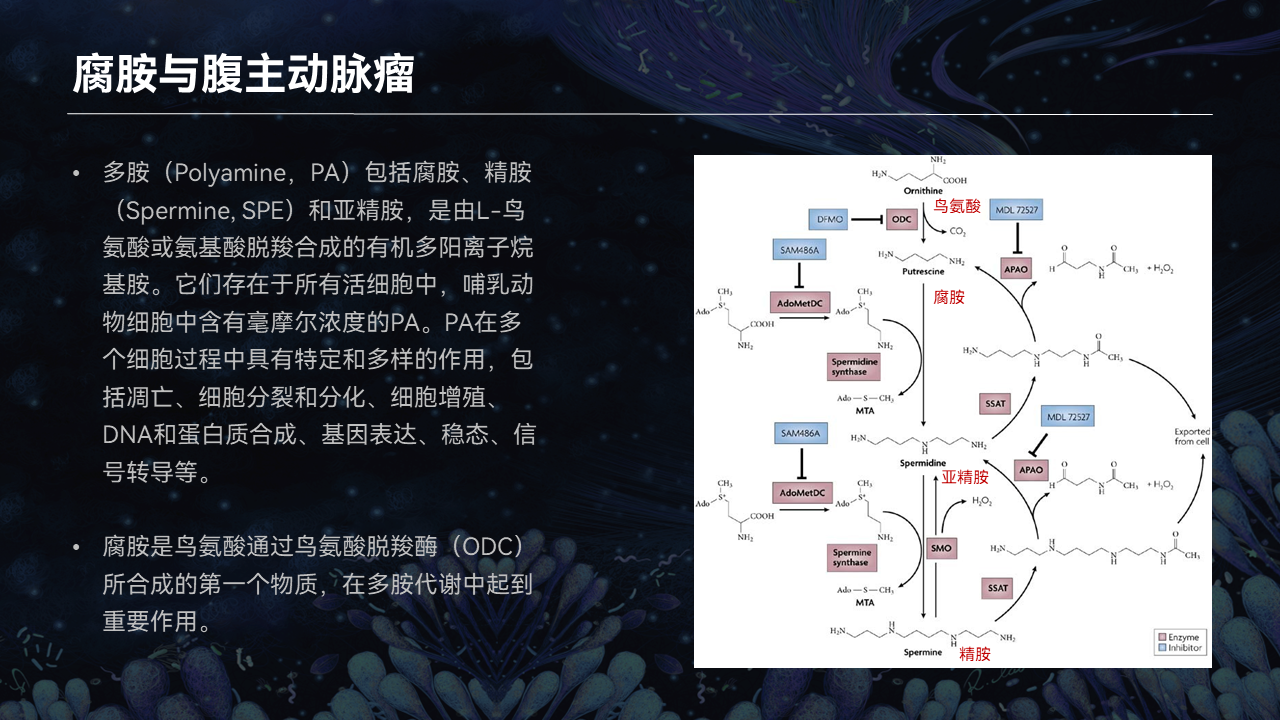
去年和今年我们又发现,肠道菌群和我们人体里面产生另一种代谢物叫腐胺,可能对血管的结构产生了重要影响。
我们可以从精氨酸产生腐胺,而腐胺也可以从多种的代谢产生了多胺代谢,它在癌症中的研究很多。
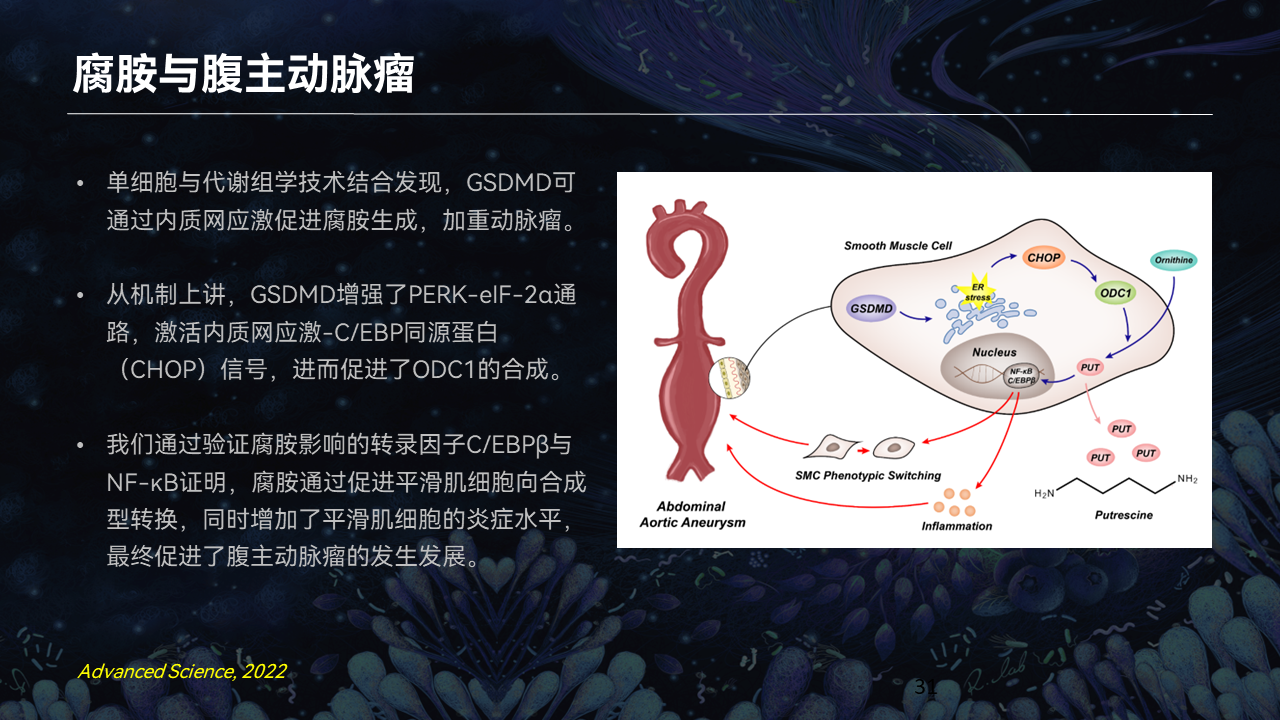
但在心血管的研究中,我们发现它可以影响到平滑肌细胞,让平滑肌细胞从伸缩型变成分泌型,从而加剧动脉瘤和夹层。
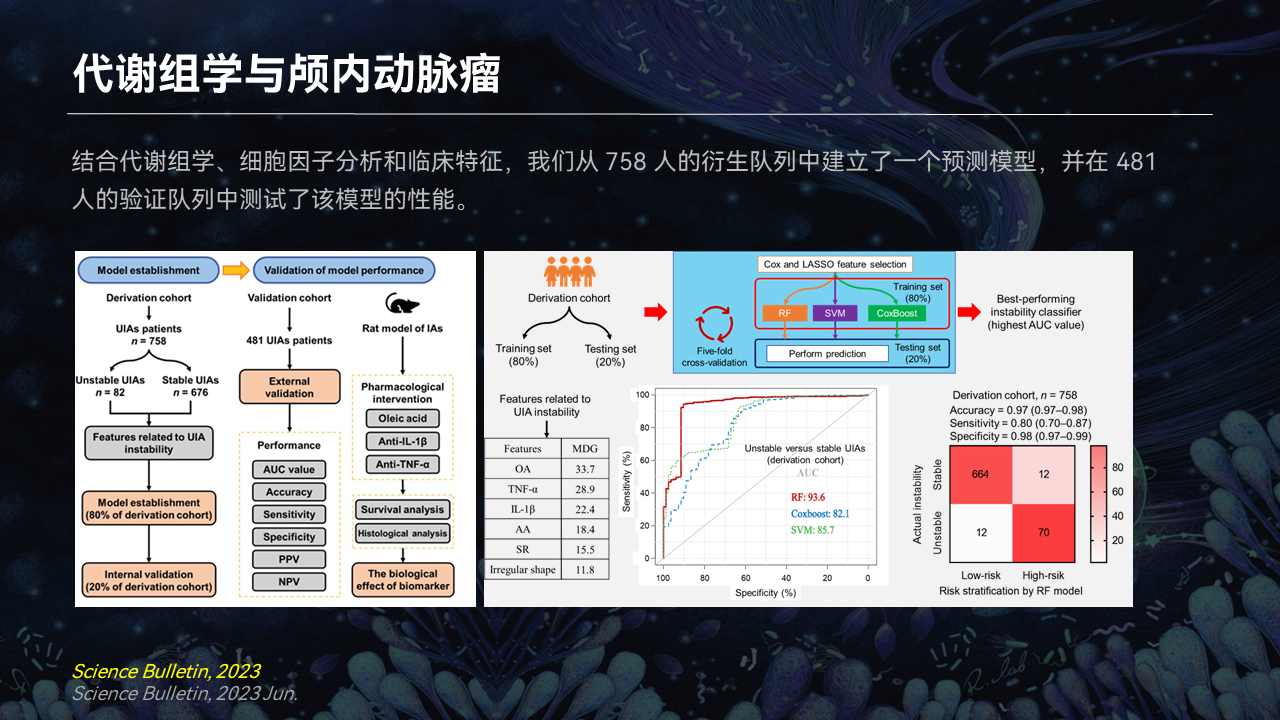
我们和天坛医院王硕主任合作,把代谢的理论、把炎症因子以及疾病的表型联合起来判断,可以更好地推断颅内动脉瘤的破裂。
所以我们今年发表在Science Bulletin上,讨论了多组学联合发现动脉瘤的破裂。
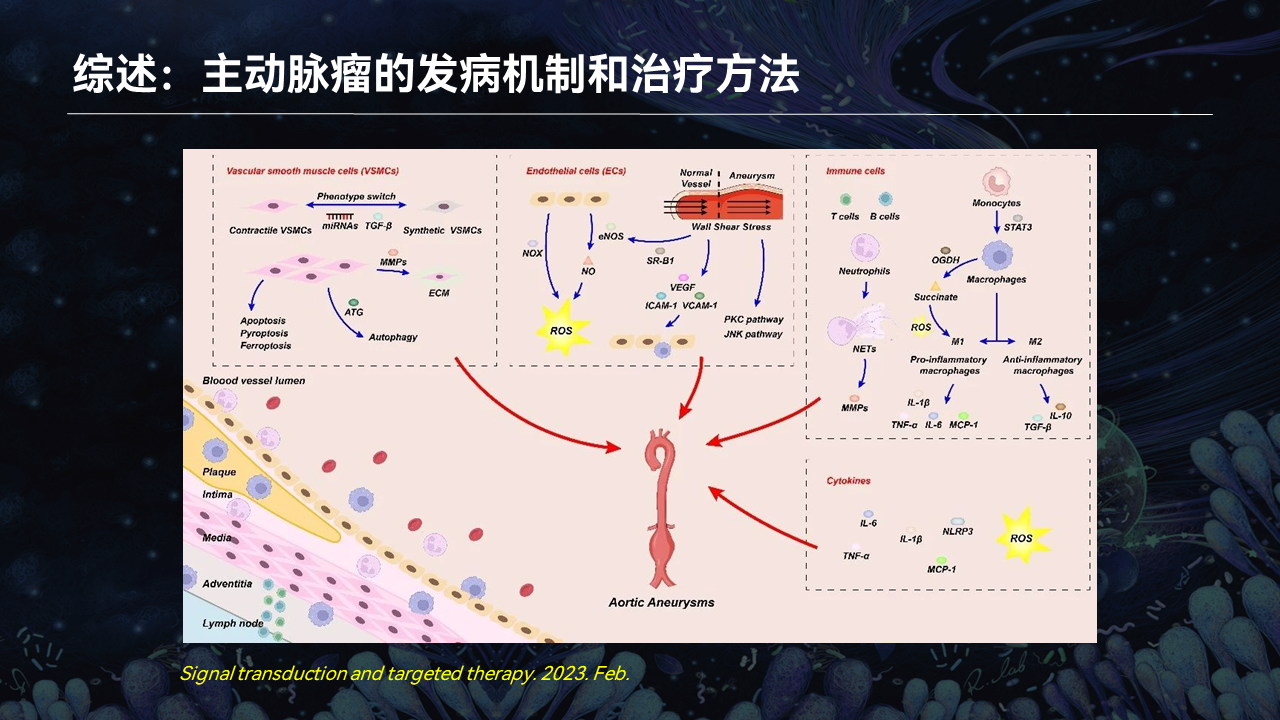
而且我们今年在Signal Transduction and Targeted Therapy上,讨论了动脉瘤的治疗以及代谢对内皮细胞、平滑肌细胞、炎症细胞的影响。
CX43-PARP1-NAD+

今天我还要重点讨论血脑屏障。为什么?因为我觉得衰老与代谢和肠道菌群代谢,是所有人关注的特别重要的问题。
包括最近抗衰老药NMN火了一阵子,它到底是否可以有效,我们也做了一个研究。

我们首先发现,血脑屏障原来不仅是对细菌感染有效,对一些逐渐的衰老、卒中、阿尔茨海默以及帕金森都起到很大的作用。
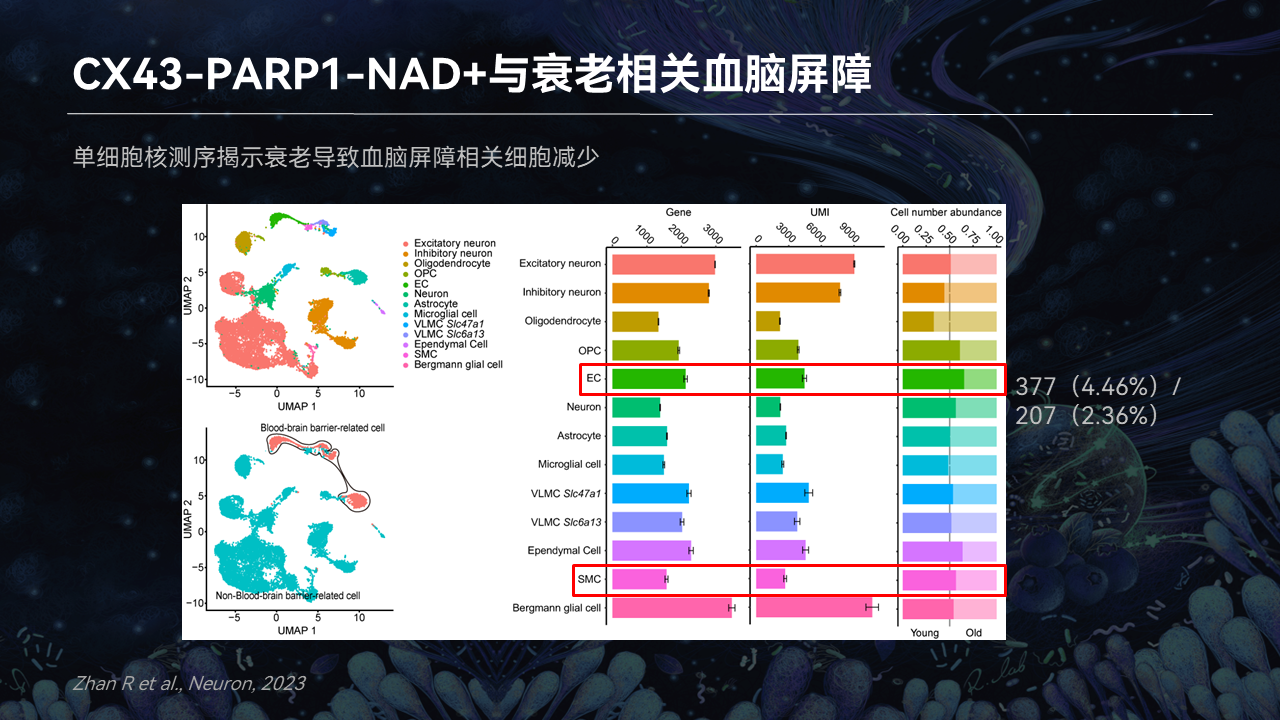
我们从单细胞测序小鼠的衰老模型中发现,内皮细胞会减少,平滑肌细胞会减少。就可见随着衰老,我们的血管结构是慢慢的变差了。

另外从单细胞测序的研究中,我们发现了一种蛋白,叫间隙连接蛋白。
大家要区分于紧密连接蛋白,它是把两种细胞紧密地连在一起。而间隙连接蛋白发挥离子通道的作用,它发挥很多传递代谢物的作用。
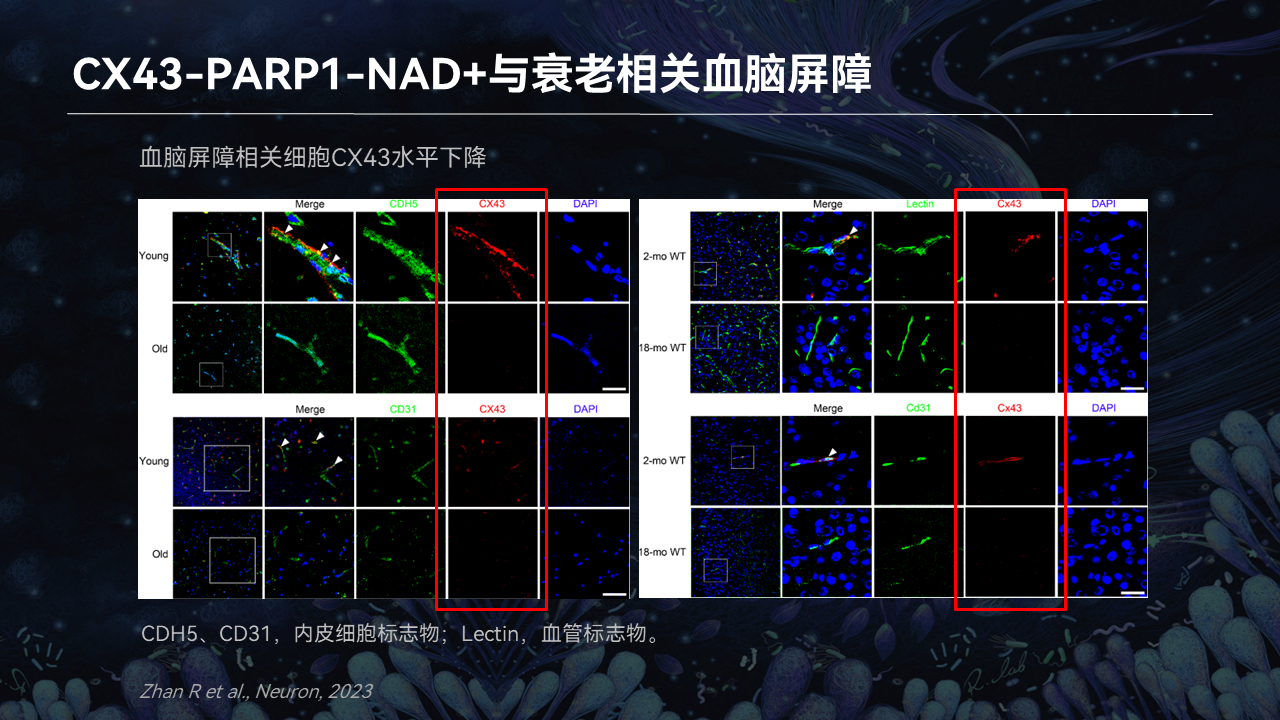
我们发现,随着人和老鼠的变老,内皮细胞中间隙连接蛋白的量会下降。
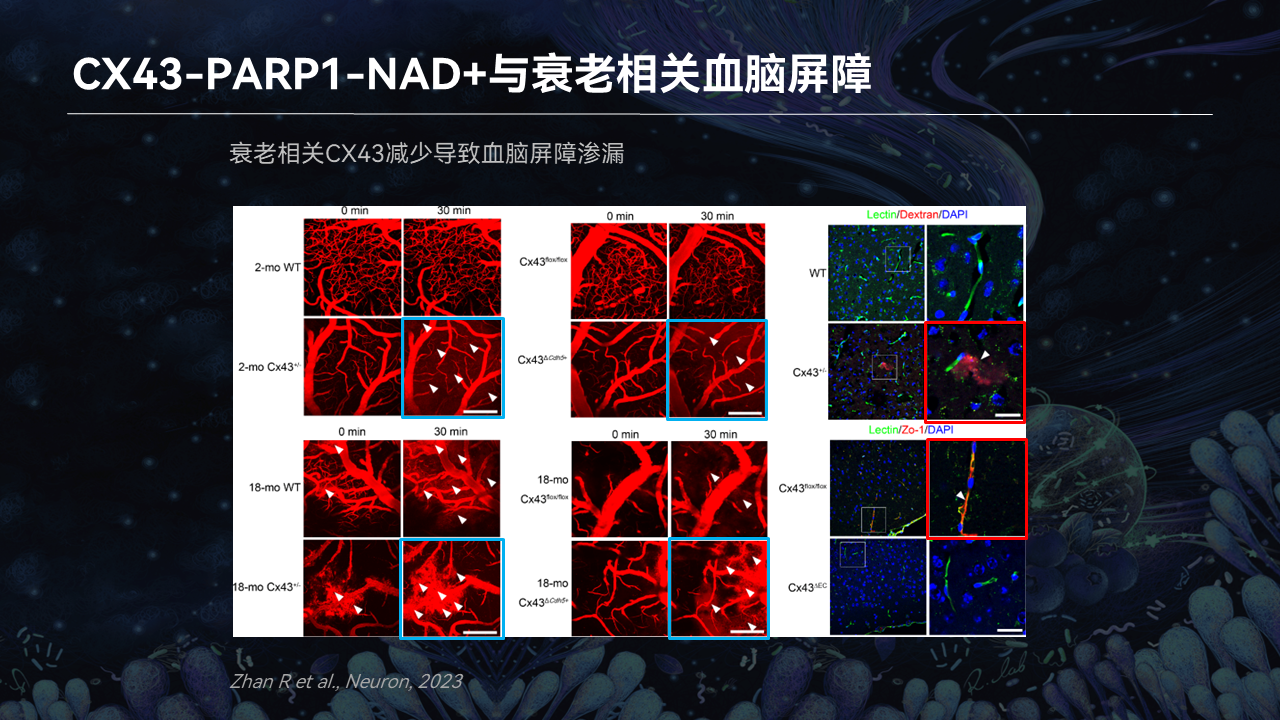
另外我们把小鼠的头盖骨打薄了以后,通过共聚焦的镜头放在头盖骨上,我们可以发现了血管的渗漏。如果我们把内皮细胞Connexin-43基因敲除以后,我们发现渗漏加剧了。
这就表明了人变老,Connexin-43在内皮细胞下降,然后血脑屏障逐渐地打开。

我们就很奇怪,它是不是跟离子通道和半离子通道有关。我们用了离子通道和半离子通道的抑制剂,发现并不是这个原因。
我们做了代谢组学以后发现,能量代谢大量的下降。我们用了NAD的探针发现NAD也下降了,而NAD是能量代谢的重要的中间物。
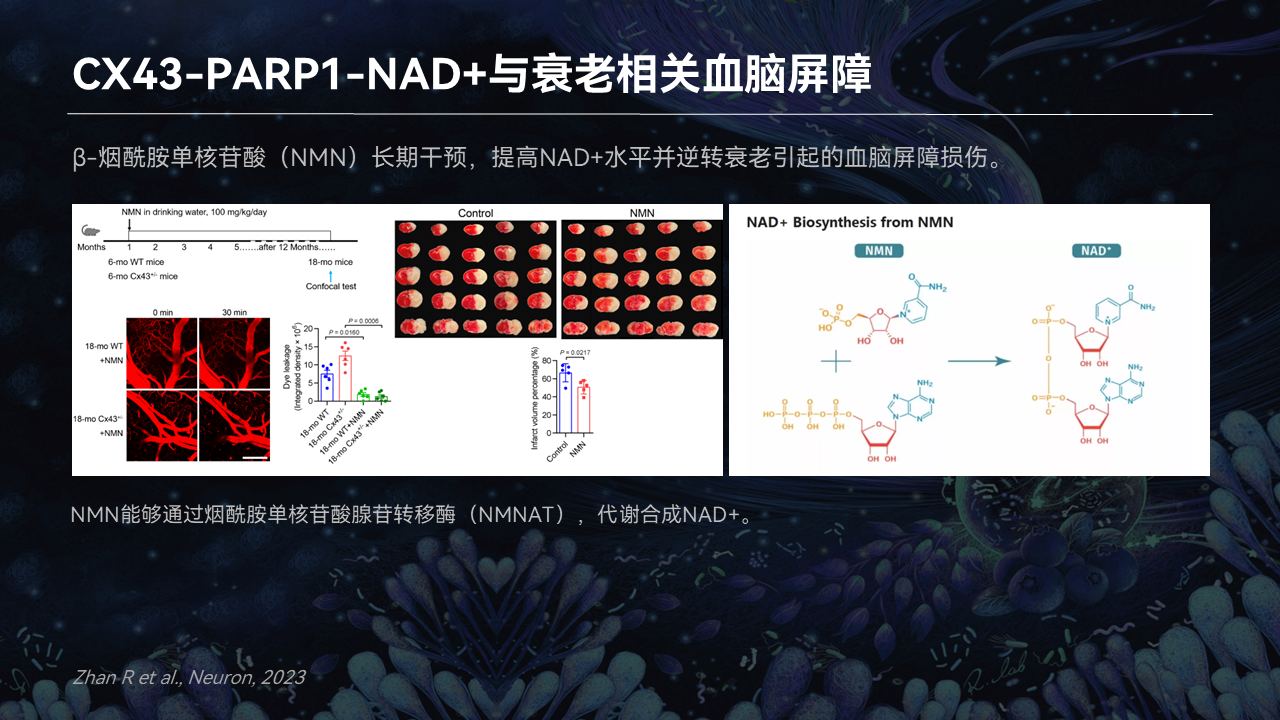
说编委会问我们,你们血脑屏障的打开和什么疾病有关,我们就提到了卒中。我们发现Connexin-43越少,脑梗的面积越大,渗漏越大。
所以我们提出来的理论是,PARP1能消耗NAD,进行DNA的修复。但是如果敲低Connexin-43以后,PARP1会激活并消耗更多的NAD,所以NAD的量就减少了,血脑屏障越打开,他的认知障碍也出来了。

这个研究,我们也是今年发表在Cell 子刊Neuron上。
我们发现,人变老以后血脑屏障逐渐打开,通过单细胞测序发现内皮细胞、平滑肌细胞变少了。在内皮细胞里,我们又发现了Connexin-43的变少,它的能量代谢下降了。为什么能量代谢下降了?因为PARP1激活了。
我们觉得抗衰老的神药,它可能在健康人中不知道会不会起到这么大的作用,但至少在这个疾病模型中它起到了很好的作用,它减少了脑梗的面积、保护了血脑屏障。另外我们用了工具药PARP1的抑制剂,也发现改善了血脑屏障。
所以我觉得NMN可能能作为某种状态下,这种血脑屏障引起的疾病的治疗。它可能不会广泛地用在每一个人的衰老,但对于某种疾病类型,它还是有一定的治疗效果的。
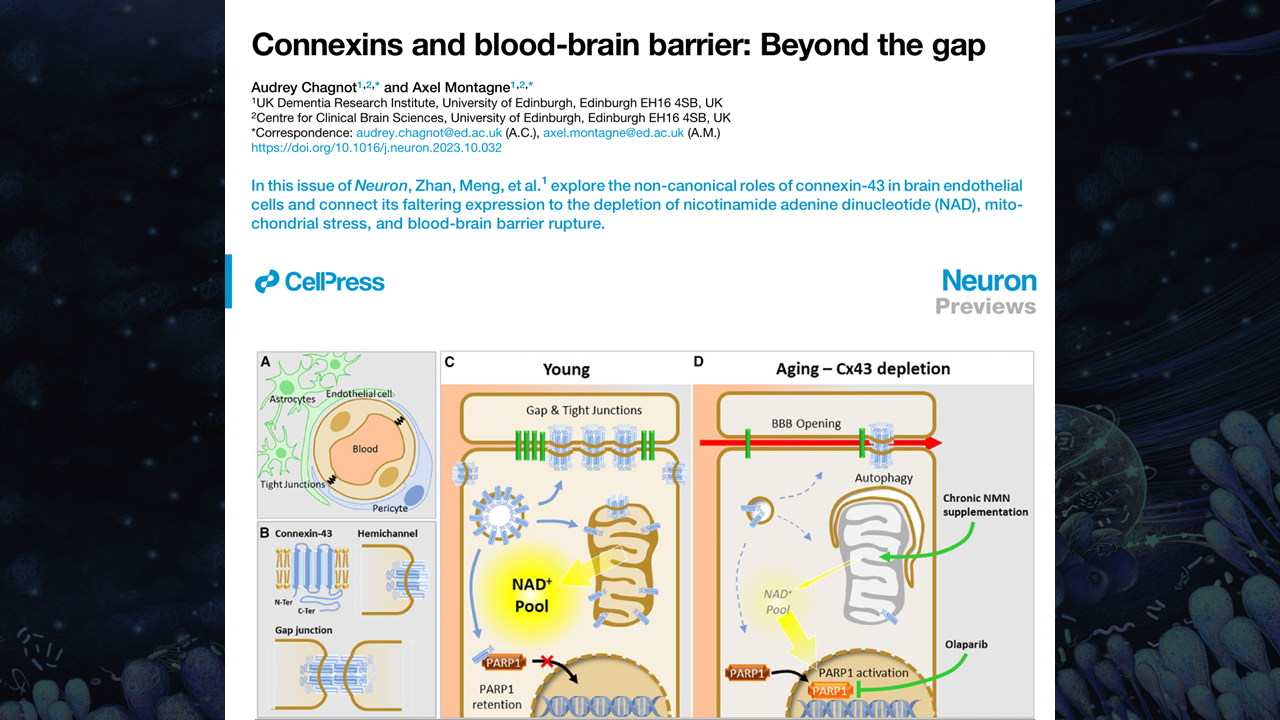
所以说在Neuron上也给我们一个预览(preview),讨论了能量代谢对我们大脑认知的影响,讨论了线粒体的重要性。
在内皮中,我们需要线粒体提供大量的能量,保持内皮细胞的完整性。在Connexin-43敲低了以后,我们也发现线粒体会出现异常的自噬,线粒体的数量也会减少,所以我们确实需要补充能量。
那我们怎么补充能量呢?在这个研究中,我们也提出来了NMN可能能成为补充能量的一个好的底物。所以这个研究也引起了大家很大的关注。

这个是我们的公众号,我们也会发布一些代谢、肠道代谢与心脑血管疾病和相关内分泌疾病影响的内容。
我们实验室的网站是Leminlab.com,欢迎大家多交流,希望对代谢和心脑血管疾病感兴趣的博士生来我们团队做博后。
我们最近在进行菌群改造、基因改造,也期待跟更多的菌群和菌群改造的公司进行合作,研究菌群的各种酶并进行改造,然后改造代谢物,然后将菌群移植到病人的体内,最终发挥心脑血管治疗作用。
希望肠道菌群逐渐会进入心脑血管治疗的第一线,这个是我们的期待。

最后谢谢大家!


