
编者按:
如果说良好的开始是成功的一半,那么,对微生物组研究而言,这个开始就是样本的收集。如果选择错了样本收集或保存方法,可能不仅仅意味着错过了关键的线索,还有可能产生与事实相反的结果。
那么,微生物样本收集和保存过程究竟需要考虑哪些因素呢?不同的方法会对你的研究和后续的实验造成什么影响呢?
今天我们特别编译了加利福尼亚大学圣迭戈分校(UCSD)两位学者发表的关于粪便样品采集和保存的文章。希望该文能够为研究人员和各位读者在微生物样本的收集上提供一些指导和帮助。
粪便样品的“稳定性”
简便且安全地收集人体粪便样品是研究人体微生物组方面的关键。虽然在实验设计中,研究人员所做的重要的决定之一是选择准确的设备试剂,然而由于资金的问题,设备试剂选择时需要考虑的因素很容易被我们忽视。
不幸的是,目前并不存在一种收集方法,可以适合全球不同研究的限制,并满足所有实验室要进行的不同实验的要求。
对于设备试剂的选择,比如化学药品的使用、样本的收集方式、甚至使用的塑料种类都可以引起偏差,同时也会限制和影响样本后续的分子生物学实验。
许多的分子生物学实验的黄金标准是在采集样品后尽快速冻,最好是保存在 -80℃。尽管这一方法在临床研究中是理想且可行的,但是在许多研究中,由于冰柜使用、运费成本和物流的限制,这种方法在实际实施过程中会有一定的困难。
想象一下,携带液氮到印度尼西亚的遥远村落中带来的不便,或者实验参与者在家中收集样本并正确地将样品放置于干冰过夜直至送到实验室中所产生的成本。
因此,许多粪便微生物组研究聚焦于是否存在一种方案,可以使样品在室温下长时间稳定存放。
不过,样品“稳定性”的定义会因实验设计和探究问题的不同而不同。
举例来说,研究人员研究粪便的代谢组学时担心的问题是,在样品中发现的小分子是否还是样品收集时的分子分布,并且不需要去担心 RNA 的降解问题。
相反,研究细菌和古菌分类学组成的科研人员,所担心的是基因组 DNA 组成是否反映了样品收集时的情况,而不会关心使用塑料是否会带来小分子污染。

干湿保存法:有何要注意?
一个收集设备至少应该包含两部分,一是获得样品的方式,二是能够提供安全运送的方式。
保持一个样品稳定的方法,通常是在收集样品的设备(比如拭子)上预先添加保护剂,或者将保护剂作为样品容器的一部分(比如在试管中的 95%乙醇)。
化学保护剂用来抑制特定的生化反应,或者裂解并杀死细胞,或者阻止微生物样品的生长。但是使用化学保护剂的成本较高,所以一些设备会额外采用一些小珠子,提供一种在剧烈摇动时破碎细胞的物理方法,可以实现“在现场”就能够保存基因组 DNA。
广义来讲,样品保存主要分为两个大类:干保存法和湿保存法。
(1)湿保存法是将粪便生物质悬浮于水溶液中。这种方法对细胞、核酸、氨基酸和小分子的影响取决于在溶液中所用到的化学成分。
市售的溶剂,包括 RNALater 和 OMNIgene 是特别为固定样品中的 RNA 或者 DNA 所设计的,这种溶剂中的化学成分可以阻断使核酸降解的细胞进程和酶的生化反应。
如果使用普通 95%的乙醇会破坏细胞壁,导致样品中很大一部分的细胞裂解,导致细胞死亡,从而影响转录组的数据结果,影响差异表达基因的结果。
(2)干保存法是使用棉签或者硬纸板,在其表面可能含有使细胞裂解并固定核酸的粉末。通常,在干保存法中使用的化学成分在设计时就应该考虑到其特定的目标,比如阻断细胞复制。
比如 American Gut 项目,使用一种不含有任何保护剂的干拭子,通过干燥样品使微生物停止生长。但是,当实验人员在拭子中添加过多的样品时,造成湿度的增加可能引起运输过程中细菌生长,并破坏信号。
因此,不含有保护剂的干性拭子或者硬纸板必须尽快在冷冻或速冻的条件下运送,最好还能维持一个低湿度的环境。
总之,所有的这些保存方法(使用或不使用保护剂)都会对微生物细胞造成不同的干扰。这些差异通过许多方式呈现,比如:细胞对缓冲液中细胞裂解物质敏感性的不同,细胞周围物质的变化对保存效果的影响也不同等等。
重要的是,这些不同会导致在样品的最终结果呈现中造成一定的技术偏差,甚至使用的一些化学成分可能会阻碍后续的分子生物学实验。比如,高盐保护剂可能不适用于质谱研究设备中,因为其可能会干扰设备对小分子物质和肽类物质的检测。
收集获得样品的方法
不管使用什么保存方法,物理收集或获得样品都是必须要考虑的一个重要环节。
对生物量要求较大的研究中,比如用于蛋白质组研究的,可以使用医疗便桶。这种放置在马桶圈内的设备,类似一种塑料管,可以收集全部的粪便。在一些情况下,医疗便桶配备一个小勺子,并会提示实验参与者将粪便从便桶收集到一个可能包含保护剂的小瓶中。
可以理解的是,由于需要对粪便进行直接处理,导致发生一些不愉快的经历,可能会把一些实验参与者拒之门外。
如果对生物量的要求较低,比如对扩增子和宏基因组的研究中,其下游步骤仅需要皮克或者纳克的 DNA 量,通常使用的收集设备是棉签拭子。
收集方法是用棉签擦拭使用过的厕纸,使棉签变色即可。接着将棉签放回试管中,或者可以将其折断到试管中。这些试管可能有也可能没有保护剂。
像使用便桶一样,这种方法可能对实验参与者来说也是一种不舒服的经历。但是相比于需要与粪便进行更多接触的勺子采集方法,实验参与者可能更倾向于采用厕纸收集的方法。
保护剂谁更强?
研究人员需要做的进一步的考虑是有关保护剂毒性的问题。保护剂具有较高的毒性是很正常的。毕竟这些试剂的目的是阻断在人体中所发现的分子生物进程。在使用时一定要注意人类和动物的意外中毒。
尽管大部分的化学物质可能是有毒的,但也不全是,比如 95%的乙醇,可以基本认为是安全的,虽然在使用中仍然需要远离小孩和宠物。
另外,还要考虑到保护剂的成本和适用性。
一项由 Rob Knight 团队发表在 mSystems 的研究测试了 5 种保存剂保存人和狗的粪便样本 DNA 的效果,具体为:乙醇(浓度分别为 70%和 95%)和三种市售试剂——RNAlater,OMNIgene Gut(DNA Genotek)和 FAT Card(Whatman)1。
并将每个样本暴露于各种温度环境,包括 -20℃,-4℃ 的恒定温度和环境温度,以及模拟冻融循环和周期性热梯度的温度波动(从 4 ℃ 到 40 ℃)。
结果发现,即使最糟糕的方法,包括那些没有保护剂的方法,依然能够在8周时揭示物种之间以及 1 周后个体之间微生物组的差异。
研究还发现 FAT Card 引起的差异是系统性的,可以消除。同时与其它研究一样,建议不要使用 70%的乙醇。
另一项研究评估了保存剂在代谢组方面的效果2。结果发现,对于非靶向代谢组学,95%的乙醇效果最好,其次为 FAT Card 和 OMNIgene Gut。
不同的保存剂的效果总结如下:
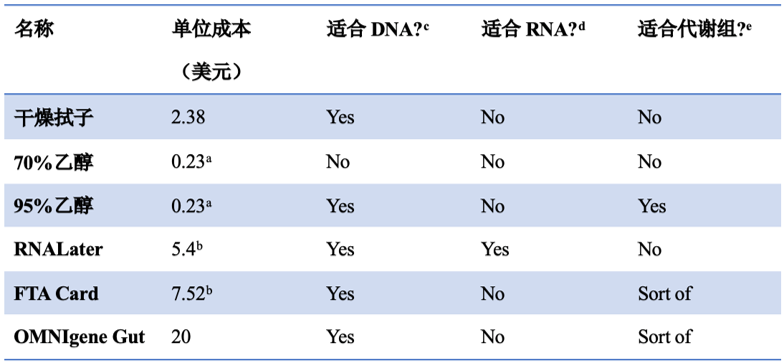
表1:不同保存剂的成本和适用性
【注:除 OMNIgene Gut 外,大部分产品的价格来自于 fishersci.com 网站。对 OMNIgene Gut 成本的估算来源于同行评审的研究。
a:适用于 2ml 的 DNA 样品且不包括收集设备。
b:不包括收集设备。
c:保存剂对 DNA 的适用性结果基于同行评审。
d:RNALater 是唯一已知的用于固定 RNA 的保存剂。
e:保存剂对代谢组的适用性结果基于同行评审。】
如何选择:简单一些?
当考虑到实验中的粪便收集时,最重要的是理解粪便的收集方式、保存方法、运输方法和这些方法导致的对下游分析的影响。
不是所有的设备试剂带来的差异都是相同的,这些差异表现在单位成本、与其他研究比较时的技术偏差、实验限制和与目标人群的兼容性等方面。
针对不同目的的实验,可能会存在不止一种最佳方案,因此在进行任何实验之前,需要与粪便微生物专家进行讨论。
当存在问题时,采用已有研究中的设备试剂和方案是一种合理的策略,因为在这些研究中已经做了一系列比较去减小技术差异。并且就像在科学或者其他领域中那样,宁可简单一些才是合理的策略,尤其是对大型流行病调查而言。
参考文献:
1.Song, Se Jin, et al."Preservation methods differ in fecal microbiome stability, affectingsuitability for field studies." MSystems 1.3 (2016).
2.Wang, Zheng, et al."Comparison of fecal collection methods for microbiome and metabolomicsstudies." Frontiers in cellular and infection microbiology 8(2018): 301.
原文链接:
3.https://www.biotechniques.com/clinical-research/fecal-sample-collection-for-clinical-microbiome-research/
作者|Daniel McDonald、Jack Gilbert
翻译|gemiu
审校|617


